Clear Sky Science · zh
SMARCA4通过调控H3K27乙酰化作用于PROX1,促进前列腺癌谱系可塑性及恩杂鲁胺耐药
这项研究对前列腺癌患者为何重要
患有晚期前列腺癌的男性常接受抑制雄激素的药物治疗,但许多肿瘤最终会绕开这些疗法,以更具侵袭性的形式复发。本研究提出了一个关键问题:在恩杂鲁胺治疗后,是什么让前列腺癌细胞改变其身份,变得更难被杀死且更致命?通过揭示驱动这种形态转变的关键分子开关,该工作指向了可延缓或阻止这一危险演化的新策略。
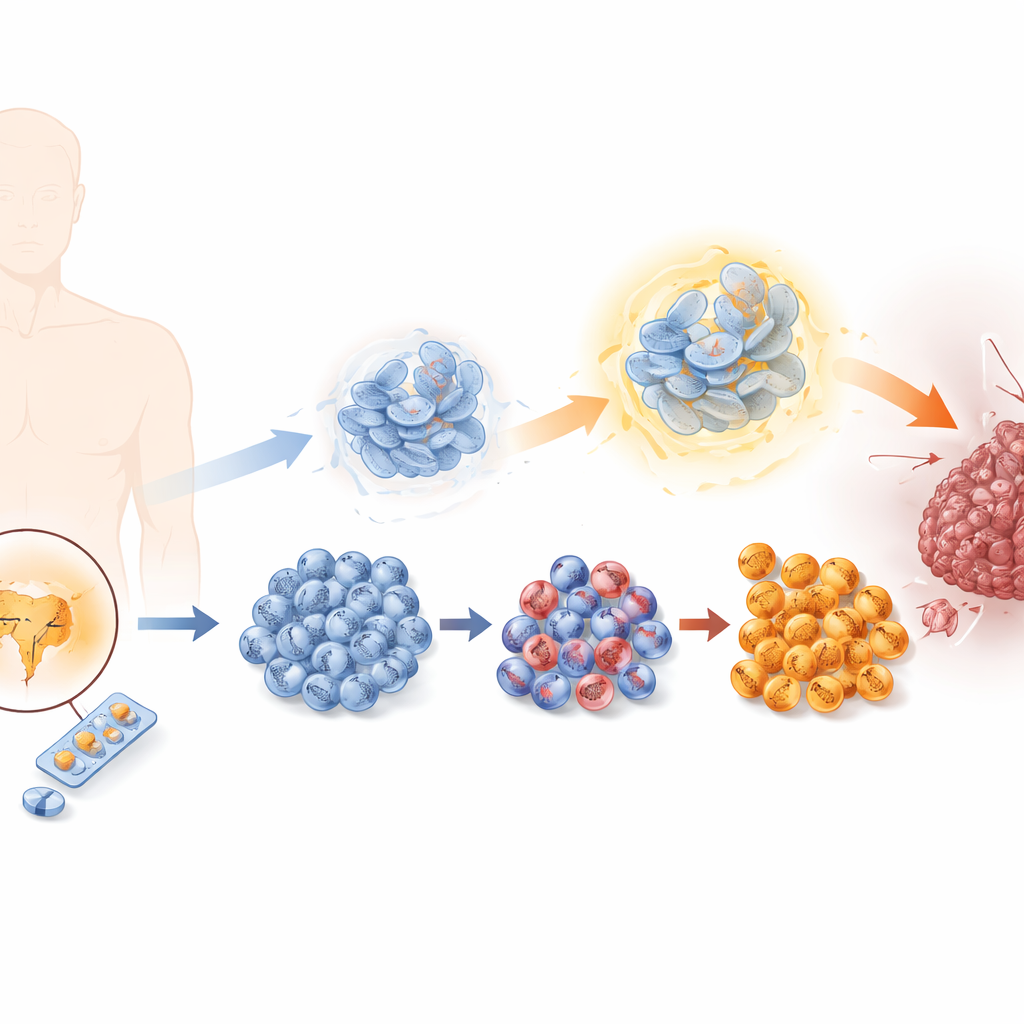
肿瘤如何学会躲避阻断激素的疗法
前列腺癌细胞通常依赖通过雄激素受体传递的雄激素信号。恩杂鲁胺通过阻断该信号起效,但随着时间推移,一些细胞能够逃逸。研究者在实验室中通过让前列腺癌细胞暴露于逐步增加的恩杂鲁胺剂量来重建这一过程,生成了一系列从敏感到高度耐药的细胞系。随着耐药性的增加,细胞增殖加快、迁移更容易、对周围组织的侵袭性增强,这些都是更恶性肿瘤的标志。同时,它们失去了典型前列腺细胞的特征并获得了所谓神经内分泌细胞的性状——这是一种罕见但高度侵袭、治疗选择有限的肿瘤类型。
细胞身份的改变记载在DNA的包装方式中
为了解这些危险性状如何出现,团队超越了DNA序列本身,考察了DNA在细胞核内的包装与展开方式。使用在基因组范围内绘制哪些区域开放、哪些区域紧密缠绕的方法,他们发现耐药性的发展与染色质的广泛重塑同时发生。控制雄激素依赖基因的区域变得不那么可及,而与干细胞样和神经内分泌程序相关的片段则变得开放。这些变化与基因活性的改变密切对应,显示出细胞调控电路的协调性重接线,而不仅仅是随机突变。
一种名为SMARCA4的染色质引擎推动肿瘤走向更致命的状态
在众多改变的调控因子中,SMARCA4尤为突出:它是一个滑动并重构染色质的分子机器的核心组分。在最耐药、类神经内分泌的细胞及侵袭性患者肿瘤中,SMARCA4水平显著升高,且高表达与较差的生存相关。当科学家在耐药细胞中降低SMARCA4表达时,增殖减慢,迁移和侵袭减少,更多细胞进入程序性死亡。重要的是,神经内分泌身份的标记减弱,典型前列腺细胞的特征在培养皿和小鼠肿瘤中部分恢复。这些发现将SMARCA4定位为一个中心引擎,帮助肿瘤既抵抗治疗又采纳更危险的表型。
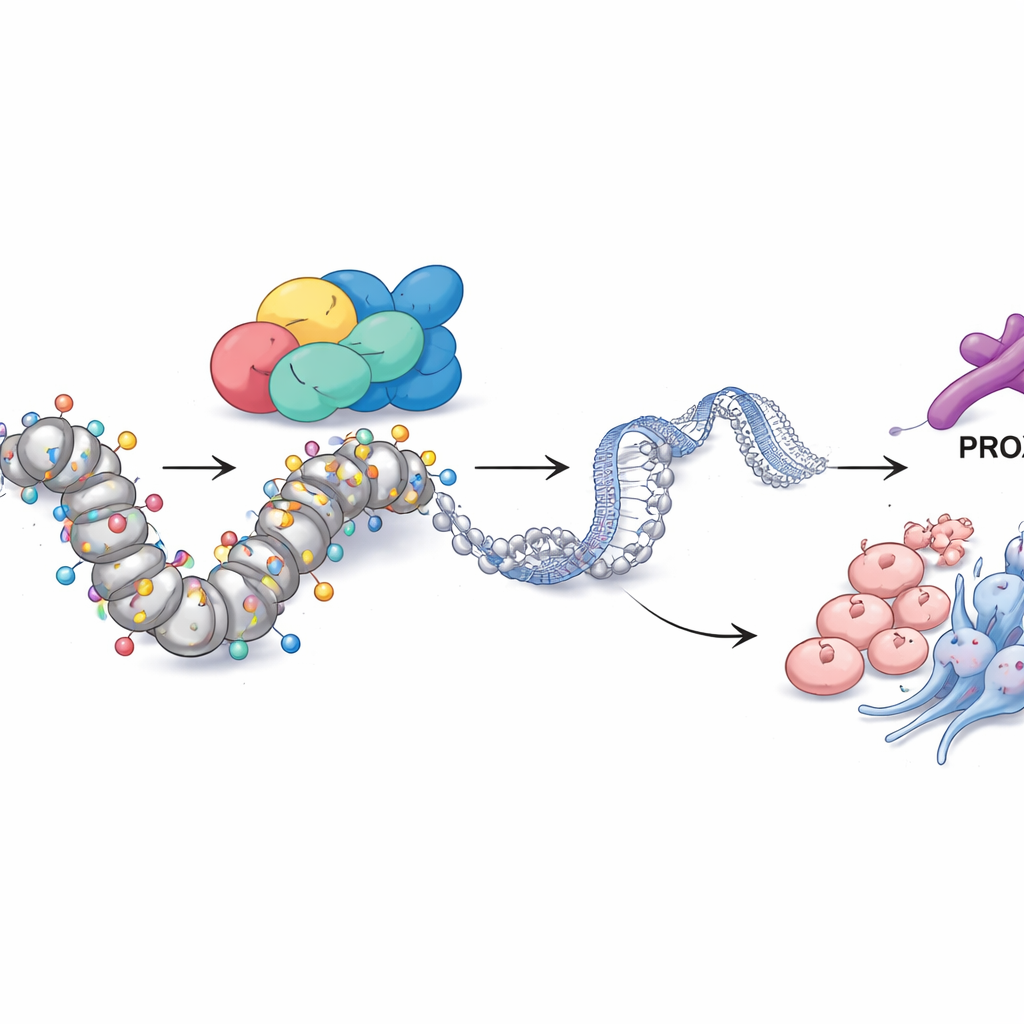
PROX1与化学标记将SMARCA4与肿瘤行为联系起来
更深入挖掘时,团队探究了SMARCA4如何施加如此广泛的控制。通过整合多层基因组数据,他们鉴定出另一种蛋白质——转录因子PROX1,作为关键的合作伙伴。在耐药细胞中,PROX1在基因组中的控制区异常开放,并带有一种活性DNA的化学标记,即被称为H3K27ac的组蛋白乙酰化。SMARCA4直接位于该位点,当降低SMARCA4时,PROX1的表达水平和该区域的H3K27ac都随之下降。单独抑制PROX1就足以减少细胞增殖、侵袭、神经内分泌标记和干细胞样特性,显示出PROX1是SMARCA4程序的重要执行者。值得注意的是,阻断去乙酰化酶(使用组蛋白去乙酰化酶抑制剂)或人为提升PROX1水平在很大程度上能够挽救SMARCA4丧失带来的效应,强调了这一通路通过PROX1位点的乙酰化运行。
这对未来治疗意味着什么
简言之,本研究揭示了一条事件链:在恩杂鲁胺压力下,前列腺癌细胞激活SMARCA4,SMARCA4重塑染色质以增加PROX1位点的乙酰化与激活,这对组合随后帮助细胞放弃原有身份并采用耐药、类神经内分泌的状态。对于患者而言,这表明针对SMARCA4、对乙酰化标记进行添加或移除的酶,或直接针对PROX1的药物,可与标准激素阻断疗法联合使用,以阻止肿瘤演化为这种高风险形式。尽管这些发现仍需在更多人类样本中得到验证,但它们勾勒出一个具体的表观遗传学通路,为临床医生和药物开发者提供了可被针对的方向,以对抗前列腺癌最致命的逃逸途径之一。
引用: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
关键词: 前列腺癌, 药物耐受, 表观遗传学, 神经内分泌转化, 染色质重塑