Clear Sky Science · he
SMARCA4 מקדם פלסטיות של קו תאי ועמידות לאנזלוטמיד בסרטן הערמונית על‑ידי ויסות PROX1 דרך אצטילציה של H3K27
מדוע מחקר זה חשוב למטופלים בסרטן הערמונית
גברים עם סרטן הערמונית מתקדם מטופלים לעתים קרובות בתרופות שמכבות את ההורמונים הזכריים, אך רבות מהגידולים בסופו של דבר מתגברים על הטיפולים וחוזרים בצורה אגרסיבית הרבה יותר. המחקר שואל שאלה מכרעת: מה מאפשר לתאי סרטן הערמונית לשנות את זהותם ולהיות גם קשים יותר להמית וגם קטלניים יותר לאחר טיפול באנזלוטמיד? על ידי גילוי מתג מולקולרי מרכזי המניע את השינוי הזה, העבודה מצביעה על אסטרטגיות חדשות שעשויות לעכב או למנוע את ההתפתחות המסוכנת הזו.
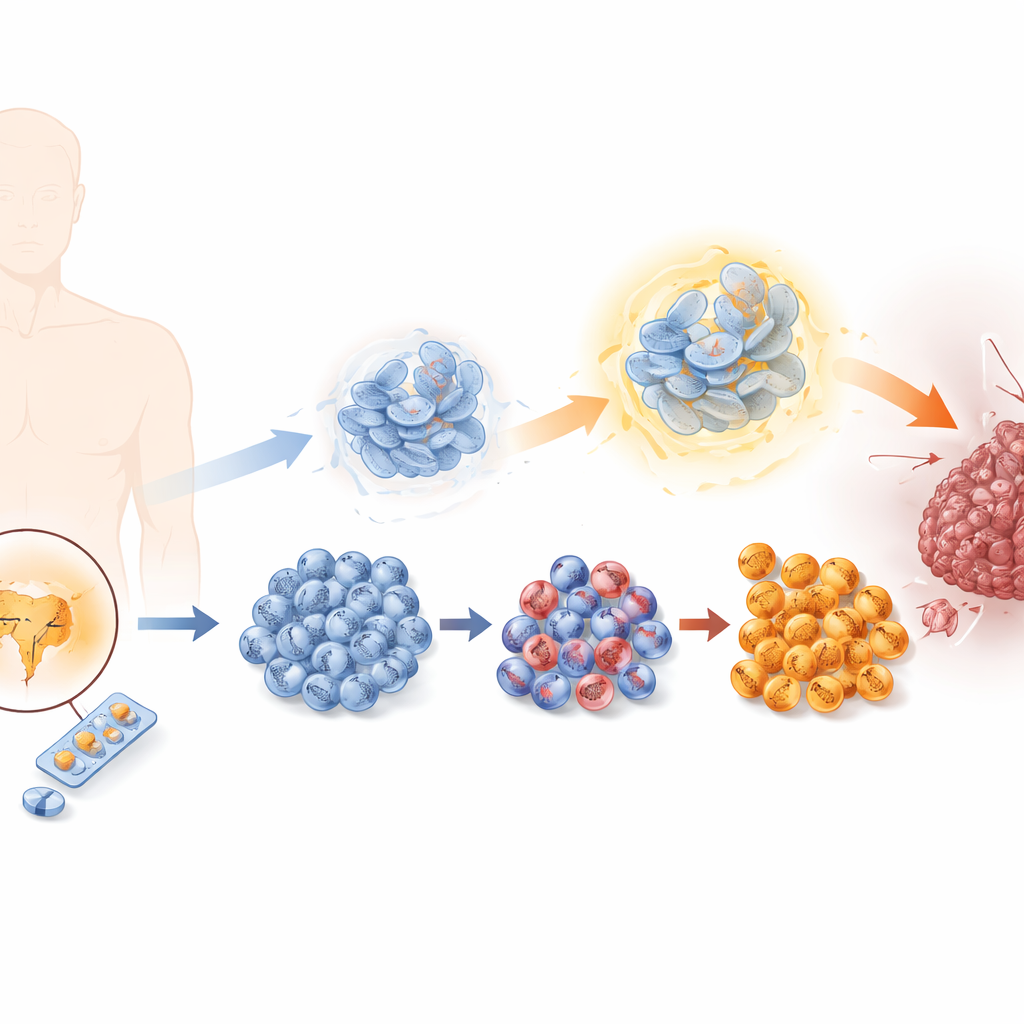
כיצד הגידולים לומדים להתחמק מטיפולים שחוסמים הורמונים
תאי סרטן הערמונית בדרך כלל תלויים בהורמונים זכריים הפועלים דרך קולטני האנדרוגן. אנזלוטמיד פועל על ידי חסימת אות זו, אבל עם הזמן חלק מהתאים מצליחים להימלט. החוקרים שיחזרו תהליך זה במעבדה על‑ידי חשיפת תאי סרטן הערמונית למינונים הולכים ועולים של אנזלוטמיד, ויצרו סדרת קווי תאים שנעו מרגישים לעמידים מאוד. ככל שהעמידות גדלה, התאים התחלקו מהר יותר, נדדו ביתר קלות וחדרו לרקמות מסביב ביתר קלות — כולם סימנים של גידול מזיק יותר. במקביל, הם איבדו מאפיינים טיפוסיים של תאי ערמונית ורכשו תכונות של תאים נוירואנדוקריניים, סוג נדיר אך אגרסיבי עם אפשרויות טיפול מועטות.
שינויים בזהות התאים נכתבים באריזת ה‑DNA
כדי להבין כיצד תכונות מסוכנות אלה צצות, הצוות הביט מעבר לקוד ה‑DNA עצמו אל הדרך שבה ה‑DNA נארז ומתפרש בתוך גרעין התא. באמצעות שיטות רחבות היקף שממפות אילו אזורים ב‑DNA פתוחים ואילו מהודקים, הם מצאו כי העמידות התפתחה לצד שינויים נרחבים בכרומטין, החומר החלבוני‑DNA שמארגן את הגנום. אזורים ששולטים בגנים התלויים באנדרוגן הפכו לפחות נגישים, בעוד מקטעים המקושרים לתכניות דמויות‑גזע ולתכניות נוירואנדוקריניות נפתחו. שינויים אלה תיאמו בצמוד לשינויים בפעילות הגנים, וחושפים כיוונון מחודש מתואם של מעגלי הבקרה התאית ולא רק מוטציות אקראיות.
מנוע כרומטין בשם SMARCA4 דוחף את הגידולים לכיוון מצב קטלני יותר
בין רגולטורים רבים שעברו שינוי, אחד בלט: SMARCA4, מרכיב מרכזי במכונה מולקולרית שמזיזה ומבנית מחדש את הכרומטין. רמות SMARCA4 היו גבוהות בהרבה בתאים שהיו העמידים ביותר ובתאי דמיון נוירואנדוקריני ובגידולים אגרסיביים ממטופלים, ורמות גבוהות נקשרו להישרדות גרועה יותר. כשמדענים הפחיתו את SMARCA4 בתאים עמידים, הגדילה הועטה, הנדידה והחדירה פחתו, ויותר תאים עברו מוות מתוכנת. מהותי, סמנים של זהות נוירואנדוקרינית דהו ותכונות של תאי ערמונית טיפוסיים שבו והופיעו, הן במנות תרבית והן בגידולים בעכברים. ממצאים אלה מציבים את SMARCA4 כמנוע מרכזי המסייע לגידולים גם לעמוד בטיפול וגם לאמץ פרסונה מסוכנת יותר.
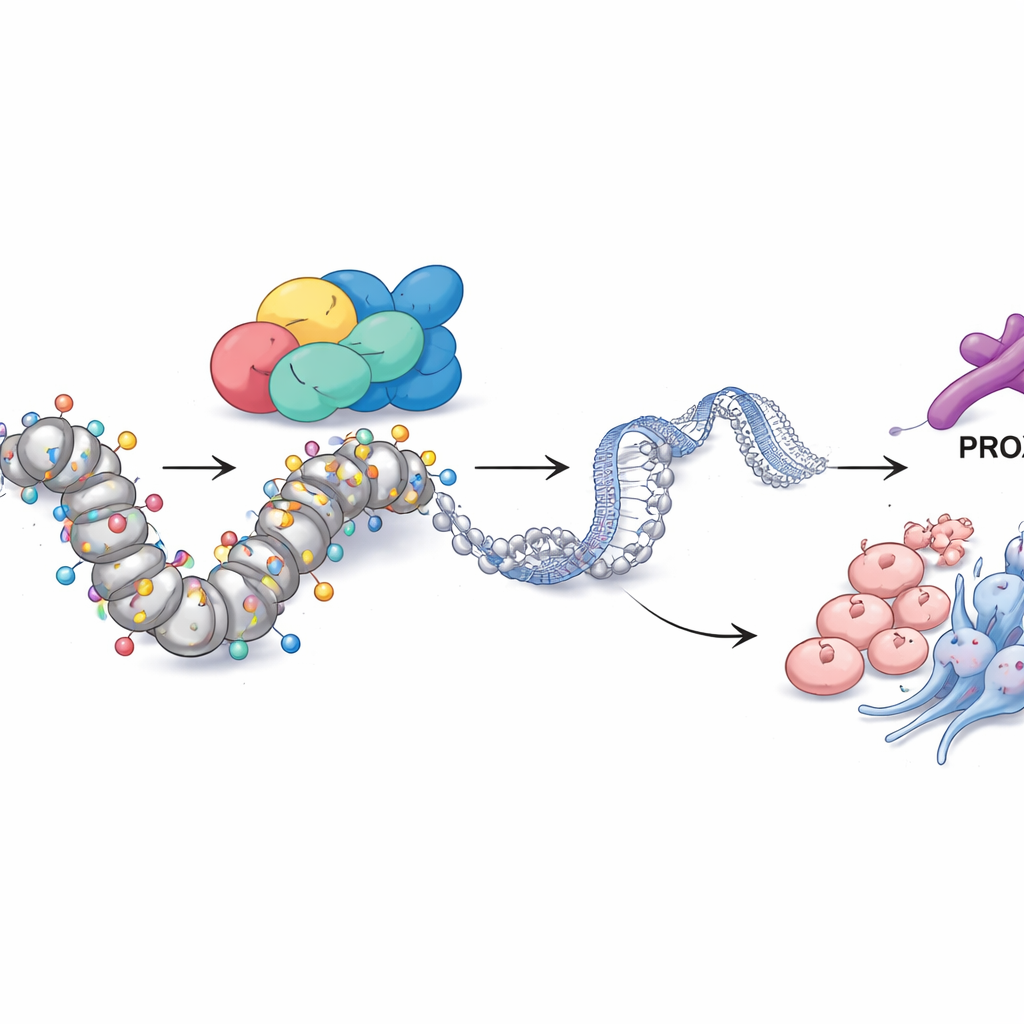
PROX1 ותויות כימיות מקשרות את SMARCA4 להתנהגות הגידול
בהעמקה נוספת, הצוות חקר כיצד SMARCA4 מפעיל שליטה כה רחבת היקף. באמצעות שילוב שכבות נתונים גנומיים שונות, הם זיהו חלבון נוסף — גורם השעתוק PROX1 — כשותף מרכזי. בתאים עמידים, אזור הבקרה של PROX1 בגנום היה פתוח באופן בלתי רגיל ומקושט בסימן כימי של DNA פעיל, סוג של אצטילציה בהיסטון הידועה כ‑H3K27ac. SMARCA4 נשב בדיוק באתר זה, וכאשר הפחיתו את SMARCA4, הן רמות PROX1 והן H3K27ac באזור זה ירדו. השתקת PROX1 לבדה הספיקה לצמצם גדילה, חדירה, סמנים נוירואנדוקריניים ותכונות דמויות‑גזע, מה שמראה כי PROX1 פועל כמבצע חשוב בתכנית של SMARCA4. באופן ראוי לציון, חסימת אנזימים שמסירים קבוצות אצטיל (עם מעכב דה‑אצטילאז היסטונים) או חיזוק מלאכותי של PROX1 יכלו בשיעור גדול להחזיר את ההשפעה של אבדן SMARCA4, ובכך מדגישים שהמסלול הזה פועל דרך אצטילציה בלוקוס של PROX1.
מה משמעות הדבר עבור טיפולים עתידיים
בקיצור, המחקר חושף שרשרת אירועים: תחת לחץ אנזלוטמיד, תאי סרטן הערמונית מדליקים את SMARCA4, שמעצב מחדש את הכרומטין כדי להגביר אצטילציה והפעלה של PROX1, והצמד הזה מסייע לתאים להפטר מהזהות המקורית שלהם ולאמץ מצב עמיד בדמיון נוירואנדוקריני. עבור מטופלים, משמעות הדבר היא שתרופות המכוונות ל‑SMARCA4, לאנזימים שמוסיפים או מסירים תגי אצטיל, או ל‑PROX1 עצמו יכולות להיות משולבות עם טיפולים סטנדרטיים שחוסמים הורמונים כדי למנוע מהגידולים להתפתח לצורה עם סיכון גבוה זו. על אף שהממצאים דורשים עדיין אימות בדוגמאות אנושיות, הם מסמנים מסלול אפיגנטי מוחשי שאנשי רפואת אונקולוגיה ומפתחי תרופות יכולים כעת למקד במטרה להילחם באחד ממסלולי ההימלטות הקטלניים ביותר בסרטן הערמונית.
ציטוט: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
מילות מפתח: סרטן הערמונית, עמידות לתרופות, אפיגנטיקה, טרנספורמציה נוירואנדוקרינית, שחזור כרומטין