Clear Sky Science · it
SMARCA4 promuove la plasticità di linea e la resistenza a enzalutamide nel cancro della prostata regolando PROX1 tramite acetilazione di H3K27
Perché questa ricerca è importante per i pazienti con cancro della prostata
Gli uomini con cancro prostatico avanzato vengono spesso trattati con farmaci che sopprimono gli ormoni maschili, ma molti tumori finiscono per eludere queste terapie e ricompaiono in una forma molto più aggressiva. Questo studio pone una domanda cruciale: che cosa permette alle cellule del cancro della prostata di cambiare identità e diventare sia più difficili da eliminare sia più letali dopo il trattamento con enzalutamide? Identificando un interruttore molecolare chiave che guida questo cambiamento di forma, il lavoro indica nuove strategie che potrebbero ritardare o prevenire questa pericolosa evoluzione.
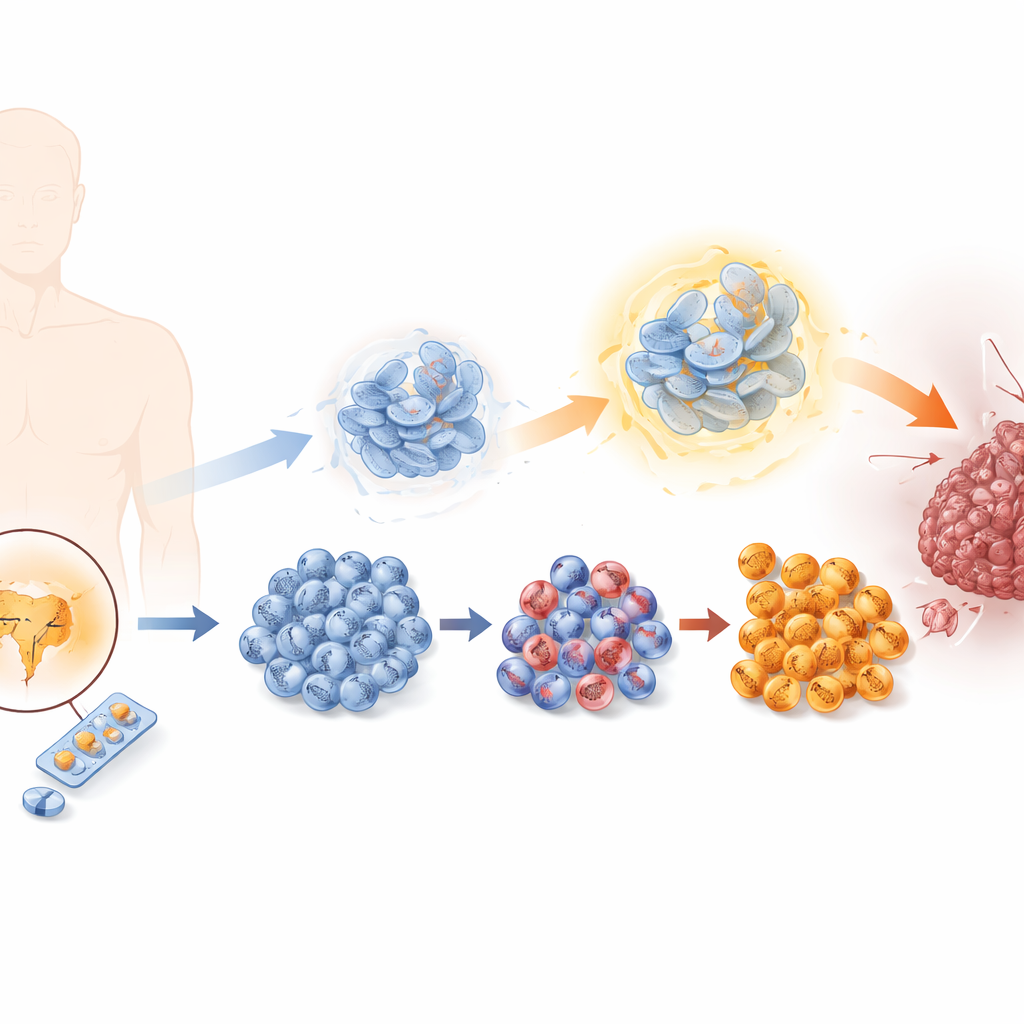
Come i tumori imparano a eludere la terapia che blocca gli ormoni
Le cellule del cancro della prostata dipendono solitamente dagli ormoni maschili che agiscono tramite il recettore degli androgeni. L’enzalutamide funziona bloccando questo segnale, ma col tempo alcune cellule riescono a sfuggire. I ricercatori hanno ricreato questo processo in laboratorio esponendo le cellule prostatiche a dosi crescenti di enzalutamide, generando una serie di linee cellulari che andavano da sensibili a altamente resistenti. Con l’aumentare della resistenza, le cellule proliferavano più rapidamente, migravano più facilmente e invadevano più prontamente i tessuti circostanti, tutti segni di un tumore più maligno. Allo stesso tempo, persero caratteristiche tipiche delle cellule prostatiche e acquisirono tratti delle cosiddette cellule neuroendocrine, un tipo tumorale raro ma molto aggressivo con poche opzioni terapeutiche.
I cambiamenti di identità cellulare sono scritti nel confezionamento del DNA
Per comprendere come emergono questi tratti pericolosi, il gruppo ha guardato oltre il codice del DNA stesso, esaminando il modo in cui il DNA è impacchettato e srotolato all’interno del nucleo cellulare. Utilizzando metodi su scala genomica che mappano quali regioni del DNA sono aperte e quali sono strettamente avvolte, hanno scoperto che lo sviluppo della resistenza avveniva di pari passo con cambiamenti estesi nella cromatina, il complesso proteina–DNA che organizza il genoma. Le regioni che controllano i geni dipendenti dagli androgeni diventavano meno accessibili, mentre porzioni associate a programmi di tipo staminale e neuroendocrino si aprivano. Questi spostamenti si allineavano strettamente con cambiamenti nell’attività genica, rivelando una riorganizzazione coordinata del circuito regolatorio delle cellule piuttosto che sole mutazioni casuali.
Un motore della cromatina chiamato SMARCA4 spinge i tumori verso uno stato più letale
Tra i numerosi regolatori alterati, uno è emerso in modo particolare: SMARCA4, un componente chiave di una macchina molecolare che scivola e ristruttura la cromatina. I livelli di SMARCA4 erano molto più alti nelle cellule più resistenti e di tipo neuroendocrino e nei tumori aggressivi dei pazienti, e valori elevati erano associati a una sopravvivenza peggiore. Quando gli scienziati ridussero SMARCA4 nelle cellule resistenti, la crescita rallentò, la migrazione e l’invasione diminuirono e più cellule andarono incontro ad apoptosi. Importante, i marcatori di identità neuroendocrina si attenuarono e riemersero tratti tipici delle cellule prostatiche, sia in colture che in tumori murini. Questi risultati pongono SMARCA4 come un motore centrale che aiuta i tumori sia a resistere al trattamento sia ad assumere una personalità più pericolosa.
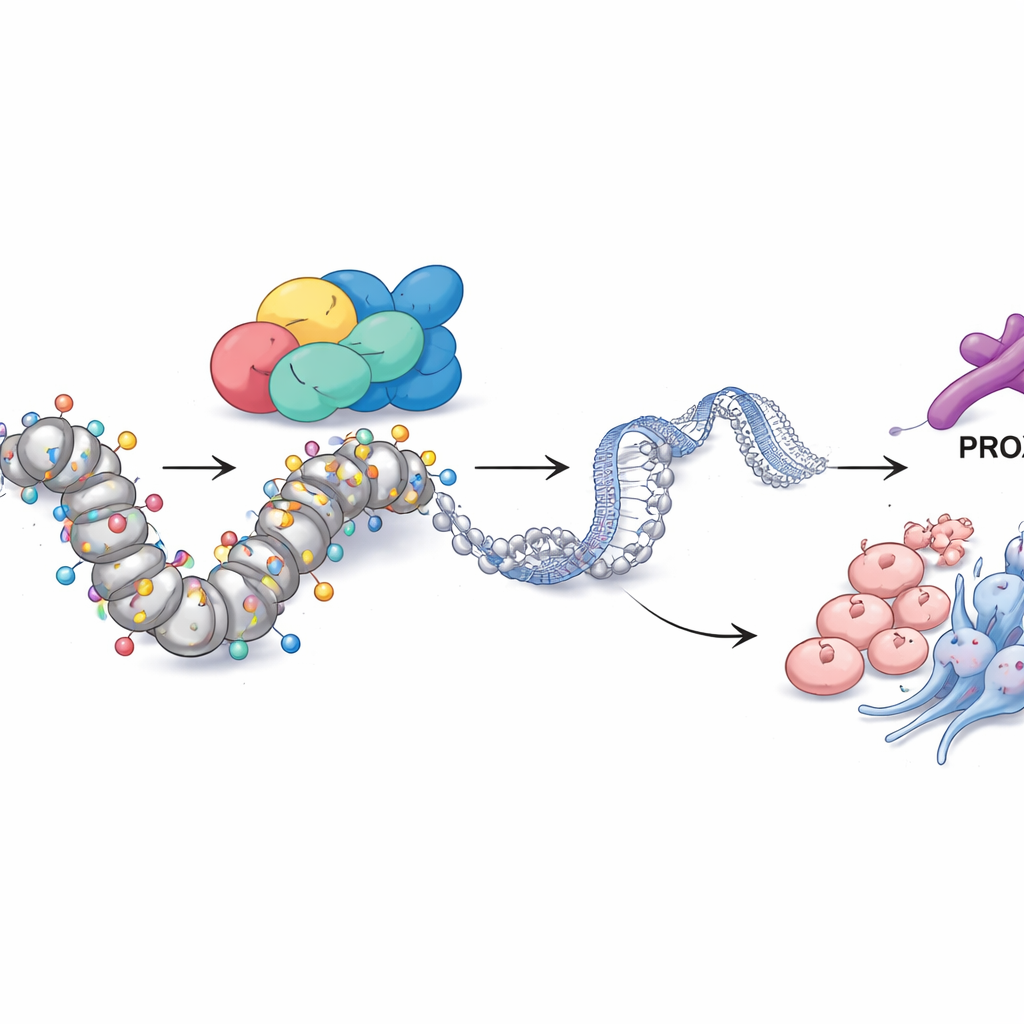
PROX1 e le etichette chimiche collegano SMARCA4 al comportamento tumorale
Approfondendo, il team ha indagato come SMARCA4 eserciti un controllo così ampio. Integrando più livelli di dati genomici hanno identificato un’altra proteina, il fattore di trascrizione PROX1, come partner chiave. Nelle cellule resistenti, la regione di controllo genomica di PROX1 era insolitamente aperta e decorata con un segnale chimico di DNA attivo, un tipo di acetilazione degli istoni noto come H3K27ac. SMARCA4 era presente direttamente in questo sito e, quando SMARCA4 veniva ridotto, sia i livelli di PROX1 sia H3K27ac in quella regione diminuivano. L’abbassamento di PROX1 da solo era sufficiente a ridurre la crescita cellulare, l’invasione, i marcatori neuroendocrini e le proprietà di tipo staminale, dimostrando che PROX1 agisce come un esecutore importante del programma di SMARCA4. Notevolmente, bloccare gli enzimi che rimuovono gruppi acetile (con un inibitore delle deacetilasi degli istoni) o aumentare artificialmente PROX1 poteva in gran parte compensare la perdita di SMARCA4, sottolineando che questa via opera attraverso l’acetilazione nel locus di PROX1.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio rivela una catena di eventi: sotto la pressione dell’enzalutamide, le cellule del cancro prostatico attivano SMARCA4, che rimodella la cromatina per aumentare l’acetilazione e l’attivazione di PROX1; questa coppia aiuta poi le cellule a perdere la loro identità originale e ad assumere uno stato resistente e simile al neuroendocrino. Per i pazienti, ciò suggerisce che farmaci mirati a SMARCA4, agli enzimi che aggiungono o rimuovono marche acetiliche, o allo stesso PROX1 potrebbero essere combinati con le terapie ormonali standard per impedire ai tumori di evolvere in questa forma ad alto rischio. Sebbene questi risultati richiedano ancora conferma in campioni umani, delineano una via epigenetica concreta che clinici e sviluppatori di farmaci possono ora prendere di mira per combattere una delle vie di fuga più letali nel cancro della prostata.
Citazione: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Parole chiave: cancro della prostata, resistenza ai farmaci, epigenetica, trasformazione neuroendocrina, rimodellamento della cromatina