Clear Sky Science · ru
SMARCA4 способствует пластичности клеточной линии и резистентности к энзалутамиду при раке предстательной железы, регулируя PROX1 через ацетилирование H3K27
Почему это исследование важно для пациентов с раком предстательной железы
Мужчин с распространённым раком предстательной железы часто лечат препаратами, блокирующими мужские гормоны, но многие опухоли в конце концов обходят эти терапии и возвращаются в значительно более агрессивной форме. В этом исследовании поставлен ключевой вопрос: что позволяет клеткам рака предстательной железы изменять свою идентичность и становиться одновременно труднее убиваемыми и более смертоносными после лечения энзалутамидом? Выявив важный молекулярный переключатель, который приводит к этой смене «роли», работа указывает на новые стратегии, которые могли бы отсрочить или предотвратить это опасное развитие событий.
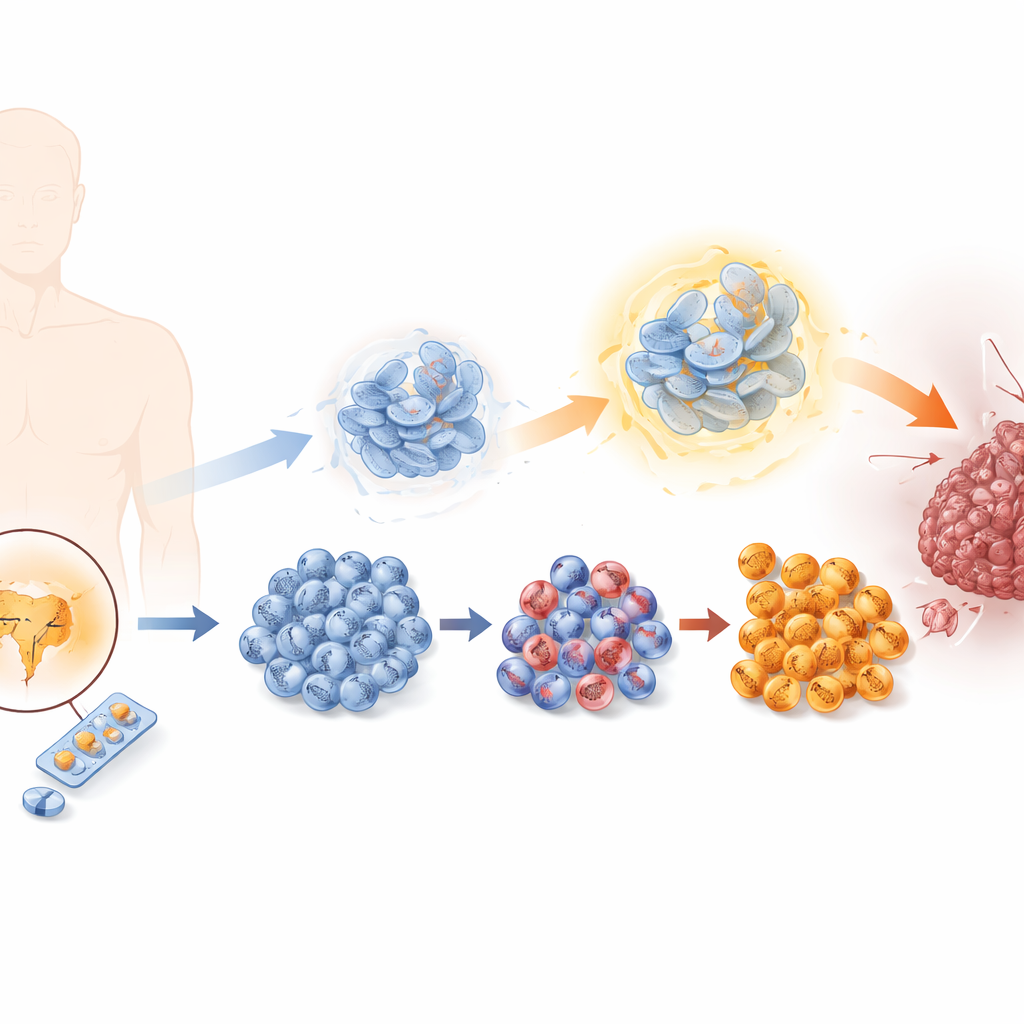
Как опухоли учатся избегать терапии, блокирующей гормоны
Клетки рака предстательной железы обычно зависят от действия мужских гормонов через андрогеновый рецептор. Энзалутамид действует, блокируя этот сигнал, но со временем некоторые клетки ускользают. Исследователи воссоздали этот процесс в лаборатории, подвергая клетки постепенному увеличению доз энзалутамида, получив серию линий клеток — от чувствительных до сильно резистентных. По мере нарастания резистентности клетки делились быстрее, легче мигрировали и активнее вторгались в окружающие ткани — все признаки более злокачественной опухоли. Одновременно они теряли признаки типичных предстательных клеток и приобретали черты так называемых нейроэндокринных клеток — редкого, но очень агрессивного типа опухоли с ограниченными вариантами лечения.
Изменения идентичности клеток зафиксированы в упаковке ДНК
Чтобы понять, как появляются эти опасные свойства, команда посмотрела за пределы самой последовательности ДНК на то, как ДНК упакована внутри ядра клетки. С помощью методов скрининга по всему геному, которые отображают, какие участки ДНК открыты, а какие плотно свернуты, они обнаружили, что развитие резистентности сопровождается масштабными изменениями в хроматине — белково‑ДНКовой матрице, организующей геном. Участки, контролирующие андроген‑зависимые гены, становились менее доступными, тогда как области, связанные со стволовыми и нейроэндокринными программами, открывались. Эти сдвиги хорошо коррелировали с изменениями активности генов, указывая на координированную перенастройку регуляторной схемы клеток, а не только на случайные мутации.
Хроматиновый «двигатель» SMARCA4 толкает опухоли к более опасному состоянию
Среди множества изменённых регуляторов выделялся один: SMARCA4, ключевой компонент молекулярного механизма, который передвигает и перестраивает хроматин. Уровни SMARCA4 были намного выше в наиболее резистентных, похожих на нейроэндокринные, клетках и в агрессивных опухолях пациентов, и высокая экспрессия связывалась с худшей выживаемостью. Когда учёные снизили SMARCA4 в резистентных клетках, рост замедлился, миграция и инвазия уменьшились, а больше клеток прошло запрограммированную гибель. Важно, что маркёры нейроэндокринной идентичности ослабли, а признаки типичных предстательных клеток вновь появились — как в культурных чашках, так и в опухолях мышей. Эти результаты показывают, что SMARCA4 действует как центральный двигатель, способствующий и резистентности к лечению, и приобретению опухолями более опасной «персоны».
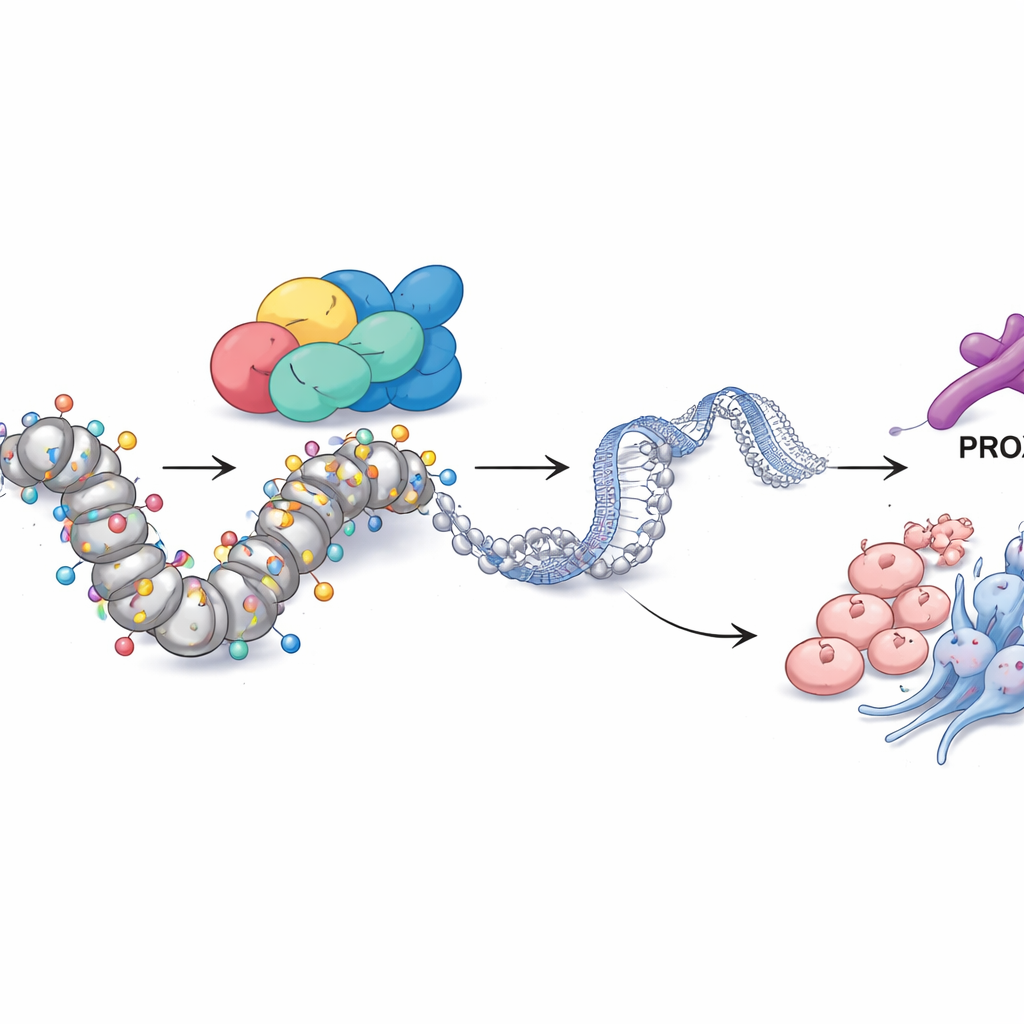
PROX1 и химические метки связывают SMARCA4 с поведением опухоли
Углубившись, команда выяснила, как SMARCA4 обеспечивает такое широкое управление. Интегрируя несколько слоёв геномных данных, они выделили ещё один белок — транскрипционный фактор PROX1 — как ключевого партнёра. В резистентных клетках регуляторная область PROX1 в геноме была необычно открыта и украшена химической меткой активной ДНК — типом ацетилирования гистона, известным как H3K27ac. SMARCA4 находился непосредственно в этой зоне, и при снижении SMARCA4 как уровни PROX1, так и H3K27ac в этой области падали. Понижение только PROX1 было достаточно, чтобы уменьшить рост клеток, инвазию, выражение нейроэндокринных маркёров и стволоподобные свойства, показывая, что PROX1 выступает важным исполнителем программы SMARCA4. Примечательно, что блокирование ферментов, снимающих ацетильные группы (с помощью ингибитора гистондеацетилаз), или искусственное повышение PROX1 в значительной степени компенсировало потерю SMARCA4, подчёркивая, что этот путь проходит через ацетилирование в локусе PROX1.
Что это значит для будущих методов лечения
Проще говоря, исследование выявляет цепочку событий: под давлением энзалутамида клетки рака предстательной железы включают SMARCA4, который перестраивает хроматин, усиливая ацетилирование и активацию PROX1; эта пара затем помогает клеткам утратить исходную идентичность и принять резистентное, похожее на нейроэндокринное состояние. Для пациентов это означает, что препараты, нацеленные на SMARCA4, ферменты, ставящие или снимающие ацетильные метки, или на сам PROX1, могут быть объединены со стандартной гормональной терапией, чтобы не дать опухолям развиться в эту высокорискованную форму. Хотя эти выводы требуют подтверждения на образцах человека, они очерчивают конкретный эпигенетический путь, по которому теперь могут работать клиницисты и разработчики лекарств для борьбы с одним из самых опасных путей уклонения при раке предстательной железы.
Цитирование: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Ключевые слова: рак предстательной железы, лекарственная резистентность, эпигенетика, нейроэндокринная трансформация, ремоделирование хроматина