Clear Sky Science · pl
SMARCA4 promuje plastyczność linii komórkowej i oporność na enzalutamid w raku prostaty przez regulację PROX1 za pośrednictwem acetylacji H3K27
Dlaczego te badania są ważne dla pacjentów z rakiem prostaty
Mężczyźni z zaawansowanym rakiem prostaty często są leczeni lekami blokującymi hormony męskie, lecz wiele guzów ostatecznie omija te terapie i pojawia się w znacznie bardziej agresywnej formie. To badanie stawia kluczowe pytanie: co pozwala komórkom raka prostaty zmienić swoją tożsamość i stać się jednocześnie trudniejszymi do zlikwidowania oraz bardziej śmiertelnymi po leczeniu enzalutamidem? Odkrycie istotnego przełącznika molekularnego napędzającego tę metamorfozę wskazuje nowe strategie, które mogą opóźnić lub zapobiec temu niebezpiecznemu rozwojowi.
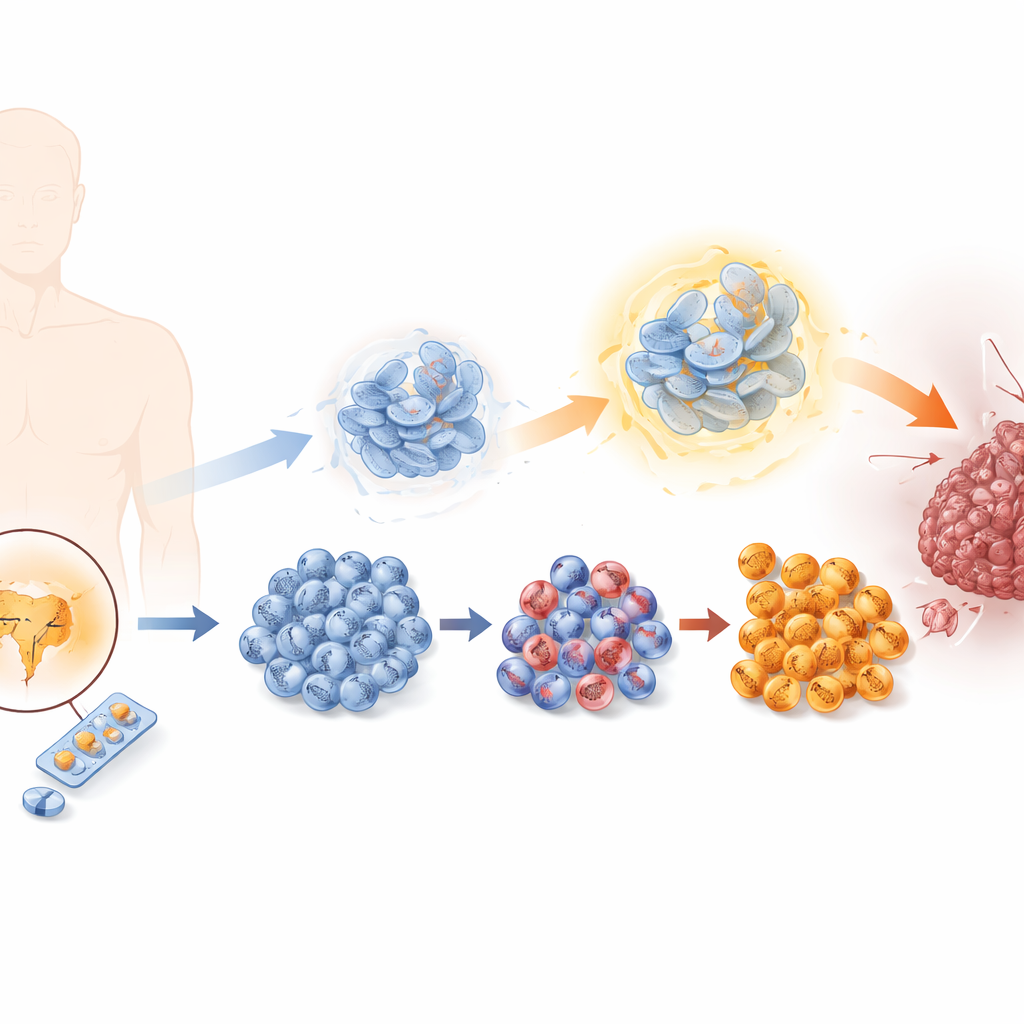
Jak guzy uczą się unikać terapii blokującej hormony
Komórki raka prostaty zwykle zależą od hormonów męskich działających przez receptor androgenowy. Enzalutamid działa, blokując ten sygnał, lecz z czasem niektóre komórki się wymykają. Naukowcy odtworzyli ten proces w laboratorium, eksponując komórki raka prostaty na stopniowo rosnące dawki enzalutamidu, tworząc serię linii komórkowych od wrażliwych do wysoko odpornych. Wraz ze wzrostem oporności komórki dzieliły się szybciej, przemieszczały się łatwiej i bardziej inwazyjnie naciekały otaczające tkanki — wszystkie cechy bardziej złośliwego guza. Równocześnie traciły cechy typowych komórek prostaty i zdobywały właściwości komórek neuroendokrynnych, rzadkiego lecz wysoce agresywnego typu guza z ograniczonymi opcjami leczenia.
Zmiany tożsamości komórkowej są zapisane w upakowaniu DNA
Aby zrozumieć, jak pojawiają się te niebezpieczne cechy, zespół spojrzał poza sam kod DNA na to, jak DNA jest pakowane i rozpakowywane w jądrze komórkowym. Korzystając z metod omicznych mapujących, które regiony DNA są otwarte, a które ściśle zwinięte, odkryli, że rozwój oporności szedł w parze z daleko idącymi zmianami w chromatynie — białkowo‑DNA materiałem organizującym genom. Regiony kontrolujące geny zależne od androgenów stawały się mniej dostępne, podczas gdy obszary związane z programami typu „staminalnego” i neuroendokrynnymi otwierały się. Te przesunięcia ściśle korelowały ze zmianami aktywności genów, ukazując skoordynowane przeprogramowanie układu regulacyjnego komórek, a nie jedynie przypadkowe mutacje.
Silnik chromatynowy o nazwie SMARCA4 popycha guzy w kierunku bardziej śmiertelnego stanu
Wśród wielu zmienionych regulatorów wyróżniał się jeden: SMARCA4, kluczowy składnik molekularnej maszyny przesuwającej i przebudowującej chromatynę. Poziomy SMARCA4 były znacznie wyższe w komórkach najbardziej odpornych, przypominających typ neuroendokrynny, oraz w agresywnych guzach pacjentów, a wysoka ekspresja wiązała się z gorszym przeżyciem. Gdy naukowcy zmniejszyli ilość SMARCA4 w komórkach odpornych, wzrost spowolnił, migracja i inwazja zmalały, a więcej komórek przeszło zaprogramowaną śmierć. Co ważne, markery tożsamości neuroendokrynnej zanikły, a cechy typowych komórek prostaty pojawiły się na nowo, zarówno w hodowlach komórkowych, jak i w guzach mysich. Wyniki te stawiają SMARCA4 jako centralny „silnik”, który pomaga guzom zarówno opierać się leczeniu, jak i przyjmować bardziej niebezpieczną postać.
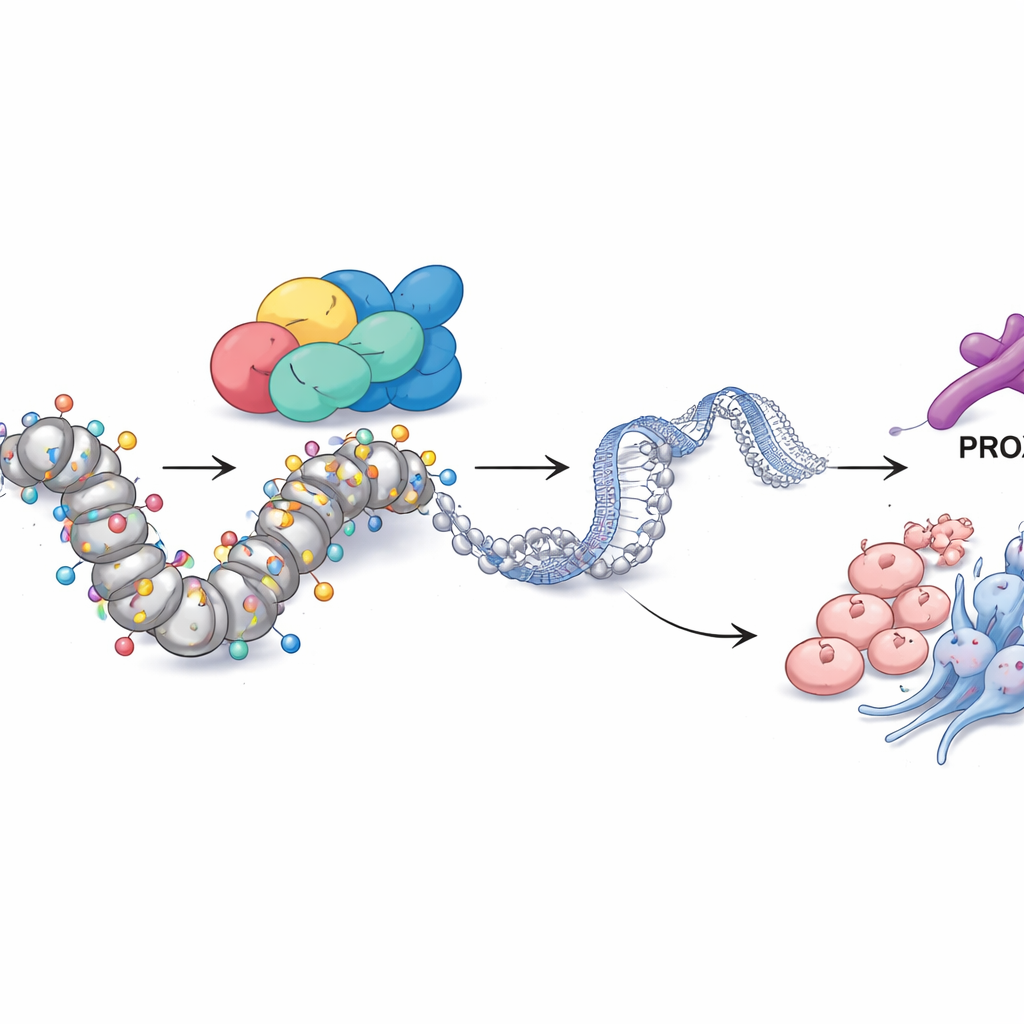
PROX1 i chemiczne znaczniki łączą SMARCA4 z zachowaniem guza
Sięgając głębiej, zespół zapytał, jak SMARCA4 wywiera tak szeroką kontrolę. Poprzez integrację kilku warstw danych genomowych zidentyfikowali kolejny proteinowy czynnik — czynnik transkrypcyjny PROX1 — jako kluczowego partnera. W komórkach odpornych obszar kontrolny PROX1 w genomie był wyjątkowo otwarty i ozdobiony chemicznym znacznikiem aktywnego DNA — rodzajem acetylacji histonów znanej jako H3K27ac. SMARCA4 znajdował się bezpośrednio w tym miejscu, a gdy SMARCA4 został zmniejszony, zarówno poziomy PROX1, jak i H3K27ac w tym regionie spadły. Przytłumienie PROX1 samo w sobie wystarczyło, by ograniczyć wzrost komórek, inwazję, markery neuroendokrynne i cechy przypominające komórki macierzyste, pokazując, że PROX1 działa jako istotny egzekutor programu SMARCA4. Co istotne, zablokowanie enzymów usuwających grupy acetylowe (przy użyciu inhibitora deacetylaz histonowych) lub sztuczne zwiększenie PROX1 mogło w dużej mierze zrekompensować utratę SMARCA4, podkreślając, że ta ścieżka przebiega przez acetylację w locus PROX1.
Co to oznacza dla przyszłych terapii
Mówiąc wprost, badanie ujawnia łańcuch zdarzeń: pod presją enzalutamidu komórki raka prostaty włączają SMARCA4, które przekształca chromatynę, zwiększając acetylację i aktywację PROX1; ten duet pomaga komórkom zrzucić pierwotną tożsamość i przyjąć stan odporny, przypominający neuroendokrynny. Dla pacjentów sugeruje to, że leki celujące w SMARCA4, enzymy umieszczające lub usuwające znaczniki acetylowe albo sam PROX1 mogłyby być łączone ze standardową terapią blokującą hormony, by zapobiegać ewolucji guzów w tę wysokiego ryzyka formę. Choć wyniki te wymagają dalszego potwierdzenia w próbkach ludzkich, wskazują konkretną epigenetyczną ścieżkę, którą klinicyści i twórcy leków mogą teraz atakować, by zwalczyć jedną z najgroźniejszych dróg ucieczki raka prostaty.
Cytowanie: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Słowa kluczowe: rak prostaty, oporność na leki, epigenetyka, transformacja neuroendokrynna, remodeling chromatyny