Clear Sky Science · fr
SMARCA4 favorise la plasticité de lignée et la résistance à l’enzalutamide dans le cancer de la prostate en régulant PROX1 via l’acétylation de H3K27
Pourquoi cette recherche importe pour les patients atteints de cancer de la prostate
Les hommes atteints d’un cancer de la prostate avancé sont souvent traités par des médicaments qui interrompent les hormones masculines, mais de nombreuses tumeurs finissent par contourner ces thérapies et réapparaissent sous une forme beaucoup plus agressive. Cette étude pose une question cruciale : qu’est‑ce qui permet aux cellules du cancer de la prostate de changer d’identité et de devenir à la fois plus difficiles à éliminer et plus mortelles après un traitement par enzalutamide ? En mettant au jour un commutateur moléculaire clé qui pilote cette métamorphose, le travail met en évidence de nouvelles stratégies susceptibles de retarder ou d’empêcher cette évolution dangereuse.
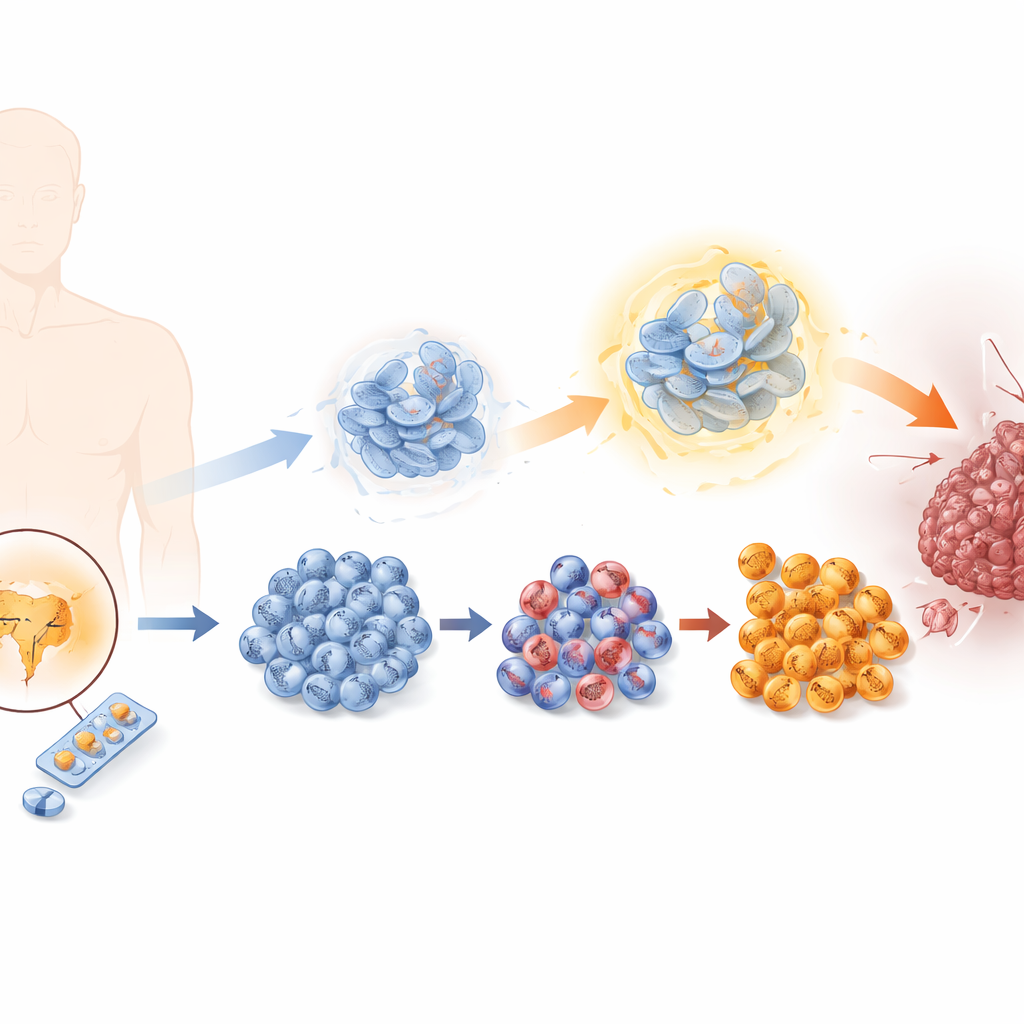
Comment les tumeurs apprennent à échapper à la thérapie anti‑hormonale
Les cellules du cancer de la prostate dépendent généralement des hormones masculines agissant via le récepteur des androgènes. L’enzalutamide bloque ce signal, mais avec le temps certaines cellules s’en échappent. Les chercheurs ont recréé ce processus en laboratoire en exposant des cellules de cancer de la prostate à des doses d’enzalutamide progressivement croissantes, générant une série de lignées cellulaires allant de sensibles à fortement résistantes. À mesure que la résistance augmentait, les cellules proliféraient plus rapidement, migraient plus facilement et envahissaient davantage les tissus voisins, autant de signes d’une tumeur plus maligne. Parallèlement, elles perdaient les traits des cellules prostatiques typiques et acquéraient des caractéristiques de cellules dites neuroendocrines, un type de tumeur rare mais très agressif et peu pourvu d’options thérapeutiques.
Les changements d’identité cellulaire sont inscrits dans l’emballage de l’ADN
Pour comprendre comment ces traits dangereux émergent, l’équipe a regardé au‑delà du code ADN lui‑même, en étudiant la manière dont l’ADN est enroulé et déroulé à l’intérieur du noyau cellulaire. En utilisant des méthodes à l’échelle du génome qui cartographient les régions d’ADN ouvertes et celles étroitement compactées, ils ont constaté que la résistance se développait de concert avec des changements profonds de la chromatine, le matériau protéine–ADN qui organise le génome. Les régions contrôlant les gènes dépendants des androgènes devenaient moins accessibles, tandis que des segments liés aux programmes de type souche et neuroendocrine s’ouvraient. Ces basculements concordaient étroitement avec des modifications de l’activité génique, révélant une reprogrammation coordonnée du circuit régulateur des cellules plutôt que de simples mutations aléatoires.
Un moteur de chromatine nommé SMARCA4 pousse les tumeurs vers un état plus mortel
Parmi les nombreux régulateurs altérés, un s’est distingué : SMARCA4, un composant central d’une machinerie moléculaire qui déplace et restructure la chromatine. Les niveaux de SMARCA4 étaient nettement plus élevés dans les cellules les plus résistantes et de type neuroendocrine et dans les tumeurs agressives de patients, et des niveaux élevés étaient associés à une survie plus mauvaise. Lorsque les scientifiques ont réduit SMARCA4 dans les cellules résistantes, la croissance a ralenti, la migration et l’invasion ont diminué, et davantage de cellules ont subi l’apoptose. De manière importante, les marqueurs d’identité neuroendocrine se sont estompés et des caractéristiques de cellules prostatiques typiques sont réapparues, à la fois en culture et dans des tumeurs de souris. Ces résultats positionnent SMARCA4 comme un moteur central qui aide les tumeurs à la fois à résister au traitement et à adopter une personnalité plus dangereuse.
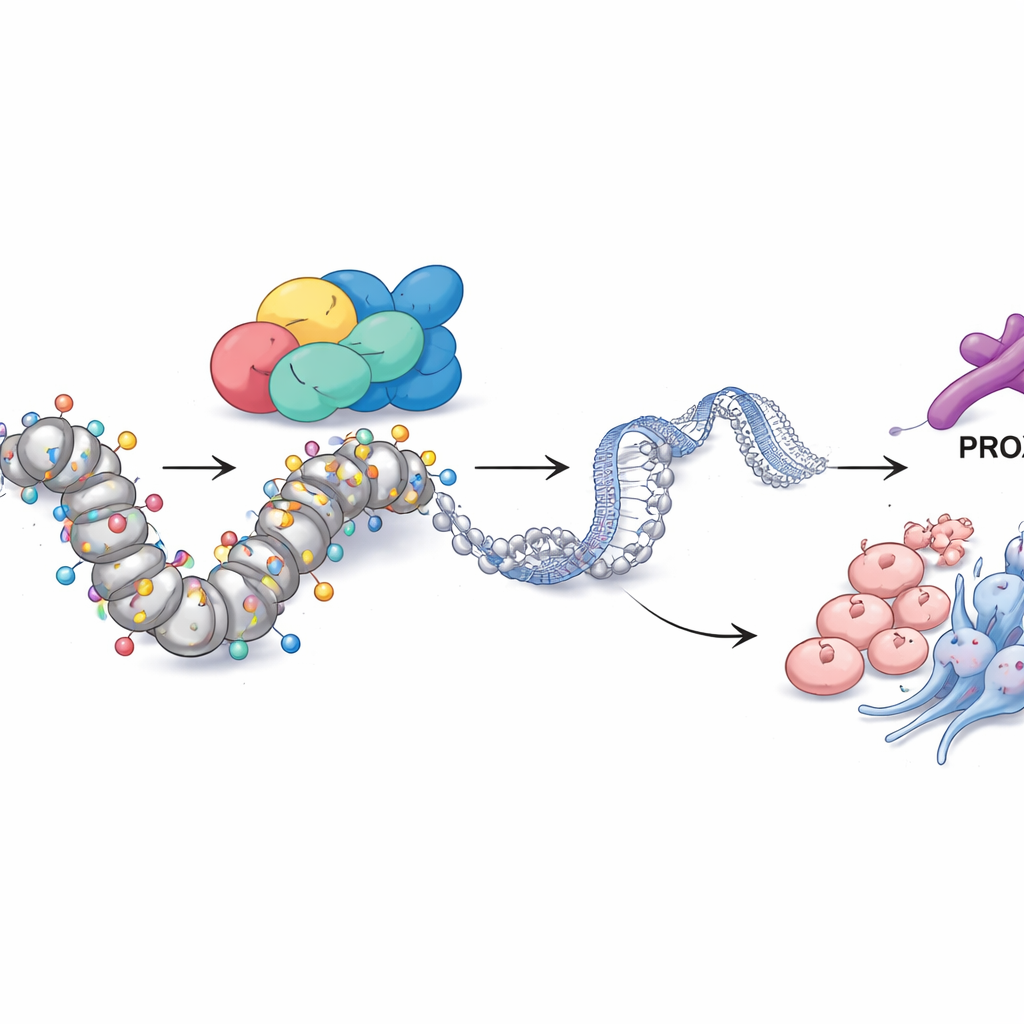
PROX1 et les marques chimiques relient SMARCA4 au comportement tumoral
En creusant plus avant, l’équipe a cherché comment SMARCA4 exerce un contrôle aussi étendu. En intégrant plusieurs couches de données génomiques, ils ont identifié une autre protéine, le facteur de transcription PROX1, comme un partenaire clé. Dans les cellules résistantes, la région de contrôle de PROX1 dans le génome était inhabituellement ouverte et décorée d’une marque chimique d’ADN actif, un type d’acétylation des histones connu sous le nom de H3K27ac. SMARCA4 se trouvait directement à cet endroit, et lorsque SMARCA4 était réduit, à la fois les niveaux de PROX1 et le H3K27ac à cette région diminuaient. Abaisser PROX1 seul suffisait à réduire la croissance cellulaire, l’invasion, les marqueurs neuroendocrines et les propriétés de type souche, montrant que PROX1 agit comme un exécuteur important du programme de SMARCA4. De façon remarquable, bloquer les enzymes qui retirent les groupes acétyle (avec un inhibiteur des histone désacétylases) ou augmenter artificiellement PROX1 pouvait en grande partie compenser la perte de SMARCA4, soulignant que cette voie fonctionne via l’acétylation au locus PROX1.
Ce que cela signifie pour les traitements futurs
En termes simples, l’étude révèle une chaîne d’événements : sous la pression de l’enzalutamide, les cellules du cancer de la prostate activent SMARCA4, qui remodèle la chromatine pour augmenter l’acétylation et l’activation de PROX1, et ce duo aide ensuite les cellules à abandonner leur identité d’origine et à adopter un état résistant de type neuroendocrine. Pour les patients, cela suggère que des médicaments ciblant SMARCA4, les enzymes qui posent ou enlèvent les marques d’acétylation, ou PROX1 lui‑même pourraient être combinés aux thérapies hormonales standard pour empêcher les tumeurs d’évoluer vers cette forme à haut risque. Bien que ces résultats doivent encore être confirmés sur des échantillons humains, ils tracent une voie épigénétique concrète que cliniciens et développeurs de médicaments peuvent désormais cibler pour combattre l’une des voies d’évasion les plus meurtrières du cancer de la prostate.
Citation: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Mots-clés: cancer de la prostate, résistance aux médicaments, épigénétique, transformation neuroendocrine, remodelage de la chromatine