Clear Sky Science · pt
SMARCA4 promove plasticidade de linhagem e resistência à enzalutamida no câncer de próstata regulando PROX1 via acetilação de H3K27
Por que esta pesquisa importa para pacientes com câncer de próstata
Homens com câncer de próstata avançado costumam ser tratados com drogas que suprimem os hormônios masculinos, mas muitos tumores acabam superando essas terapias e retornam numa forma muito mais agressiva. Este estudo faz uma pergunta crucial: o que permite que células do câncer de próstata mudem sua identidade e se tornem simultaneamente mais difíceis de eliminar e mais letais após o tratamento com enzalutamida? Ao desvendar um interruptor molecular chave que dirige essa transformação, o trabalho aponta para novas estratégias que podem retardar ou prevenir essa evolução perigosa.
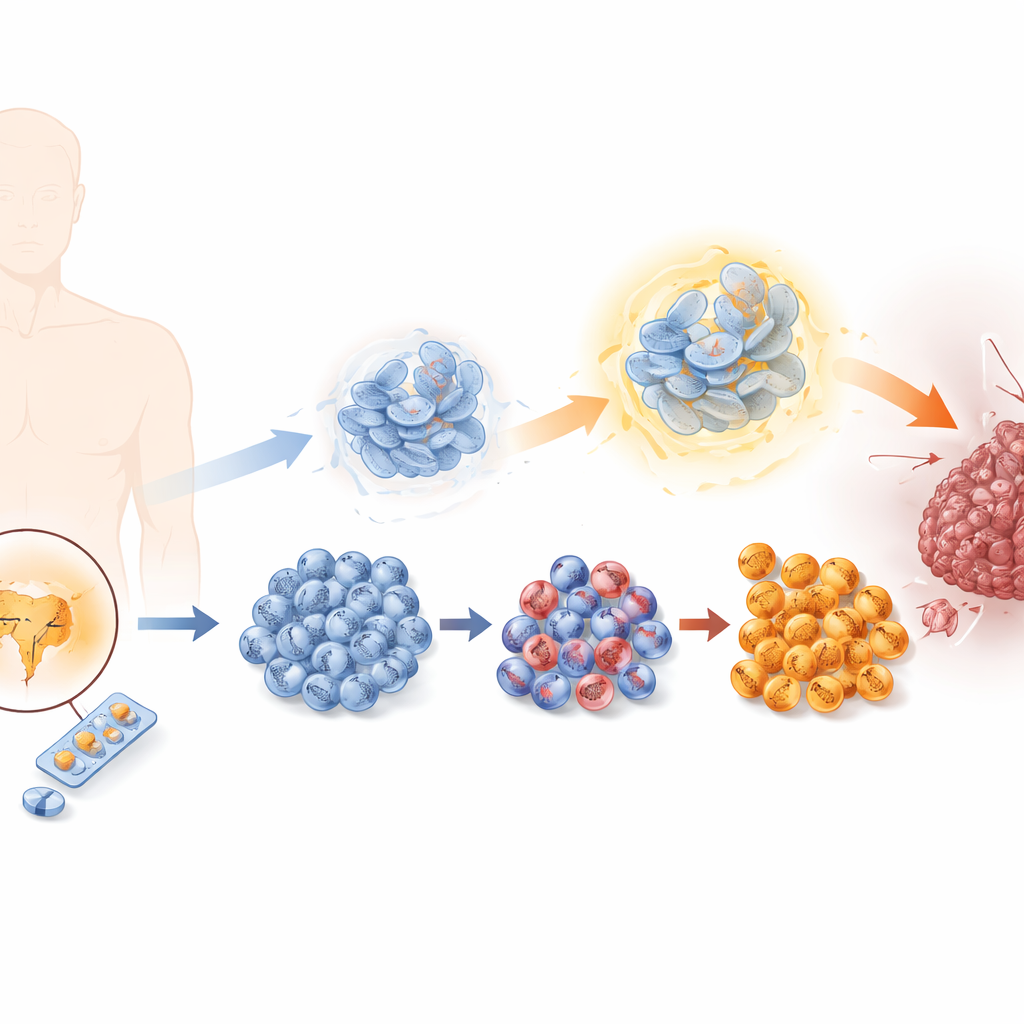
Como os tumores aprendem a escapar da terapia que bloqueia hormônios
As células do câncer de próstata geralmente dependem dos hormônios masculinos atuando pelo receptor de andrógeno. A enzalutamida funciona bloqueando esse sinal, mas com o tempo algumas células escapam. Os pesquisadores recriaram esse processo em laboratório expondo células de câncer de próstata a doses crescentes de enzalutamida, gerando uma série de linhagens celulares que variaram de sensíveis a altamente resistentes. À medida que a resistência aumentou, as células se dividiam mais rápido, migravam com mais facilidade e invadiam tecidos vizinhos com maior frequência — todas características de um tumor mais maligno. Ao mesmo tempo, perderam traços de células prostáticas típicas e ganharam características de células chamadas neuroendócrinas, um tipo raro, porém altamente agressivo, com poucas opções de tratamento.
Mudanças na identidade celular estão escritas na forma como o DNA é embalado
Para entender como essas características perigosas emergem, a equipe olhou além do próprio código de DNA para a maneira como o DNA é compactado e descompactado dentro do núcleo celular. Usando métodos em escala genômica que mapeiam quais regiões do DNA estão acessíveis e quais estão fortemente enroladas, eles descobriram que a resistência se desenvolveu em paralelo com alterações abrangentes na cromatina, o material proteína–DNA que organiza o genoma. Regiões que controlam genes dependentes de andrógeno tornaram-se menos acessíveis, enquanto trechos ligados a programas semelhantes a células-tronco e neuroendócrinos se abriram. Essas mudanças acompanharam de perto alterações na atividade gênica, revelando uma reprogramação coordenada dos circuitos regulatórios das células, e não apenas mutações ao acaso.
Um motor da cromatina chamado SMARCA4 empurra os tumores para um estado mais letal
Entre muitos reguladores alterados, um se destacou: SMARCA4, um componente central de uma máquina molecular que desliza e reestrutura a cromatina. Os níveis de SMARCA4 foram muito mais altos nas células mais resistentes e com fenótipo semelhante ao neuroendócrino e em tumores agressivos de pacientes, e níveis elevados se associaram a pior sobrevida. Quando os cientistas reduziram SMARCA4 em células resistentes, o crescimento desacelerou, a migração e a invasão diminuíram, e mais células passaram por morte celular programada. Importante, marcadores de identidade neuroendócrina enfraqueceram e traços de células prostáticas típicas ressurgiram, tanto em culturas quanto em tumores de camundongos. Esses achados posicionam SMARCA4 como um motor central que ajuda os tumores tanto a resistir ao tratamento quanto a adotar uma personalidade mais perigosa.
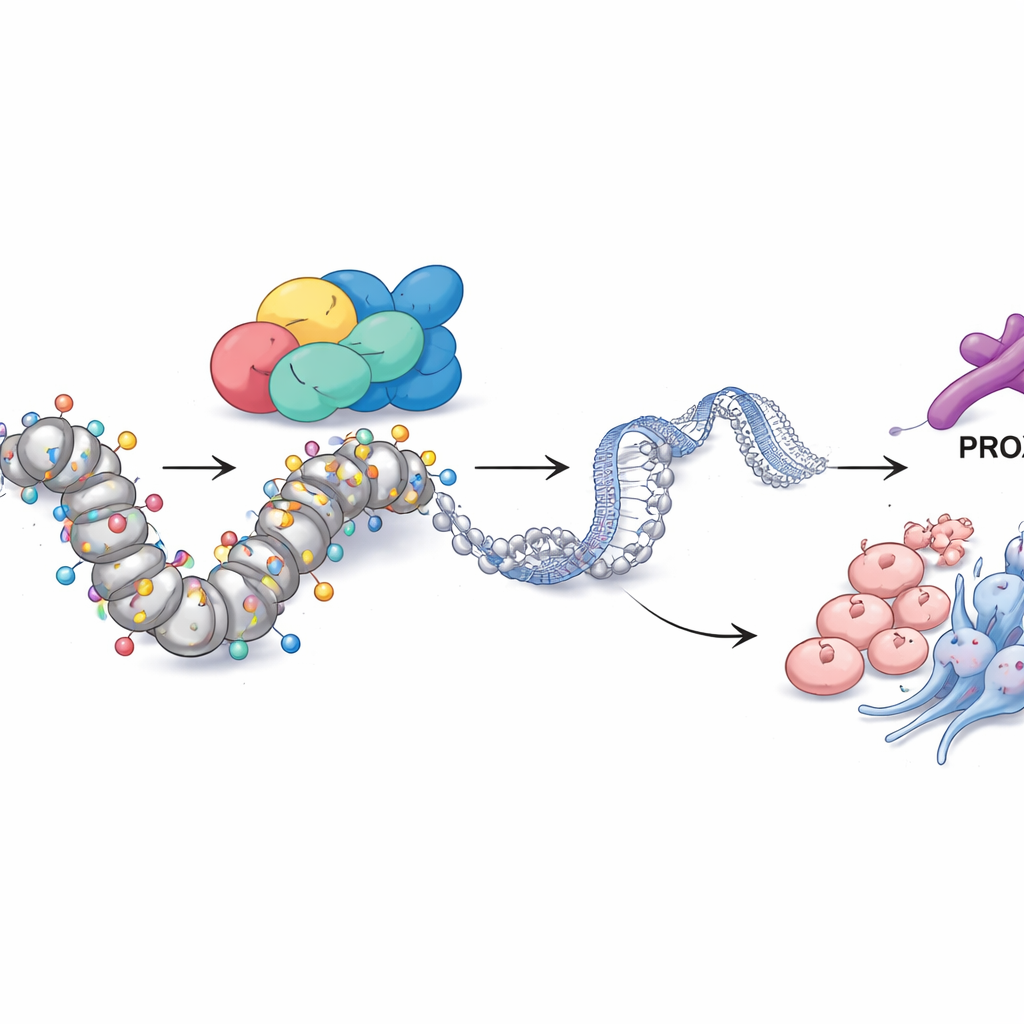
PROX1 e marcas químicas conectam SMARCA4 ao comportamento tumoral
Ao aprofundar, a equipe investigou como SMARCA4 exerce um controle tão amplo. Integrando várias camadas de dados genômicos, identificaram outra proteína, o fator de transcrição PROX1, como um parceiro chave. Nas células resistentes, a região de controle de PROX1 no genoma estava incomumente aberta e decorada com uma marca química de DNA ativo, um tipo de acetilação de histona conhecida como H3K27ac. SMARCA4 situava-se diretamente nesse sítio e, quando SMARCA4 foi reduzido, tanto os níveis de PROX1 quanto a H3K27ac naquela região caíram. Diminuir apenas PROX1 foi suficiente para cortar crescimento celular, invasão, marcadores neuroendócrinos e propriedades semelhantes a células-tronco, mostrando que PROX1 age como um executor importante do programa de SMARCA4. Notavelmente, bloquear enzimas que removem grupos acetil (com um inibidor de histona desacetilase) ou aumentar artificialmente PROX1 pôde em grande parte resgatar a perda de SMARCA4, reforçando que essa via opera através da acetilação no locus de PROX1.
O que isso significa para tratamentos futuros
Em termos simples, o estudo revela uma cadeia de eventos: sob pressão da enzalutamida, células do câncer de próstata ativam SMARCA4, que remodela a cromatina para aumentar a acetilação e ativação de PROX1, e essa dupla então ajuda as células a abandonar sua identidade original e adotar um estado resistente e semelhante ao neuroendócrino. Para pacientes, isso sugere que drogas direcionadas a SMARCA4, às enzimas que colocam ou removem marcas de acetil, ou ao próprio PROX1 poderiam ser combinadas com as terapias padrão de bloqueio hormonal para impedir que os tumores evoluam para essa forma de alto risco. Embora esses achados ainda precisem de confirmação em amostras humanas, eles delineiam uma via epigenética concreta que clínicos e desenvolvedores de fármacos podem agora mirar para combater uma das rotas de escape mais letais no câncer de próstata.
Citação: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Palavras-chave: câncer de próstata, resistência a medicamentos, epigenética, transformação neuroendócrina, remodelamento da cromatina