Clear Sky Science · tr
SMARCA4, H3K27 asetilasyonu yoluyla PROX1’i düzenleyerek prostat kanserinde hücresel hat değişkenliğini ve enzalutamide direncini artırır
Bu araştırma prostat kanseri hastaları için neden önemli
İleri evre prostat kanseri olan erkekler sıklıkla erkek hormonlarını baskılayan ilaçlarla tedavi edilir, ancak birçok tümör nihayetinde bu tedavilere karşı kaçınmayı başarır ve çok daha agresif bir biçimde geri döner. Bu çalışma hayati bir soruyu soruyor: prostat kanseri hücrelerinin enzalutamid tedavisinden sonra kimliklerini değiştirip hem öldürülmesi zor hem de daha ölümcül hale gelmelerine ne olanak tanıyor? Bu biçim değiştirmeyi yöneten temel bir moleküler anahtarı ortaya çıkararak, çalışma bu tehlikeli evrimi geciktirebilecek veya engelleyebilecek yeni stratejilere işaret ediyor.
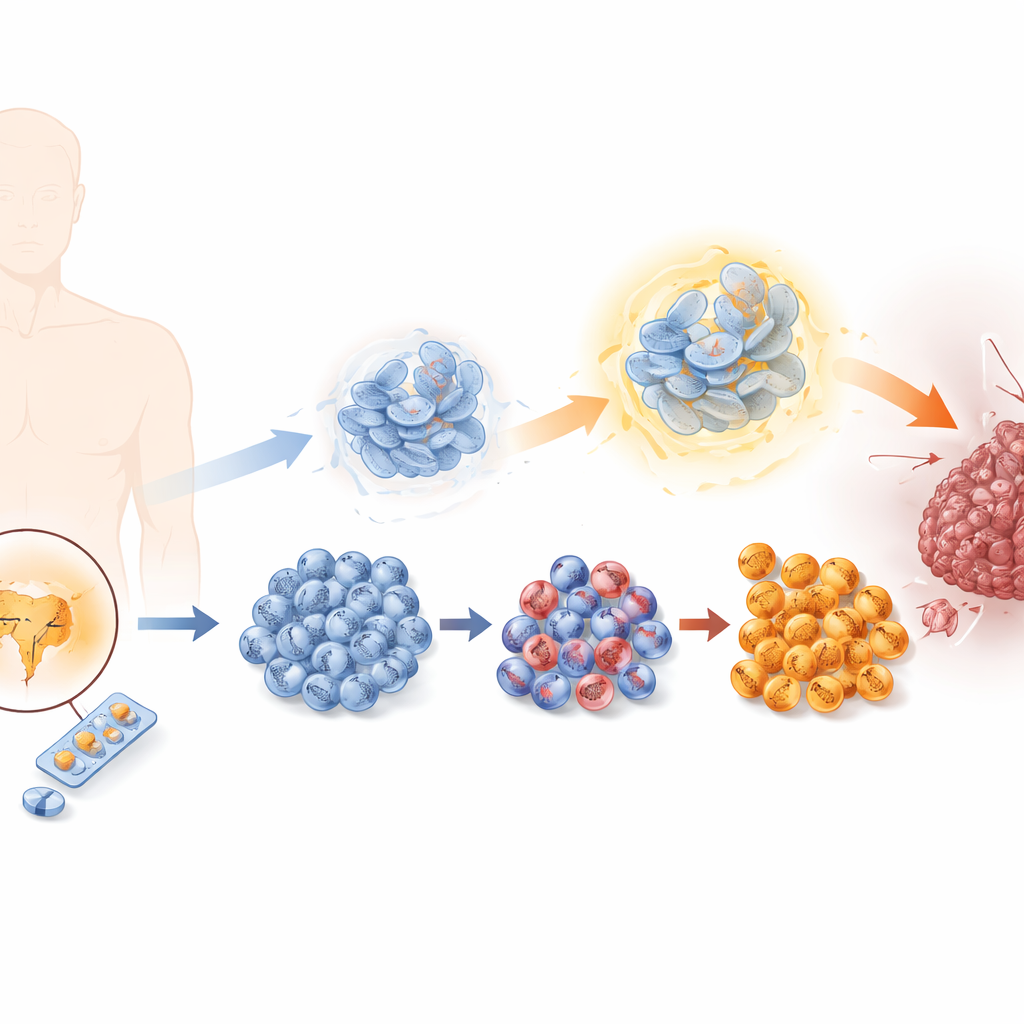
Tümörler hormon engelleyici tedaviden nasıl kaçmayı öğrenir
Prostat kanseri hücreleri genellikle androjen reseptörü aracılığıyla etkinleşen erkek hormonlarına bağımlıdır. Enzalutamid bu sinyali bloke ederek etki gösterir, ancak zamanla bazı hücreler bundan kurtulur. Araştırmacılar bu süreci laboratuvarda, prostat kanseri hücrelerini kademeli olarak artan dozlarda enzalutamide maruz bırakarak yeniden yarattılar ve hassastan yüksek dirençliye uzanan bir dizi hücre hattı ürettiler. Direnç arttıkça hücreler daha hızlı bölündü, daha kolay göç etti ve çevreleyen dokuyu daha fazla istila etti; bunların hepsi daha kötü huylu bir tümörün işaretleridir. Aynı zamanda tipik prostat hücrelerine ait özelliklerini kaybettiler ve nadir ama çok agresif olan, sınırlı tedavi seçeneği bulunan nöroendokrin hücre özelliklerini kazandılar.
Hücre kimliği değişiklikleri DNA’nın paketlenmesine yazılıyor
Bu tehlikeli özelliklerin nasıl ortaya çıktığını anlamak için ekip, DNA dizisinin ötesine, hücre çekirdeği içindeki DNA’nın nasıl paketlendiğine baktı. Hangi DNA bölgesinin açık hangisinin sıkıca sarılı olduğunu haritalayan tüm genom çapında yöntemler kullanarak, direncin kromatindeki kapsamlı değişikliklerle el ele geliştiğini buldular. Androjen bağımlı genleri kontrol eden bölgeler daha az erişilebilir hale gelirken, kök hücre benzeri ve nöroendokrin programlarla ilişkili diziler açıldı. Bu kaymalar gen aktivitesindeki değişikliklerle yakından örtüştü ve yalnızca rastgele mutasyonlar yerine hücrelerin düzenleyici devrelerinin koordine bir şekilde yeniden kablolanmasını ortaya koydu.
SMARCA4 adlı bir kromatin motoru tümörleri daha ölümcül bir duruma itiyor
Değişen birçok düzenleyici arasında öne çıkan bir tanesi vardı: kromatini kaydırıp yeniden yapılandıran moleküler bir makinenin çekirdek bileşeni olan SMARCA4. SMARCA4 düzeyleri en dirençli, nöroendokrin benzeri hücrelerde ve agresif hasta tümörlerinde çok daha yüksekti ve yüksek seviyeler daha kötü sağkalımla ilişkiliydi. Bilim insanları dirençli hücrelerde SMARCA4’ü azalttıklarında büyüme yavaşladı, göç ve invazyon azaldı ve daha fazla hücre programlı hücre ölümü yaşadı. Önemli olarak, nöroendokrin kimlik belirteçleri zayıfladı ve hem kültürlerde hem de fare tümörlerinde tipik prostat hücre özellikleri yeniden ortaya çıktı. Bu bulgular SMARCA4’ü tümörlerin hem tedaviye direnmesine hem de daha tehlikeli bir kişilik benimsemesine yardımcı olan merkezi bir motor olarak konumlandırıyor.
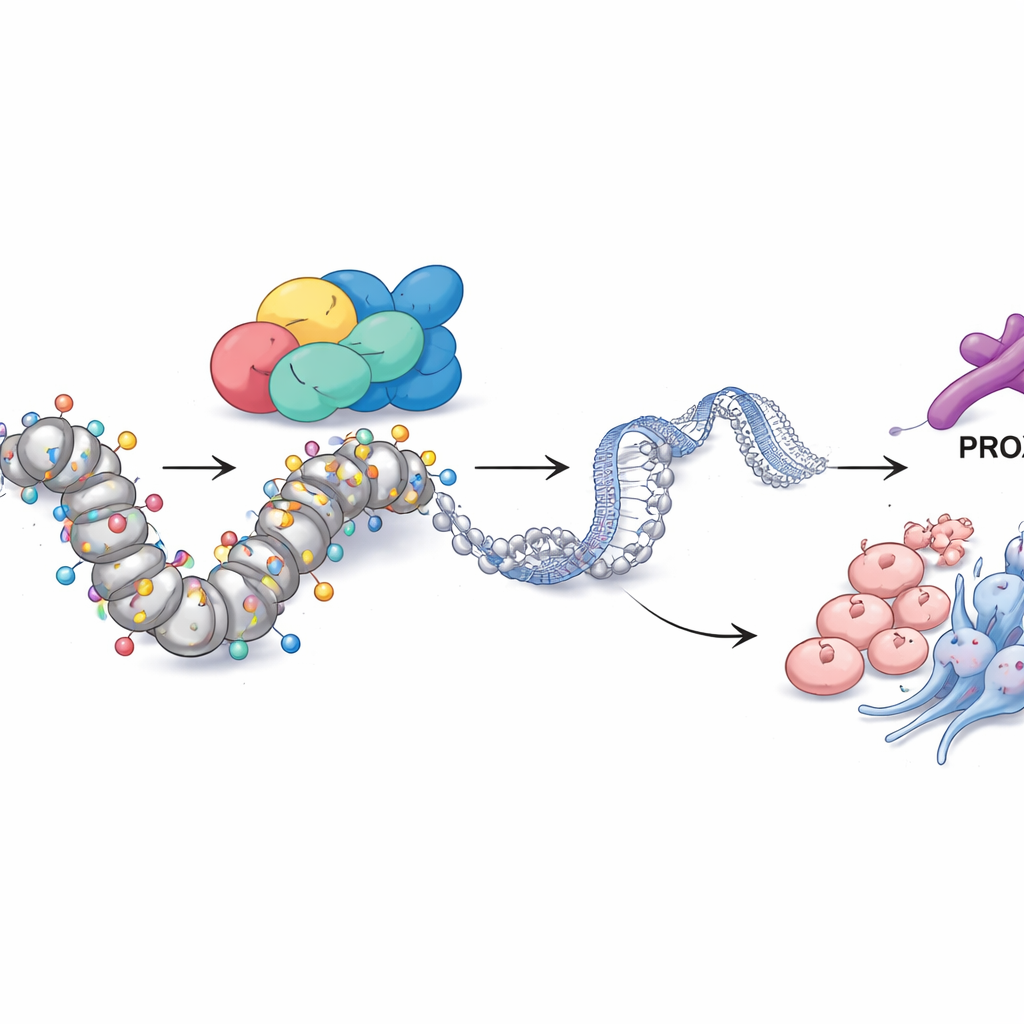
PROX1 ve kimyasal işaretler SMARCA4’ü tümör davranışıyla bağlıyor
Daha derine indiklerinde ekip, SMARCA4’ün bu kadar geniş kapsamlı kontrolü nasıl uyguladığını sordu. Birkaç genomik veri katmanını entegre ederek diğer bir protein olan transkripsiyon faktörü PROX1’i kilit bir ortak olarak tanımladılar. Dirençli hücrelerde PROX1’in genomdaki kontrol bölgesi alışılmadık şekilde açıktı ve aktif DNA’nın bir kimyasal işareti olan H3K27 asetilasyonu ile süslenmişti. SMARCA4 doğrudan bu bölgede yer alıyordu ve SMARCA4 azaltıldığında hem PROX1 düzeyleri hem de bu bölgedeki H3K27ac azaldı. Sadece PROX1’i baskılamak hücre büyümesini, invazyonu, nöroendokrin belirteçleri ve kök hücre benzeri özellikleri azaltmaya yetti; bu da PROX1’in SMARCA4 programının önemli bir yürütücüsü olduğunu gösteriyor. Dikkate değer şekilde, asetil gruplarını kaldıran enzimleri engelleyen bir histon deasetilaz inhibitörüyle bloke etmek veya yapay olarak PROX1’i artırmak SMARCA4 kaybını büyük ölçüde telafi edebiliyordu; bu da bu yolun PROX1 lokusundaki asetilasyon üzerinden işlediğini vurguluyor.
Gelecekteki tedaviler için bunun anlamı
Özetle çalışma şu olay zincirini ortaya koyuyor: enzalutamid baskısı altında prostat kanseri hücreleri SMARCA4’ü açıyor, bu da kromatini yeniden şekillendirip PROX1’in asetilasyonunu ve aktivasyonunu artırıyor ve bu ikili hücrelerin orijinal kimliklerini kaybedip dirençli, nöroendokrin benzeri bir durumu benimsemelerine yardımcı oluyor. Hastalar için bu, SMARCA4’ü, asetil işaretlerini yerleştiren veya çıkaran enzimleri ya da PROX1’in kendisini hedef alan ilaçların standart hormon-engelleyici tedavilerle birlikte kullanılarak tümörlerin bu yüksek riskli forma evrilmesini engelleme potansiyeli olduğunu öne sürüyor. Bu bulguların insan örneklerinde doğrulanması gerekiyor olsa da, klinisyenlerin ve ilaç geliştiricilerin şimdi prostat kanserindeki en ölümcül kaçış yollarından birine karşı hedefleyebileceği somut bir epigenetik yol haritası çiziyor.
Atıf: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Anahtar kelimeler: prostat kanseri, ilaç direnci, epigenetik, nöroendokrin dönüşüm, kromatin yeniden şekillendirme