Clear Sky Science · sv
SMARCA4 främjar linjeplasticitet och enzalutamid‑resistens vid prostatacancer genom att reglera PROX1 via H3K27‑acetylering
Varför denna forskning betyder något för patienter med prostatacancer
Män med avancerad prostatacancer behandlas ofta med läkemedel som släcker ner manliga hormoner, men många tumörer lyckas så småningom överlista dessa terapier och återkomma i en mycket mer aggressiv form. Denna studie ställer en avgörande fråga: vad gör det möjligt för prostatacancerceller att ändra sin identitet och bli både svårare att döda och mer dödliga efter behandling med läkemedlet enzalutamid? Genom att avslöja en nyckel‑molekylär strömbrytare som driver denna formförändring pekar arbetet mot strategier som skulle kunna fördröja eller förhindra denna farliga utveckling.
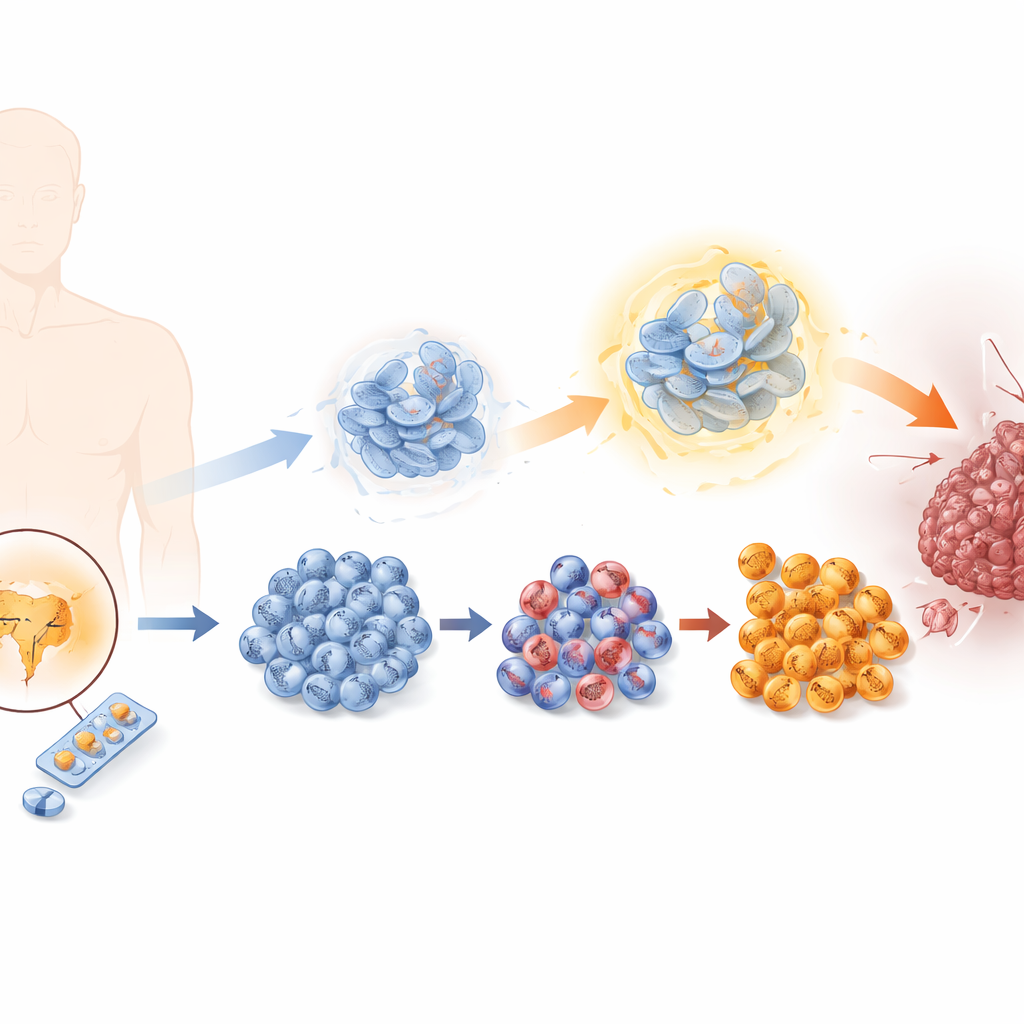
Hur tumörer lär sig undvika hormon‑blockerande behandling
Prostatacancerceller är vanligtvis beroende av manliga hormoner som verkar via androgenreceptorn. Enzalutamid fungerar genom att blockera denna signal, men med tiden lyckas vissa celler undkomma. Forskarna återskapade denna process i laboratoriet genom att utsätta prostatacancerceller för gradvis ökande doser av enzalutamid och genererade en serie cellinjer som sträckte sig från känsliga till starkt resistenta. När resistensen ökade delade cellerna sig snabbare, migrerade lättare och invaderade omgivande vävnad mer intensivt — alla tecken på en mer malign tumör. Samtidigt förlorade de egenskaper hos typiska prostataceller och erhöll drag av så kallade neuroendokrina celler, en sällsynt men mycket aggressiv tumörtyp med få behandlingsalternativ.
Förändringar i cellidentitet skrivs in i DNA:s förpackning
För att förstå hur dessa farliga egenskaper uppstår tittade teamet bortom DNA‑koden i sig till hur DNA packas och packas upp inne i cellkärnan. Genom att använda genomomfattande metoder som kartlägger vilka DNA‑regioner som är öppna respektive tätt lindade fann de att resistens utvecklades i nära samklang med omfattande förändringar i kromatin, det protein–DNA‑material som organiserar genomet. Regioner som styr androgenberoende gener blev mindre tillgängliga, medan sträckor kopplade till stamliknande och neuroendokrina program öppnade upp. Dessa skiften följde nära förändringar i genaktivitet och avslöjade en samordnad omläggning av cellernas regulatoriska kretsar snarare än enbart slumpmässiga mutationer.
En kromatinmotor kallad SMARCA4 driver tumörer mot ett farligare tillstånd
Bland många förändrade regulatorer stack en ut: SMARCA4, en kärnkomponent i en molekylär maskin som skjuter och omstrukturerar kromatin. SMARCA4‑nivåer var mycket högre i de mest resistenta, neuroendokrina‑liknande cellerna och i aggressiva patienttumörer, och höga nivåer kopplades till sämre överlevnad. När forskarna minskade SMARCA4 i resistenta celler bromsade tillväxten, migration och invasion minskade, och fler celler genomgick programmerad celldöd. Viktigt var att markörer för neuroendokrin identitet tonade bort och drag av typiska prostataceller återkom, både i odlingsskålar och i musstumörer. Dessa fynd placerar SMARCA4 som en central motor som hjälper tumörer både att motstå behandling och anta en farligare persona.
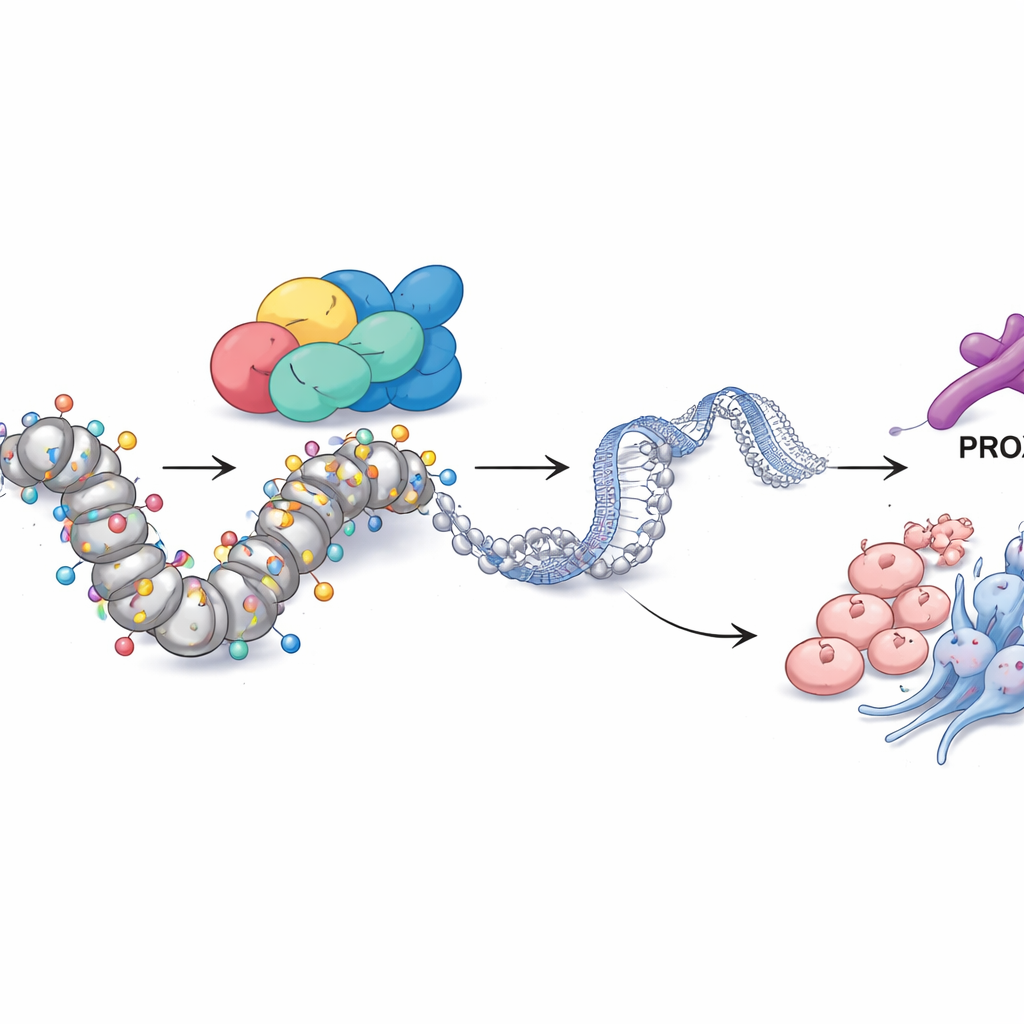
PROX1 och kemiska märkningar kopplar SMARCA4 till tumörbeteende
Genom att gå djupare frågade teamet hur SMARCA4 utövar ett så omfattande inflytande. Genom att integrera flera lager av genomisk data identifierade de ett annat protein, transkriptionsfaktorn PROX1, som en viktig partner. I resistenta celler var PROX1:s kontrollregion i genomet ovanligt öppen och dekorerad med en kemisk markör för aktivt DNA, en typ av histonacetylering känd som H3K27ac. SMARCA4 satt direkt vid denna plats, och när SMARCA4 minskades föll både PROX1‑nivåerna och H3K27ac vid denna region. Att sänka PROX1 ensamt var tillräckligt för att minska celltillväxt, invasion, neuroendokrina markörer och stamliknande egenskaper, vilket visar att PROX1 fungerar som en viktig utförare av SMARCA4:s program. Anmärkningsvärt nog kunde blockering av enzymer som tar bort acetylgrupper (med en histondeacetylashämmare) eller konstgjord uppreglering av PROX1 i hög grad återställa förlusten av SMARCA4, vilket understryker att denna väg går via acetylering vid PROX1‑lokus.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar studien en händelsekedja: under trycket från enzalutamid slår prostatacancerceller på SMARCA4, som omformar kromatin för att öka acetylering och aktivering av PROX1, och detta par hjälper cellerna att kasta av sig sin ursprungliga identitet och anta ett resistent, neuroendokrint‑liknande tillstånd. För patienter tyder detta på att läkemedel riktade mot SMARCA4, enzymerna som sätter eller tar bort acetylmärken, eller PROX1 självt skulle kunna kombineras med standard hormon‑blockerande behandlingar för att hindra tumörer från att utvecklas till denna högriskform. Även om dessa fynd fortfarande behöver bekräftas i mänskliga prover skisserar de en tydlig epigenetisk bana som kliniker och läkemedelsutvecklare nu kan rikta in sig på för att bekämpa en av de mest dödliga flyktvägarna vid prostatacancer.
Citering: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Nyckelord: prostatacancer, läkemedelsresistens, epigenetik, neuroendokrin omvandling, kromatinombyggnad