Clear Sky Science · ar
SMARCA4 يعزز المرونة النسيجية ومقاومة الإنزالاتاميد في سرطان البروستاتا عن طريق تنظيم PROX1 عبر أسيتلة H3K27
لماذا هذا البحث مهم لمرضى سرطان البروستاتا
يعالج الرجال المصابون بسرطان البروستاتا المتقدم غالبًا بأدوية توقف عمل الهرمونات الذكرية، لكن العديد من الأورام يتغلب في نهاية المطاف على هذه العلاجات ويعود بدرجة عدوانية أكبر بكثير. يطرح هذا البحث سؤالاً حاسماً: ما الذي يسمح لخلايا سرطان البروستاتا بتغيير هويتها لتصبح أصعب في القتل وأكثر فتكًا بعد العلاج بالإنزالاتاميد؟ من خلال الكشف عن مفتاح جزيئي يدفع هذا التحول، يشير العمل إلى استراتيجيات جديدة قد تؤخر أو تمنع هذا التطور الخطير.
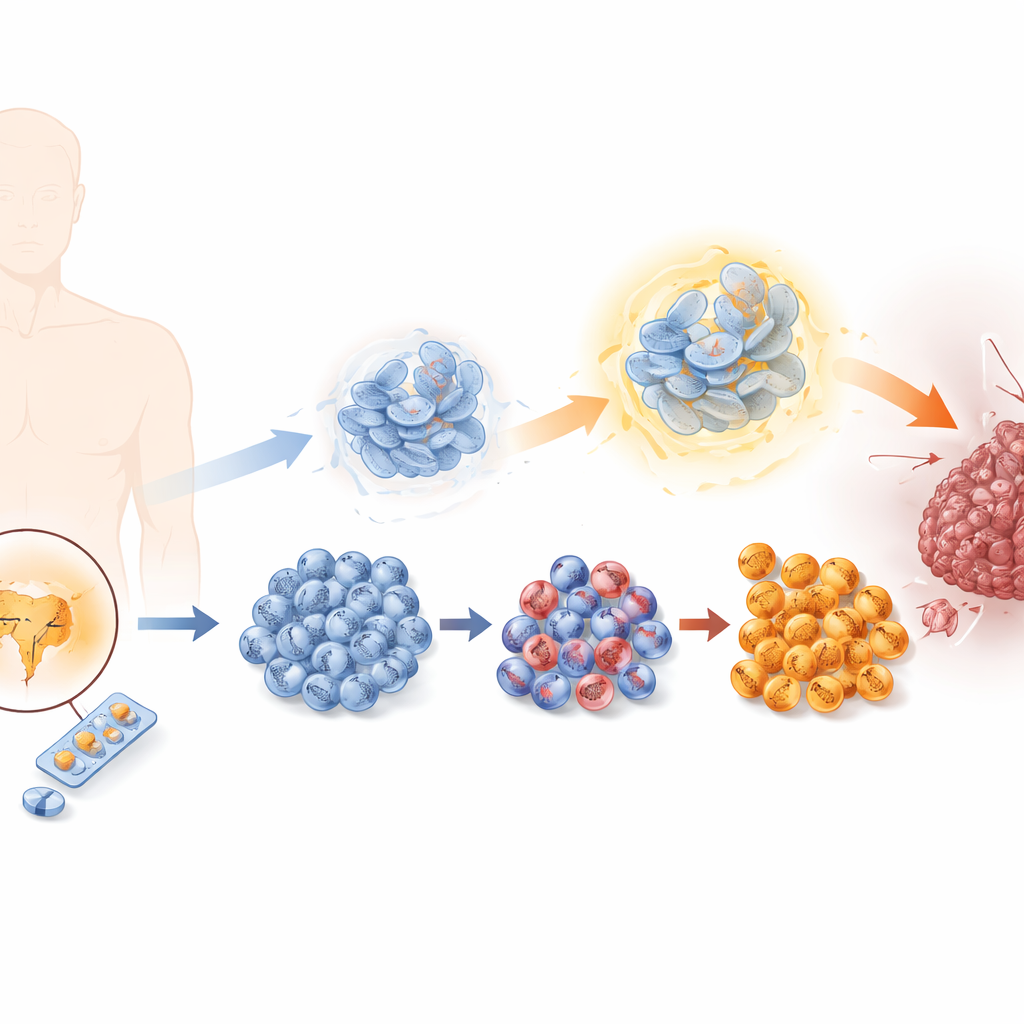
كيف تتعلم الأورام التملص من علاج حجب الهرمونات
تعتمد خلايا سرطان البروستاتا عادةً على الهرمونات الذكرية التي تعمل عبر مستقبل الأندروجين. يعمل الإنزالاتاميد عن طريق حجب هذا الإشارة، لكن مع مرور الوقت تفلت بعض الخلايا. أعاد الباحثون تكوين هذه العملية في المختبر بتعريض خلايا سرطان البروستاتا لجرعات متزايدة تدريجياً من الإنزالاتاميد، مكوّنين سلسلة من خطوط الخلايا تتراوح من حساسة إلى شديدة المقاومة. مع تزايد المقاومة، انقسمت الخلايا أسرع، وتحركت أكثر، وغزت الأنسجة المحيطة بسهولة أكبر، وهي كلها سمات لورم أكثر خباثة. في الوقت نفسه، فقدت سمات خلايا البروستاتا النمطية واكتسبت خصائص خلايا عصبية صماوية، نوع نادر لكنه عدواني للغاية من الأورام ولديه خيارات علاجية محدودة.
تتجسد تغييرات هوية الخلية في تعبئة الحمض النووي
لفهم كيف تظهر هذه الصفات الخطرة، نظر الفريق إلى ما وراء رمز الحمض النووي نفسه إلى طريقة حزم وفك حزم الحمض النووي داخل نواة الخلية. باستخدام أساليب على مستوى الجينوم ترسم أي المناطق مفتوحة وأيها مطوية بإحكام، وجدوا أن المقاومة تطورت جنبًا إلى جنب مع تغييرات واسعة في الكروماتين، المادة البروتينية-الحمض نووية التي تنظم الجينوم. أصبحت المناطق التي تتحكم في الجينات المعتمدة على الأندروجين أقل وصولاً، بينما افتتحت مساحات مرتبطة ببرامج شبيهة بالخلايا الجذعية والعصبية الصماوية. تعقبت هذه التبدلات عن كثب تغييرات في نشاط الجينات، ما كشف عن إعادة توصيل منسقة لدائرة تنظيم الخلايا بدل الاعتماد على طفرات عشوائية فقط.
محرك كروماتين يُسمى SMARCA4 يدفع الأورام نحو حالة أكثر خطرًا
من بين العديد من المنظمين المتغيرين، برز واحد: SMARCA4، مكوّن أساسي لآلة جزيئية تزيح أعمدة الكروماتين وتعيد بنائها. كانت مستويات SMARCA4 أعلى بكثير في الخلايا الأكثر مقاومة والتي تشبه العصبية الصماوية وفي الأورام العدوانية لدى المرضى، وكان المستوى المرتفع مرتبطًا ببقاء أسوأ. عندما خفّض العلماء SMARCA4 في الخلايا المقاومة، تباطأ النمو، وانخفضت الهجرة والغزو، وخضعت المزيد من الخلايا للموت المبرمج. والأهم من ذلك، تلاشت علامات الهوية العصبية الصماوية وظهرت سمات خلايا البروستاتا النمطية من جديد، سواء في الأطباق أو في أورام الفئران. تضع هذه النتائج SMARCA4 كمحرك مركزي يساعد الأورام على المقاومة وتبني شخصية أكثر خطورة.
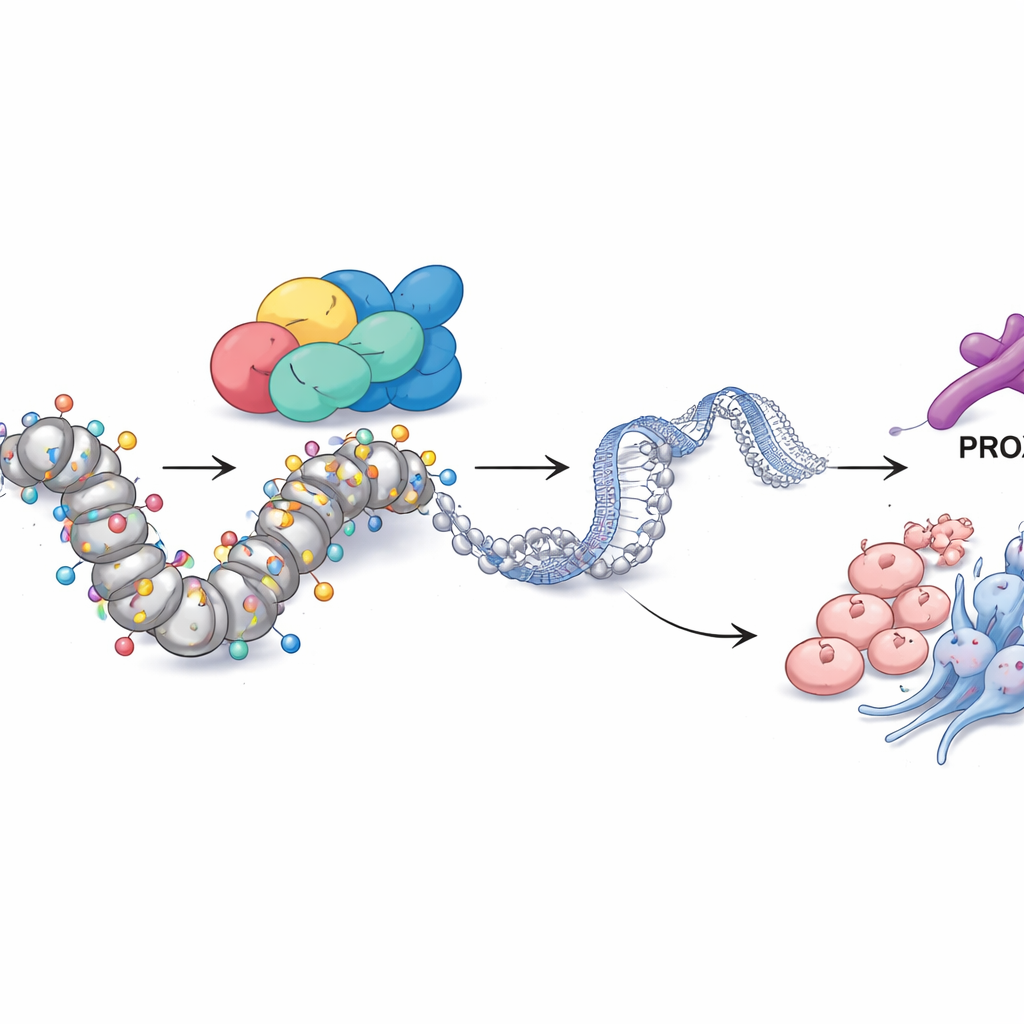
PROX1 والوسوم الكيميائية تربط SMARCA4 بسلوك الورم
بتعمق أكبر، سأل الفريق كيف يمارس SMARCA4 هذا التحكم واسع النطاق. من خلال دمج عدة طبقات من بيانات الجينوم، حددوا بروتينًا آخر، عامل النسخ PROX1، كشريك رئيسي. في الخلايا المقاومة، كانت منطقة التحكم الخاصة بـPROX1 في الجينوم مفتوحة بشكل غير عادي ومزدانة بوسم كيميائي للدنا النشط، نوع من أسيتلة الهيستون المعروفة باسم H3K27ac. وجد SMARCA4 مباشرة عند هذا الموقع، وعندما خُفض SMARCA4، انخفض كل من مستويات PROX1 وأسيتلة H3K27 في هذه المنطقة. كان خفض PROX1 وحده كافياً لتقليل نمو الخلايا والغزو وعلامات العصبية الصماوية والخصائص الشبيهة بالخلايا الجذعية، مما يبيّن أن PROX1 يعمل كمنفذ مهم لبرنامج SMARCA4. بشكل ملحوظ، أدى حجب الإنزيمات التي تزيل مجموعات الأسيتيل (بمثبط ناقض لهيستون دي أسيتلاز) أو رفع PROX1 اصطناعياً إلى إنقاذ كبير لفقدان SMARCA4، موضحًا أن هذا المسار يعمل عبر الأسيتلة عند موضع PROX1.
ماذا يعني هذا للعلاجات المستقبلية
ببساطة، يكشف البحث سلسلة أحداث: تحت ضغط الإنزالاتاميد، تشغّل خلايا سرطان البروستاتا SMARCA4، الذي يعيد تشكيل الكروماتين لزيادة الأسيتلة وتنشيط PROX1، ثم يساعد هذا الثنائي الخلايا على التخلي عن هويتها الأصلية وتبني حالة مقاومة تشبه العصبية الصماوية. للمرضى، يقترح ذلك أن الأدوية التي تستهدف SMARCA4 أو الإنزيمات التي تضع أو تزيل وسوم الأسيتيل أو PROX1 نفسه يمكن دمجها مع علاجات حجب الهرمونات القياسية لمنع الأورام من التطور إلى هذا الشكل عالي الخطورة. بينما لا تزال هذه النتائج بحاجة إلى تأكيد في عينات بشرية، فهي ترسم مسارًا فوق جينيًا ملموسًا يمكن للأطباء ومطوري الأدوية استهدافه الآن لمواجهة أحد أخطر طرق الهروب في سرطان البروستاتا.
الاستشهاد: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الأدوية, علم التخلق فوق الجيني, التحول العصبي الصماوي, إعادة تشكيل الكروماتين