Clear Sky Science · nl
SMARCA4 bevordert lineage‑plasticiteit en enzalutamide‑resistentie bij prostaatkanker door PROX1 te reguleren via H3K27‑acetylatie
Waarom dit onderzoek belangrijk is voor prostaatkankerpatiënten
Mannen met gevorderde prostaatkanker krijgen vaak medicijnen die mannelijke hormonen onderdrukken, maar veel tumoren weten deze therapieën uiteindelijk te omzeilen en keren terug in een veel agressievere vorm. Deze studie stelt een cruciale vraag: wat stelt prostaatkankercellen in staat hun identiteit te veranderen en na behandeling met het middel enzalutamide zowel moeilijker te doden als dodelijker te worden? Door een belangrijk moleculair schakelaar te onthullen die deze vormverandering aandrijft, wijst het werk op nieuwe strategieën die deze gevaarlijke evolutie kunnen vertragen of voorkomen.
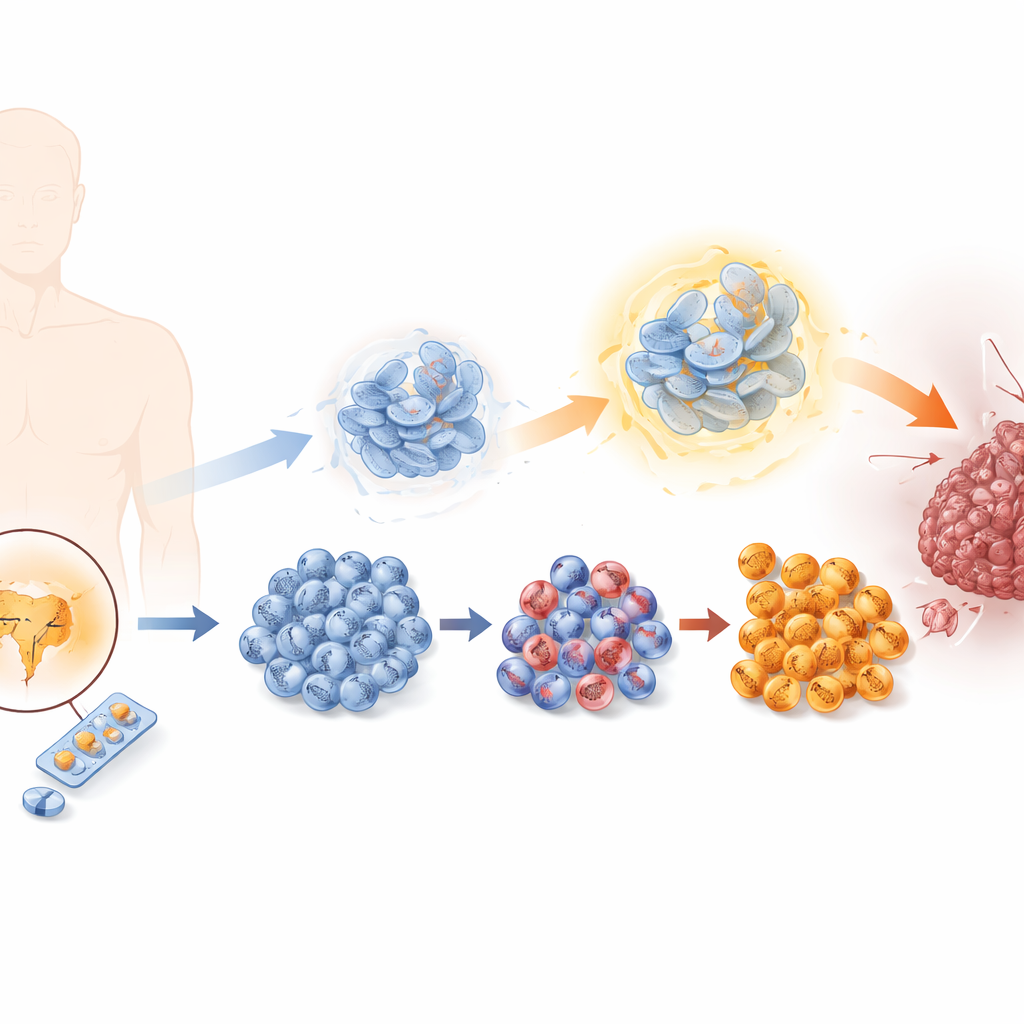
Hoe tumoren leren hormoonblokkerende therapie te ontwijken
Prostaatkankercellen zijn meestal afhankelijk van mannelijke hormonen die via de androgenenreceptor werken. Enzalutamide blokkeert dit signaal, maar na verloop van tijd weten sommige cellen te ontsnappen. De onderzoekers bootsten dit proces na in het laboratorium door prostaatkankercellen bloot te stellen aan geleidelijk toenemende doses enzalutamide, waarmee ze een reeks cellijnen genereerden van gevoelig tot sterk resistent. Naarmate de resistentie toenam, deelden de cellen sneller, migreerden ze gemakkelijker en vielen ze omliggend weefsel eerder binnen — allemaal kenmerken van een meer kwaadaardige tumor. Tegelijkertijd verloren ze eigenschappen van typische prostaatcellen en verwierf en ze kenmerken van zogenaamde neuro‑endocriene cellen, een zeldzaam maar zeer agressief tumortype met weinig behandelopties.
Veranderingen in celdifferentiatie zijn vastgelegd in de DNA‑verpakking
Om te begrijpen hoe deze gevaarlijke eigenschappen ontstaan, keek het team voorbij de DNA‑code zelf naar de manier waarop DNA in de celkern wordt verpakt en ontpakt. Met genoombrede methoden die in kaart brengen welke DNA‑gebieden open zijn en welke dichtgewonden, vonden ze dat resistentie hand in hand ging met ingrijpende veranderingen in chromatine, het eiwit‑DNA‑materiaal dat het genoom organiseert. Gebieden die androgen‑afhankelijke genen regelen werden minder toegankelijk, terwijl streken gekoppeld aan stamcel‑achtige en neuro‑endocriene programma’s opengingen. Deze verschuivingen kwamen nauw overeen met veranderingen in genactiviteit, wat wijst op een gecoördineerde herbedrading van de regulatorische circuiten van de cellen in plaats van alleen willekeurige mutaties.
Een chromatine‑motor genaamd SMARCA4 duwt tumoren naar een dodelijker staat
Te midden van vele veranderde regulatoren stak één factor bovenuit: SMARCA4, een kerncomponent van een moleculaire machine die chromatine schuift en herstructureert. SMARCA4‑niveaus waren veel hoger in de meest resistente, neuro‑endocriene‑achtige cellen en in agressieve patiëntentumoren, en hoge niveaus waren gekoppeld aan slechtere overleving. Toen de wetenschappers SMARCA4 in resistente cellen verlaagden, vertraagde de groei, namen migratie en invasie af en ondergingen meer cellen geprogrammeerde celdood. Belangrijk was dat markers van neuro‑endocriene identiteit vervaagden en kenmerken van typische prostaatcellen terugkeerden, zowel in kweek als in muistumoren. Deze bevindingen positioneren SMARCA4 als een centraal motorisch element dat tumoren helpt zowel therapie te weerstaan als een gevaarlijker identiteit aan te nemen.
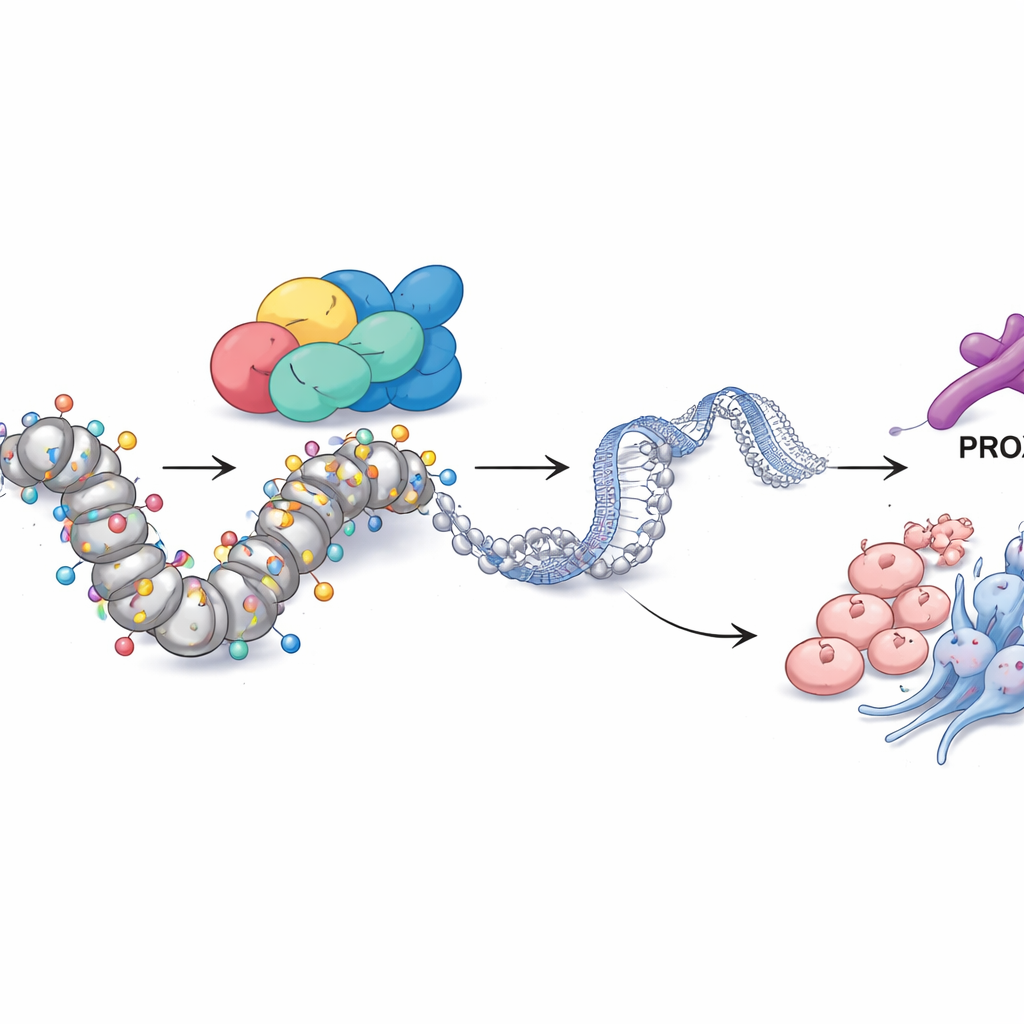
PROX1 en chemische labels verbinden SMARCA4 met tumorgedrag
Dieper graven, vroeg het team hoe SMARCA4 zo’n breed bereik aan controle uitoefent. Door verschillende lagen van genomische data te integreren identificeerden ze een ander eiwit, de transcriptiefactor PROX1, als een belangrijke partner. In resistente cellen was het controlegebied van PROX1 in het genoom ongewoon open en versierd met een chemische markering van actief DNA: een type histonacetylatie bekend als H3K27ac. SMARCA4 zat direct op deze plek, en wanneer SMARCA4 werd verlaagd, daalden zowel PROX1‑niveaus als H3K27ac op dit gebied. Het terugschakelen van PROX1 alleen was voldoende om celgroei, invasie, neuro‑endocriene markers en stamcel‑achtige eigenschappen te verminderen, wat toont dat PROX1 fungeert als een belangrijke uitvoerder van het SMARCA4‑programma. Opmerkelijk genoeg kon het blokkeren van enzymen die acetylgroepen verwijderen (met een histondeacetylaseremmer) of het kunstmatig verhogen van PROX1 grotendeels het verlies van SMARCA4 herstellen, wat benadrukt dat deze route via acetylatie op het PROX1‑locus verloopt.
Wat dit betekent voor toekomstige behandelingen
Kort gezegd onthult de studie een samenhangend proces: onder de druk van enzalutamide zetten prostaatkankercellen SMARCA4 aan, dat chromatine herschikt om acetylatie en activatie van PROX1 te versterken, en dit duo helpt de cellen hun oorspronkelijke identiteit af te leggen en een resistente, neuro‑endocriene‑achtige staat aan te nemen. Voor patiënten suggereert dit dat middelen gericht tegen SMARCA4, de enzymen die acetylgroepen plaatsen of verwijderen, of PROX1 zelf gecombineerd kunnen worden met standaard hormoonblokkerende therapieën om te voorkomen dat tumoren zich ontwikkelen tot deze hoogrisico‑vorm. Hoewel deze bevindingen nog bevestiging vereisen in menselijke monsters, schetsen ze een concreet epigenetisch pad dat clinici en medicijnontwikkelaars nu kunnen targeten om een van de dodelijkste ontsnappingsroutes bij prostaatkanker te bestrijden.
Bronvermelding: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Trefwoorden: prostaatkanker, medicatieresistentie, epigenetica, neuro‑endocriene transformatie, chromatine‑herstructurering