Clear Sky Science · de
SMARCA4 fördert Linienplastizität und Enzalutamid‑Resistenz beim Prostatakrebs durch Regulation von PROX1 über H3K27‑Acetylierung
Warum diese Forschung für Prostatakrebs‑Patienten wichtig ist
Männer mit fortgeschrittenem Prostatakrebs werden häufig mit Medikamenten behandelt, die männliche Hormone ausschalten; viele Tumoren umgehen diese Therapien jedoch schließlich und kehren in deutlich aggressiverer Form zurück. Diese Studie stellt eine zentrale Frage: Was ermöglicht es Prostatakrebszellen, ihre Identität zu verändern und nach Behandlung mit dem Medikament Enzalutamid schwerer zu töten und tödlicher zu werden? Durch das Aufdecken eines wichtigen molekularen Schalters, der dieses Formwechseln antreibt, weist die Arbeit auf neue Strategien hin, die diese gefährliche Entwicklung verzögern oder verhindern könnten.
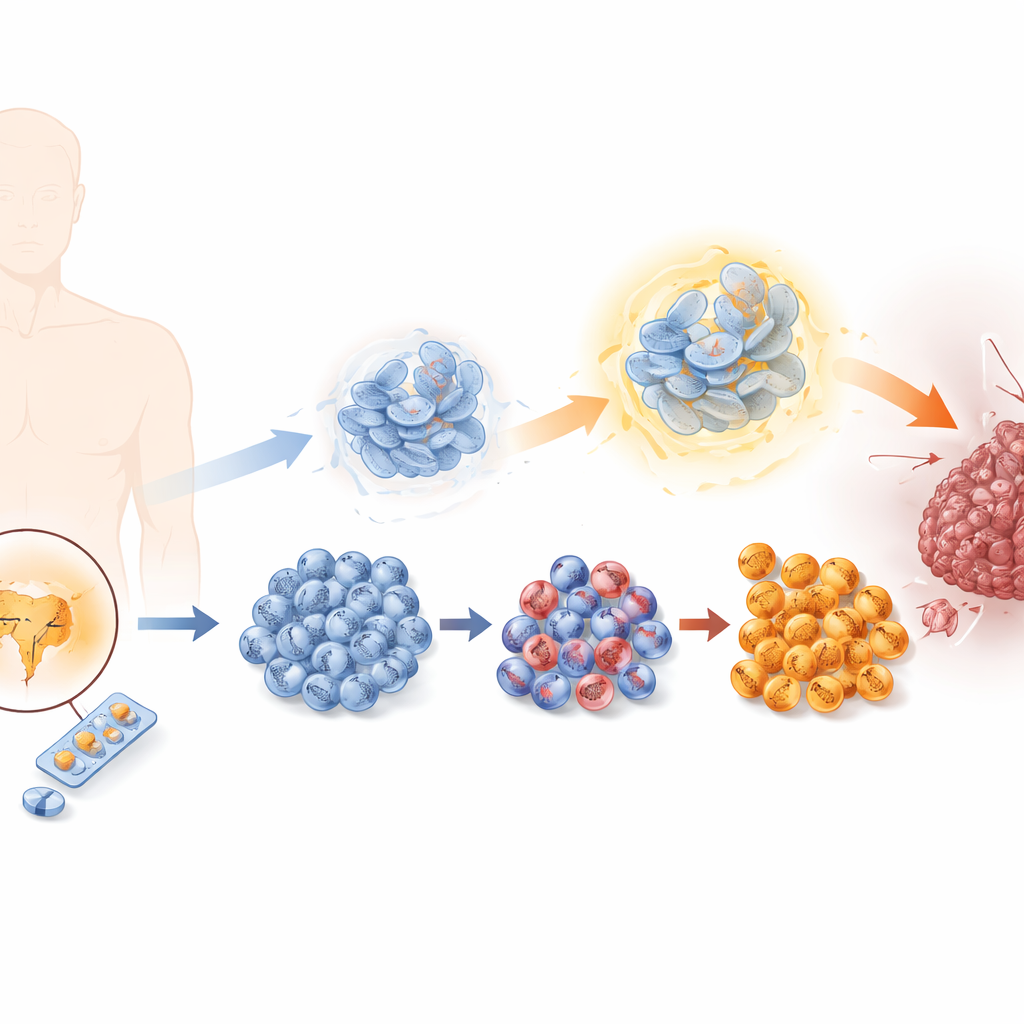
Wie Tumoren lernen, Hormonblockade zu umgehen
Prostatakrebszellen sind normalerweise auf männliche Hormone angewiesen, die über den Androgenrezeptor wirken. Enzalutamid blockiert dieses Signal, doch mit der Zeit entkommen einige Zellen. Die Forschenden rekonstruierten diesen Prozess im Labor, indem sie Prostatakrebszellen zunehmenden Dosen von Enzalutamid aussetzten und so eine Reihe von Zelllinien erzeugten, die von empfindlich bis hochresistent reichten. Mit zunehmender Resistenz teilten sich die Zellen schneller, wanderten leichter und drangen umgebendes Gewebe stärker ein – typische Merkmale eines bösartigeren Tumors. Gleichzeitig verloren sie Eigenschaften typischer Prostatazellen und gewannen Merkmale sogenannter neuroendokriner Zellen hinzu, einer seltenen, aber sehr aggressiven Tumorform mit wenigen Behandlungsoptionen.
Veränderungen der Zellidentität sind in der Verpackung der DNA verankert
Um zu verstehen, wie diese gefährlichen Merkmale entstehen, betrachtete das Team nicht nur den DNA‑Code selbst, sondern auch die Art und Weise, wie DNA im Zellkern verpackt und wieder geöffnet wird. Mithilfe genomweiter Methoden, die aufzeigen, welche DNA‑Regionen offen und welche stark gewunden sind, fanden sie heraus, dass sich die Resistenz parallel zu weitreichenden Veränderungen des Chromatins entwickelte – des Protein‑DNA‑Materials, das das Genom organisiert. Regionen, die androgensensible Gene steuern, wurden weniger zugänglich, während Bereiche, die mit Stammzell‑ähnlichen und neuroendokrinen Programmen verknüpft sind, aufschlossen. Diese Verschiebungen korrespondierten eng mit Änderungen in der Genaktivität und zeigten eine koordinierte Umverdrahtung der regulatorischen Schaltkreise der Zellen statt nur zufälliger Mutationen.
Eine Chromatin‑Maschine namens SMARCA4 treibt Tumoren in einen tödlicheren Zustand
Unter den vielen veränderten Regulatoren stach einer hervor: SMARCA4, ein Kernbestandteil einer molekularen Maschine, die Chromatin verschiebt und umstrukturiert. Die SMARCA4‑Spiegel waren in den am stärksten resistenten, neuroendokrin‑ähnlichen Zellen und in aggressiven Patiententumoren deutlich erhöht, und hohe Werte korrelierten mit schlechterem Überleben. Wenn die Forschenden SMARCA4 in resistenten Zellen reduzierten, verlangsamte sich das Wachstum, Migration und Invasion nahmen ab und mehr Zellen durchliefen programmierte Zellsterblichkeit. Wichtig war, dass Marker der neuroendokrinen Identität nachließen und Merkmale typischer Prostatazellen wieder auftraten, sowohl in Zellkulturen als auch in Maus‑Tumoren. Diese Befunde positionieren SMARCA4 als zentrale Maschine, die Tumoren hilft, sowohl Therapien zu widerstehen als auch ein gefährlicheres Erscheinungsbild anzunehmen.
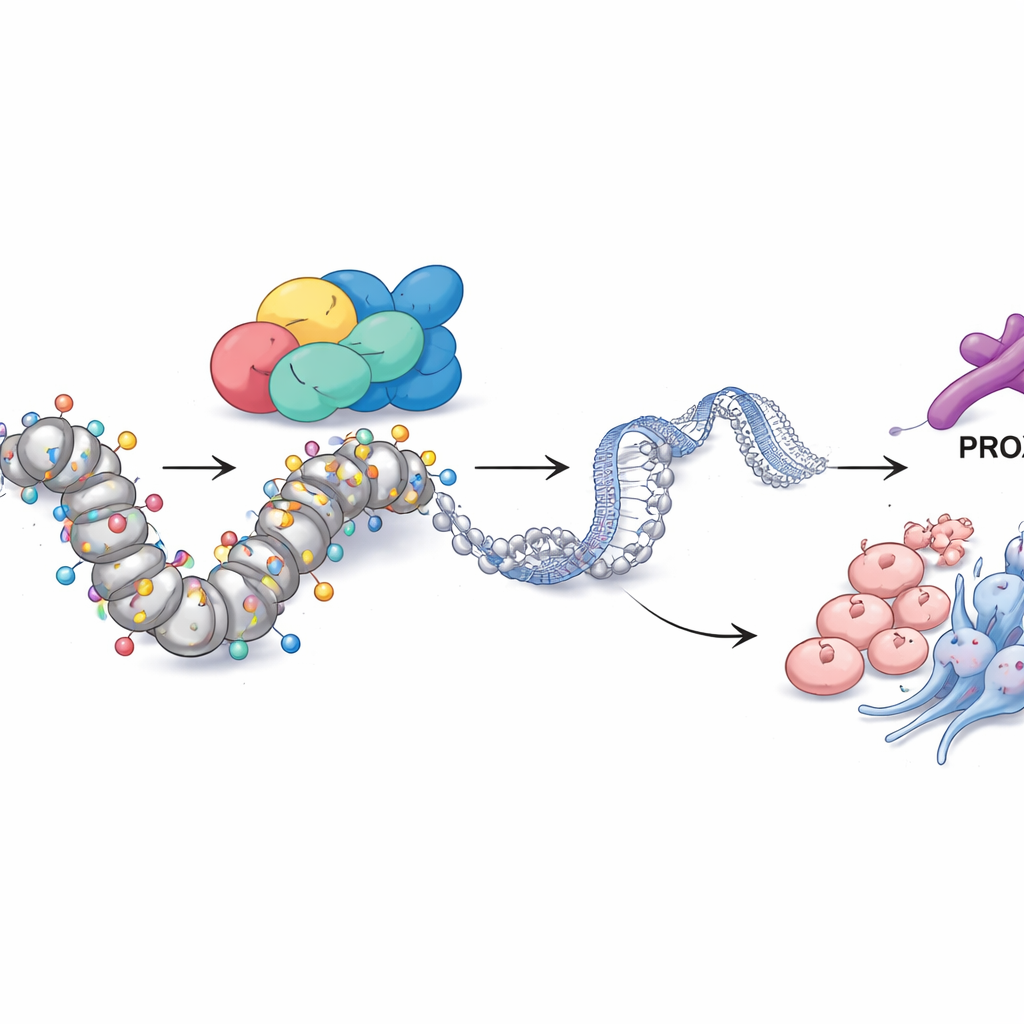
PROX1 und chemische Marker verbinden SMARCA4 mit dem Tumorverhalten
Tiefer gehend untersuchten die Forschenden, wie SMARCA4 eine so weitreichende Kontrolle ausübt. Durch die Integration mehrerer genomischer Datenebenen identifizierten sie ein weiteres Protein, den Transkriptionsfaktor PROX1, als wichtigen Partner. In resistenten Zellen war die Kontrollregion für PROX1 im Genom ungewöhnlich offen und mit einer chemischen Markierung aktiver DNA versehen – einer Form der Histon‑Acetylierung, bekannt als H3K27ac. SMARCA4 saß direkt an dieser Stelle, und bei Reduktion von SMARCA4 sanken sowohl PROX1‑Spiegel als auch H3K27ac an dieser Region. Allein die Herunterregulierung von PROX1 reichte aus, um Zellwachstum, Invasion, neuroendokrine Marker und stammesähnliche Eigenschaften zu verringern, was zeigt, dass PROX1 als wichtiger Ausführer des SMARCA4‑Programms fungiert. Bemerkenswerterweise konnte das Blockieren von Enzymen, die Acetylgruppen entfernen (mit einem Histon‑Deacetylase‑Inhibitor), oder das künstliche Anheben von PROX1 den Verlust von SMARCA4 weitgehend ausgleichen, was unterstreicht, dass dieser Weg über Acetylierung am PROX1‑Lokus läuft.
Was das für zukünftige Therapien bedeutet
Kurz gesagt legt die Studie eine Kette von Ereignissen offen: Unter dem Druck von Enzalutamid schalten Prostatakrebszellen SMARCA4 ein, das das Chromatin so umgestaltet, dass die Acetylierung und Aktivierung von PROX1 steigt; dieses Duo hilft den Zellen dann, ihre ursprüngliche Identität abzulegen und einen resistenten, neuroendokrin‑ähnlichen Zustand anzunehmen. Für Patientinnen und Patienten bedeutet das, dass Wirkstoffe, die auf SMARCA4, die Enzyme, die Acetylgruppen anbringen oder entfernen, oder auf PROX1 selbst abzielen, in Kombination mit standardmäßigen Hormonblockern eingesetzt werden könnten, um zu verhindern, dass Tumoren sich zu dieser hochriskanten Form entwickeln. Zwar müssen diese Befunde noch an menschlichen Proben bestätigt werden, doch skizzieren sie einen konkreten epigenetischen Weg, den Kliniker und Wirkstoffentwickler nun anvisieren können, um eine der tödlichsten Fluchtstrategien beim Prostatakrebs zu bekämpfen.
Zitation: Wu, C., Luo, M., Wu, C. et al. SMARCA4 promotes lineage plasticity and enzalutamide resistance in prostate cancer by regulating PROX1 via H3K27 acetylation. Cell Death Discov. 12, 175 (2026). https://doi.org/10.1038/s41420-026-03068-0
Schlüsselwörter: Prostatakrebs, Arzneimittelresistenz, Epigenetik, neuroendokrine Transformation, Chromatin‑Remodelling