Clear Sky Science · zh
由 ADAM12/IGF1 轴介导的糖酵解重编程促进后纵韧带骨化
当脊柱的一条支撑带变成骨头
在脊柱深处,有一条称为后纵韧带的坚韧组织带,帮助维持椎骨排列。有些人,尤以东亚人群为多,这条本应有弹性的韧带会逐渐钙化为骨,压迫脊髓,引起疼痛、无力甚至瘫痪。这种称为 OPLL 的疾病通常需要风险较高的手术,目前尚无药物治疗。这里总结的研究提出了一个简洁却有力的问题:这些细胞如何利用糖,是否是驱动这种异常骨化的隐秘引擎?
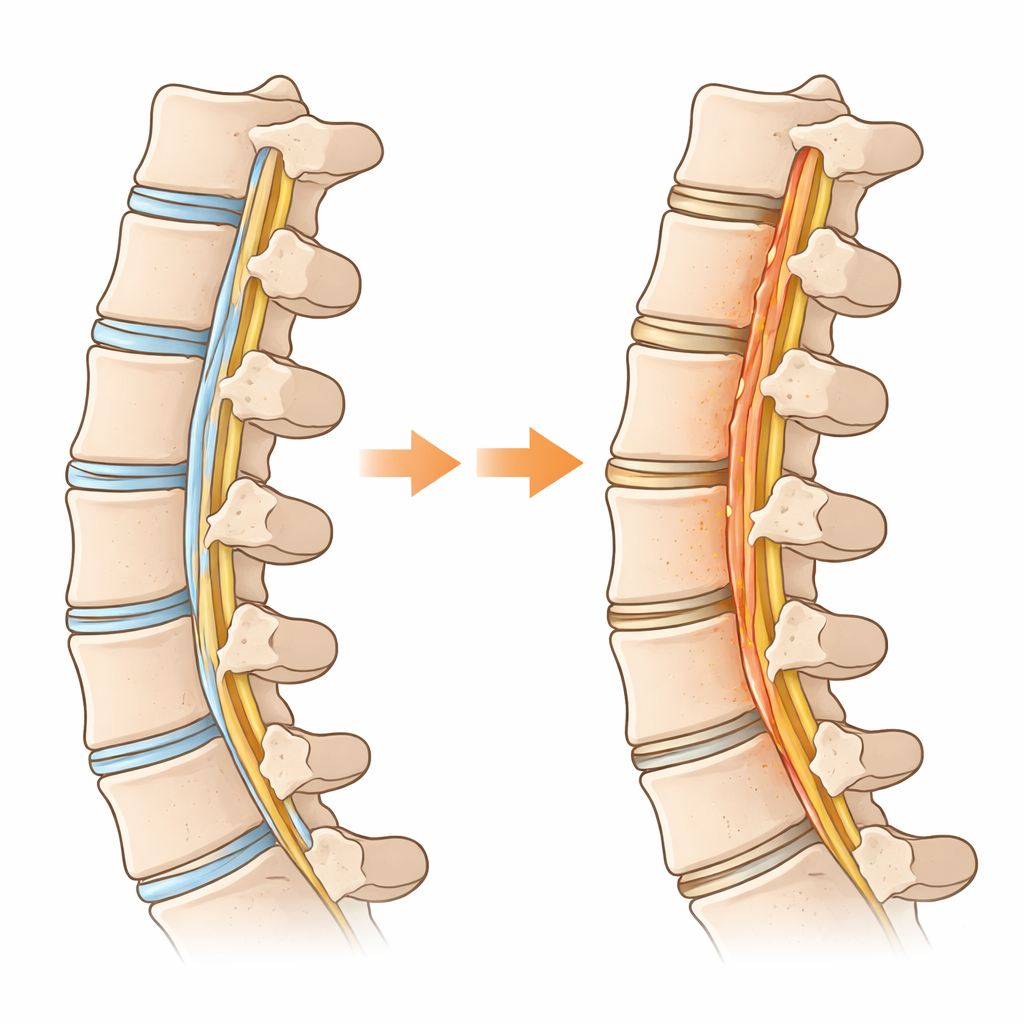
为何脊柱韧带开始像骨组织一样表现
研究者将 OPLL 患者的病变韧带组织与因其他颈部问题接受手术的正常韧带进行了比较。通过大规模基因组和单细胞分析,他们绘制出存在哪些细胞类型及每类细胞的活动状态。结果显示,一部分通常作为修复准备细胞的韧带前体细胞,正在走向成骨细胞的分化路线。在这一过程中,细胞改变了能量策略:不再主要依赖线粒体燃烧燃料,而是转向快速分解糖,这种代谢风格常见于癌症和增殖组织。这种向高强度糖代谢——即糖酵解——的转变,在那些实际在韧带内形成骨的细胞中尤为显著。
糖燃烧作为流氓骨生长的燃料
为检验这一代谢变化是随风旁观还是疾病的驱动因子,研究团队从患者处分离出韧带细胞,并在体外诱导其成骨。来自 OPLL 患者的细胞摄取更多葡萄糖,产生更多如乳酸等酸性代谢产物,并表现出较弱的线粒体活性。当科学家用名为 2-DG 的药物抑制糖酵解时,细胞向成骨分化的能力显著下降,沉积的矿物质也大幅减少。在小鼠体内,同样的药物缩小了人工诱导的骨样增生并减少了早期和成熟成骨细胞的数量,表明切断这一路径可以在活体动物中减缓或软化骨化过程。
一个隐秘开关:ADAM12–IGF1 连锁反应
进一步研究中,研究者寻找可能将细胞切换到高糖酵解状态的主控开关。一种名为 ADAM12 的分子引人注目:它在 OPLL 组织中显著上调,且在那些走向成骨的韧带细胞中活性最高。ADAM12 是一种在细胞外起作用的蛋白切割酶,此处似乎通过切割结合并固定生长信号 IGF1 的载体蛋白来释放 IGF1。通过修剪其中一种载体 IGFBP5,ADAM12 使更多的 IGF1 可用于激活韧带细胞表面的受体。继而,这激活了细胞内一条已知的生长通路(PI3K–AKT–mTOR),增强了细胞分解葡萄糖和产生乳酸的执行机制。当 ADAM12 在细胞中上调时,糖酵解和乳酸产生猛增;当其被沉默或切割活性被破坏时,两者均下降。
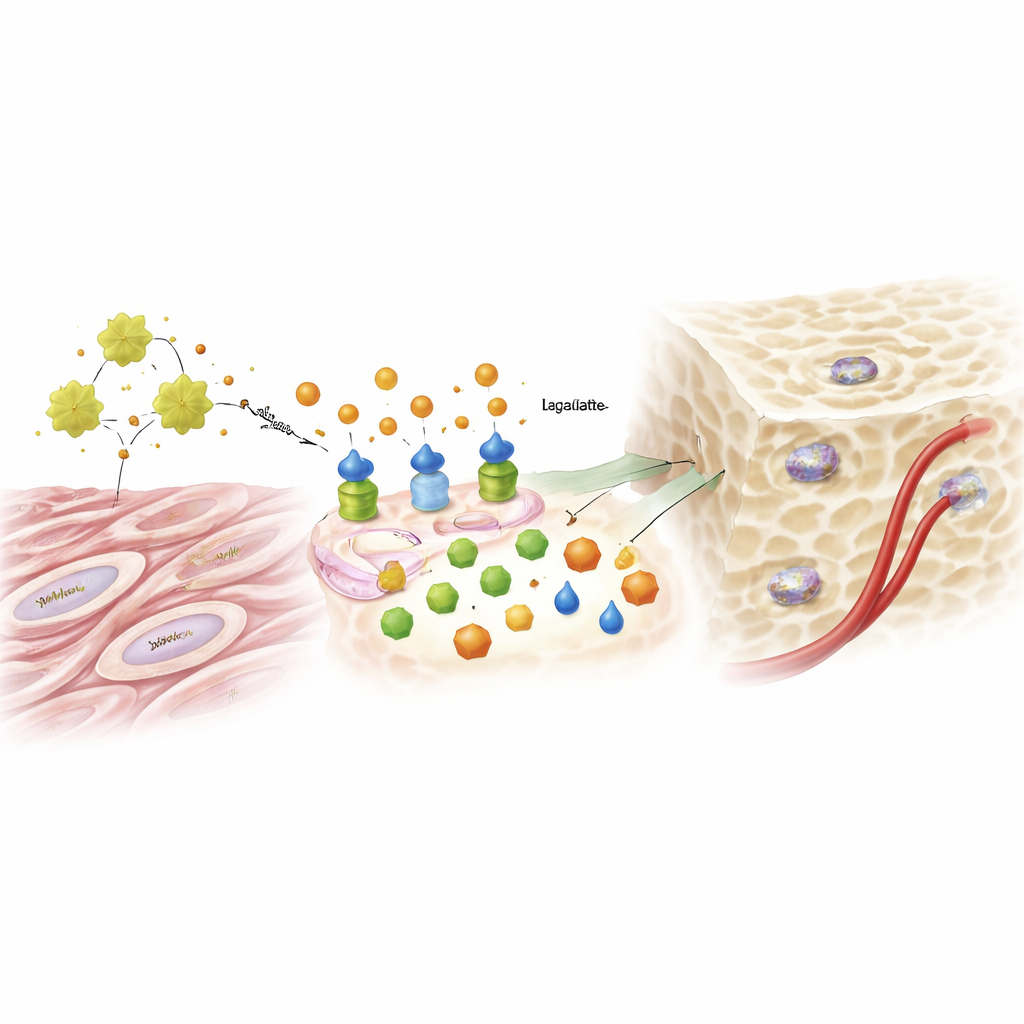
从糖的副产物到基因信号
长期被视为代谢废物的乳酸,扮演了出人意料的关键角色。在 ADAM12 和 IGF1 的影响下,糖酵解增强导致乳酸水平升高,进而影响细胞核内 DNA 的包装方式。研究者发现乳酸可以修饰特定的组蛋白——即组织 DNA 的蛋白质——形成一种称为乳酰化的化学标记。该标记松动了与成骨基因相关的 DNA 区域,帮助激活推动细胞成为成骨细胞的关键因子。向乳酸补充可在 ADAM12 被敲低的细胞中恢复成骨能力,而阻断糖酵解或生成乳酸的酶则消除了额外 ADAM12 带来的促进作用。同一条由 ADAM12 驱动的通路还增强了促进血管生长的信号,为新生骨组织提供营养供应。
通向非手术治疗的新路径
总体而言,这项研究描绘了一条清晰的事件链:脊柱韧带中 ADAM12 酶的上升释放出额外的 IGF1,激活了改写细胞糖代谢的生长程序。由此产生的糖代谢激增产生乳酸,乳酸再次改写与成骨相关的基因活性,并促进非应有部位的骨与血管形成。通过阻断 IGF1 信号或糖酵解,研究者能够在细胞培养和小鼠模型中抑制或逆转该过程。对患者而言,这项工作提示,针对 ADAM12–IGF1–糖酵解轴的药物策略有望在未来提供减缓或预防 OPLL 的非手术途径,从而减少高风险脊柱手术的需要,保护运动功能和神经功能。
引用: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
关键词: 脊柱韧带骨化, 细胞代谢, 糖酵解, 生长因子信号, 成骨