Clear Sky Science · es
La reprogramación glicolítica mediada por el eje ADAM12/IGF1 promueve la osificación del ligamento longitudinal posterior
Cuando una banda de soporte de la columna se convierte en hueso
En lo profundo de la columna, una banda resistente de tejido llamada ligamento longitudinal posterior ayuda a mantener alineadas nuestras vértebras. En algunas personas, sobre todo en Asia oriental, esta correa flexible se transforma gradualmente en hueso, comprimiendo la médula espinal y causando dolor, debilidad o incluso parálisis. Esta afección, conocida como OPLL, suele requerir cirugía arriesgada y actualmente no tiene tratamiento farmacológico. El estudio resumido aquí plantea una pregunta simple pero poderosa: ¿y si la forma en que estas células usan el azúcar es el motor oculto que impulsa este crecimiento óseo no deseado?
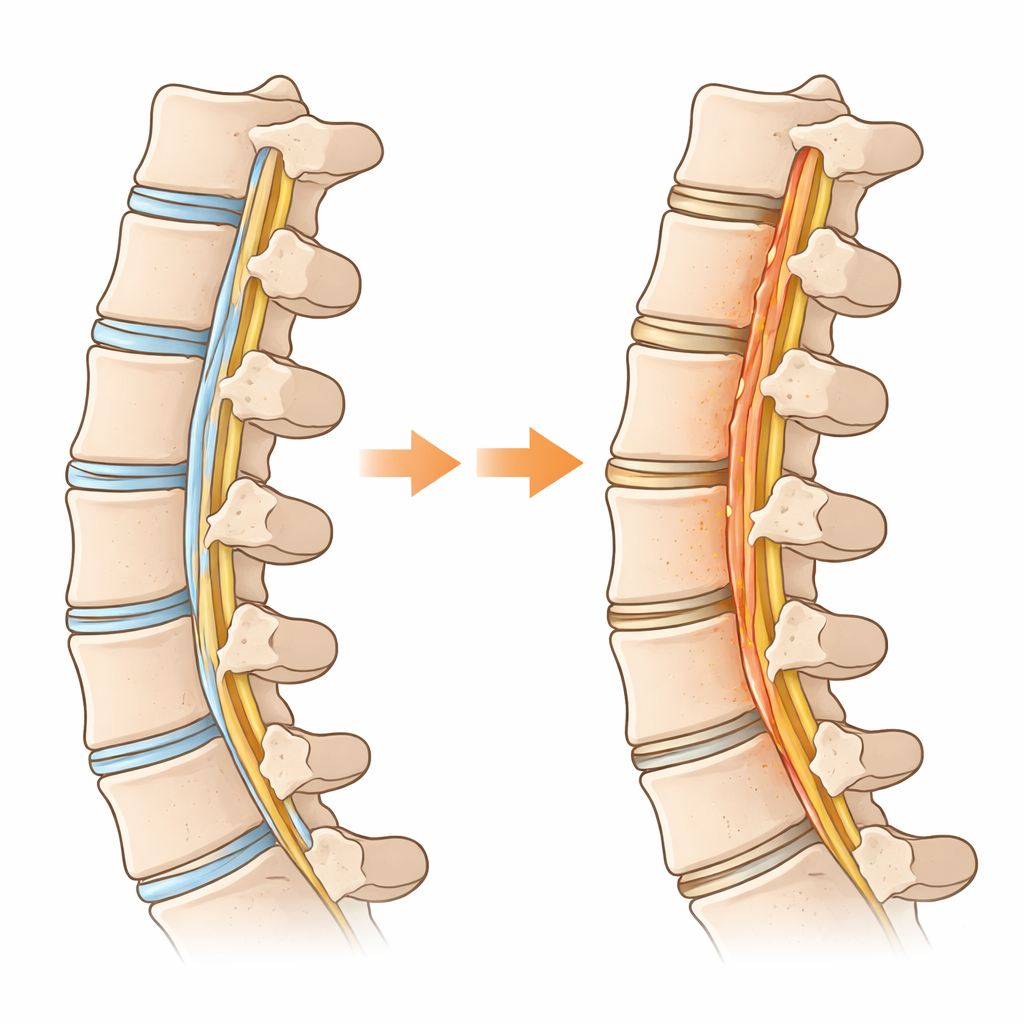
Por qué un ligamento espinal empieza a comportarse como hueso
Los investigadores compararon tejido ligamentoso enfermo de personas con OPLL con ligamento normal de pacientes con otros problemas cervicales. Mediante análisis genómicos a gran escala y de una sola célula, cartografiaron qué tipos celulares estaban presentes y qué hacía cada célula. Hallaron que un subconjunto de células del ligamento, que normalmente actúan como “progenitores” preparados para reparar, seguía un trayecto hacia convertirse en células formadoras de hueso. A lo largo de ese trayecto, las células cambiaron su estrategia energética: en lugar de quemar combustible principalmente en sus mitocondrias, se inclinaron hacia una descomposición rápida del azúcar, un estilo metabólico que se observa con frecuencia en el cáncer y en tejidos en crecimiento. Este cambio hacia un uso acelerado de la glucosa —llamado glicólisis— fue especialmente intenso en las células que realmente estaban formando hueso dentro del ligamento.
La quema de azúcar como combustible para el crecimiento óseo rebelde
Para comprobar si este cambio metabólico era simplemente un efecto secundario o un impulsor de la enfermedad, el equipo aisló células del ligamento de pacientes y las observó mientras se las estimulaba para convertirse en células formadoras de hueso en el laboratorio. Las células de pacientes con OPLL absorbieron más glucosa, produjeron más subproductos acidificantes como el lactato y mostraron una actividad mitocondrial más débil que las células normales. Cuando los científicos bloquearon la glicólisis con un fármaco llamado 2-DG, la capacidad de las células para convertirse en formadoras de hueso disminuyó drásticamente y los depósitos minerales que normalmente depositaban se redujeron notablemente. En ratones, ese mismo fármaco redujo las masas óseas inducidas artificialmente y disminuyó el número de células óseas tempranas y maduras, demostrando que cortar esta vía de quema de azúcar puede ralentizar o atenuar el proceso de osificación en animales vivos.
Un interruptor oculto: la reacción en cadena ADAM12–IGF1
Indagando más a fondo, los investigadores buscaron interruptores maestros que pudieran estar activando a las células para entrar en este modo de alta glicólisis. Una molécula, ADAM12, destacó. Estaba fuertemente elevada en tejido OPLL y era más activa en las células del ligamento que estaban en camino de convertirse en hueso. ADAM12 es una enzima que corta proteínas y flota fuera de las células; aquí parece abrir proteínas transportadoras que mantienen un factor de crecimiento llamado IGF1. Al recortar una de estas transportadoras, IGFBP5, ADAM12 libera más IGF1 para activar receptores en las células del ligamento. Eso, a su vez, desencadena una vía de crecimiento conocida dentro de la célula (PI3K–AKT–mTOR), que potencia la maquinaria para descomponer la glucosa y producir lactato. Cuando ADAM12 aumentó en las células, la glicólisis y la producción de lactato se dispararon; cuando se silenció ADAM12 o se inhabilitó su capacidad de corte, ambas disminuyeron.
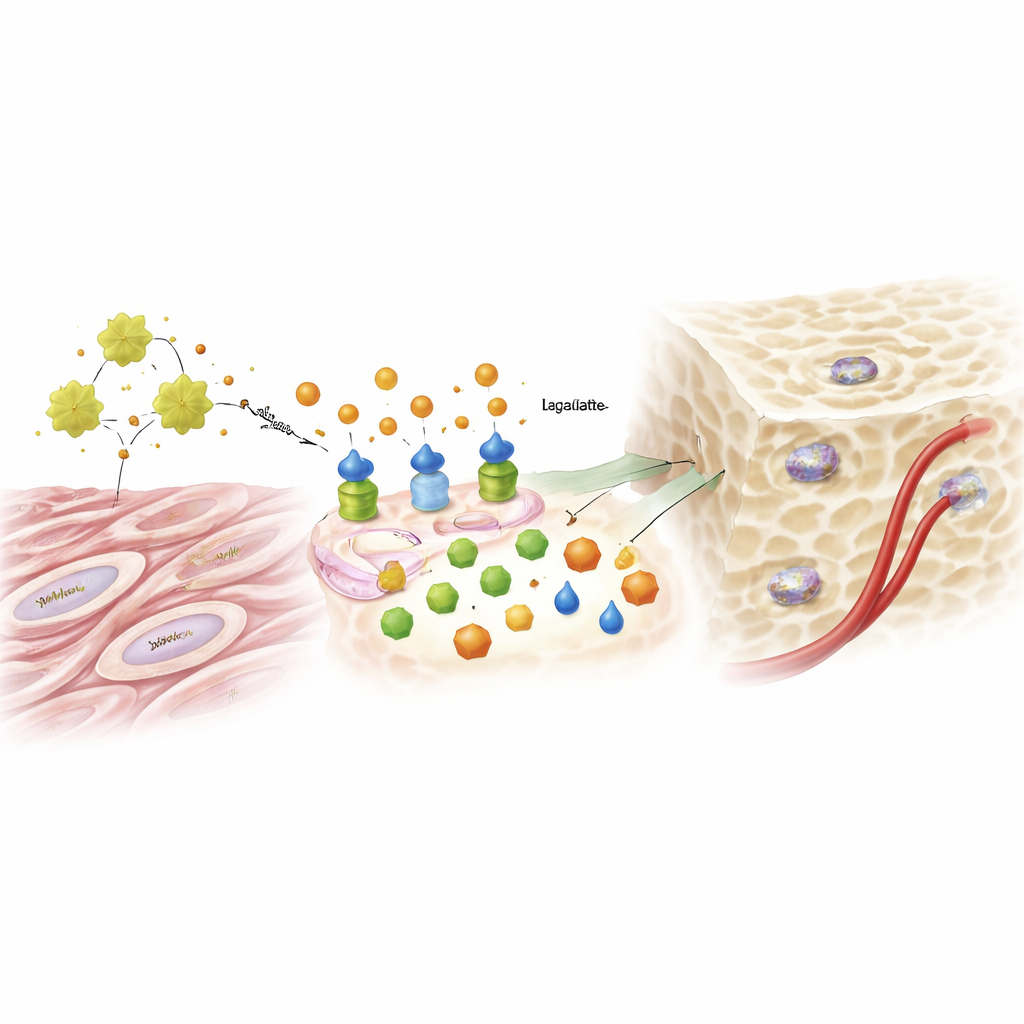
Del subproducto del azúcar a la señal genética
El lactato, durante mucho tiempo desestimado como un desecho metabólico, desempeñó un papel sorprendente. A medida que la glicólisis aumentaba bajo la influencia de ADAM12 e IGF1, los niveles de lactato se elevaron y comenzaron a influir en la forma en que el ADN se empaqueta dentro del núcleo celular. Los investigadores hallaron que el lactato marcaba histonas específicas —las proteínas que organizan el ADN— con una etiqueta química llamada lactilación. Esta etiqueta aflojó regiones del ADN vinculadas a genes formadores de hueso, ayudando a activar factores clave que empujan a una célula a convertirse en osteoblasto. Suministrar lactato adicional pudo rescatar la capacidad formadora de hueso en células donde ADAM12 había sido reducido, mientras que bloquear la glicólisis o la enzima que produce lactato borró el impulso de un exceso de ADAM12. La misma vía impulsada por ADAM12 también aumentó señales que fomentan el crecimiento de vasos sanguíneos, ayudando a suministrar nutrientes al nuevo hueso.
Nuevas vías hacia un tratamiento no quirúrgico
En conjunto, el estudio dibuja una cadena clara de eventos: un aumento de la enzima ADAM12 en los ligamentos espinales libera IGF1 adicional, que activa un programa de crecimiento que reconfigura el uso de azúcar de las células. Esta avalancha de azúcar produce lactato, que a su vez reescribe la actividad de genes relacionados con el hueso y ayuda a construir tanto hueso como vasos sanguíneos en lugares donde no deberían estar. Al bloquear la señalización de IGF1 o la glicólisis, los investigadores pudieron atenuar o revertir este proceso en cultivos celulares y modelos en ratón. Para los pacientes, este trabajo sugiere que dirigirse al eje ADAM12–IGF1–glicólisis podría algún día ofrecer una vía farmacológica para frenar o prevenir la OPLL, reduciendo la necesidad de cirugías espinales de alto riesgo y preservando la movilidad y la función nerviosa.
Cita: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Palabras clave: osificación del ligamento espinal, metabolismo celular, glicólisis, señalización de factores de crecimiento, formación ósea