Clear Sky Science · nl
Glycolytische herprogrammering gemedieerd door de ADAM12/IGF1-as bevordert ossificatie van het posterior longitudinale ligament
Wanneer een steunband in de wervelkolom bot wordt
Diep in de wervelkolom helpt een taaie weefselband, het posterior longitudinale ligament, onze wervels uitgelijnd te houden. Bij sommige mensen, vooral in Oost-Azië, verandert deze flexibele band geleidelijk in bot, waardoor het ruggenmerg wordt samengedrukt en pijn, zwakte of zelfs verlamming kan ontstaan. Deze aandoening, bekend als OPLL, vereist vaak risicovolle chirurgie en heeft momenteel geen medicamenteuze behandeling. De studie die hier wordt samengevat stelt een eenvoudige maar krachtige vraag: wat als de manier waarop deze cellen suiker gebruiken de verborgen motor is achter deze ongewenste botgroei?
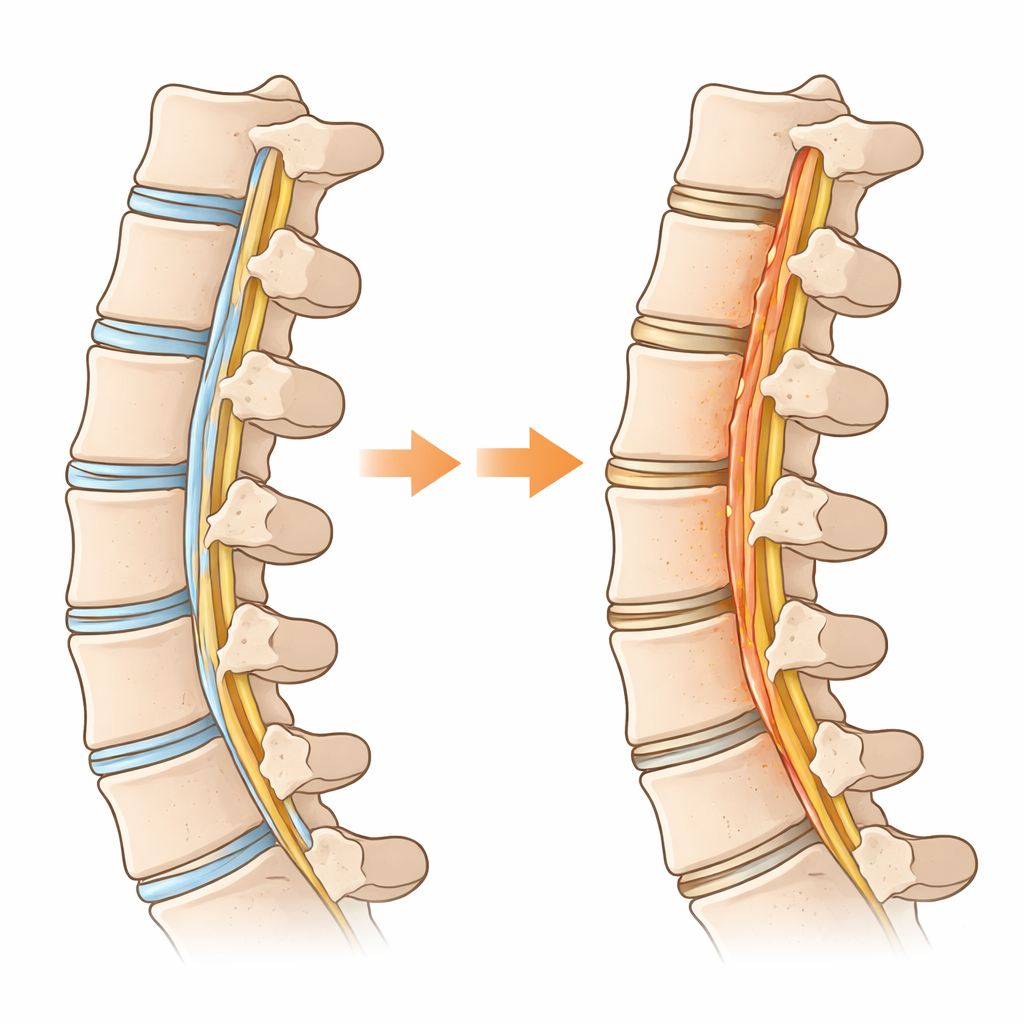
Waarom een spinale band zich als bot begint te gedragen
De onderzoekers vergeleken ziek ligamentweefsel van mensen met OPLL met normaal ligament van patiënten met andere nekklachten. Met grootschalige genanalyses en single-cell-analyse brachten ze in kaart welke celtypen aanwezig waren en wat elke cel aan het doen was. Ze ontdekten dat een subset van ligamentcellen, die normaal gesproken fungeren als reparatie-geschikte “progenitoren”, een pad volgde richting botvormende cellen. Langs dit pad schakelden de cellen hun energiestrategie om: in plaats van vooral brandstof in hun mitochondriën te verbranden, schakelden ze over op snelle suikerafbraak, een stijl van metabolisme die vaak gezien wordt in kanker en groeiend weefsel. Deze omschakeling naar intensief suikergebruik — glycolyse genoemd — was bijzonder sterk in de cellen die daadwerkelijk bot in het ligament vormden.
Suikerverbranding als brandstof voor ontspoorde botgroei
Om te testen of deze metabole verschuiving slechts een bijverschijnsel of een drijvende kracht van de ziekte was, isoleerden de onderzoekers ligamentcellen van patiënten en observeerden ze terwijl die in het laboratorium werden aangespoord om botvormende cellen te worden. Cellen van OPLL-patiënten namen meer glucose op, produceerden meer zuurvormende bijproducten zoals lactaat, en toonden zwakkere mitochondriale activiteit dan normale cellen. Wanneer de wetenschappers glycolyse blokkeerden met een middel genaamd 2-DG, daalde het vermogen van de cellen om osteoblasten te worden sterk en werden de mineraalafzettingen die ze gewoonlijk aanlegden sterk verminderd. Bij muizen kromp hetzelfde middel kunstmatig geïnduceerde botmassa’s en nam het aantal vroege en rijpe botcellen af, wat aantoont dat het afsnijden van deze suikerverbrandingsroute de ossificatie in levende dieren kan vertragen of verzachten.
Een verborgen schakelaar: de ADAM12–IGF1-ketenreactie
Dieper gravend zochten de onderzoekers naar hoofdregelaars die de cellen mogelijk in deze hoge-glycolyse-modus zetten. Eén molecuul, ADAM12, stak daarbij bovenaanuit. Het was sterk verhoogd in OPLL-weefsel en het was het actiefst in ligamentcellen die op weg waren bot te worden. ADAM12 is een eiwitsplitsend enzym dat buiten de cel rondhangt, en hier lijkt het draag-eiwitten te knippen die een groeisignaal genaamd IGF1 vasthouden. Door één van deze dragers, IGFBP5, te knippen, bevrijdt ADAM12 meer IGF1 om receptoren op ligamentcellen te activeren. Dat activeert op zijn beurt een bekende groeiroute binnen de cel (PI3K–AKT–mTOR), die de machinerie voor het afbreken van glucose en de productie van lactaat opvoert. Wanneer ADAM12 in cellen werd verhoogd, stegen glycolyse en lactaatproductie; wanneer het werd uitgeschakeld of zijn knipactiviteit werd uitgeschakeld, daalden beide.
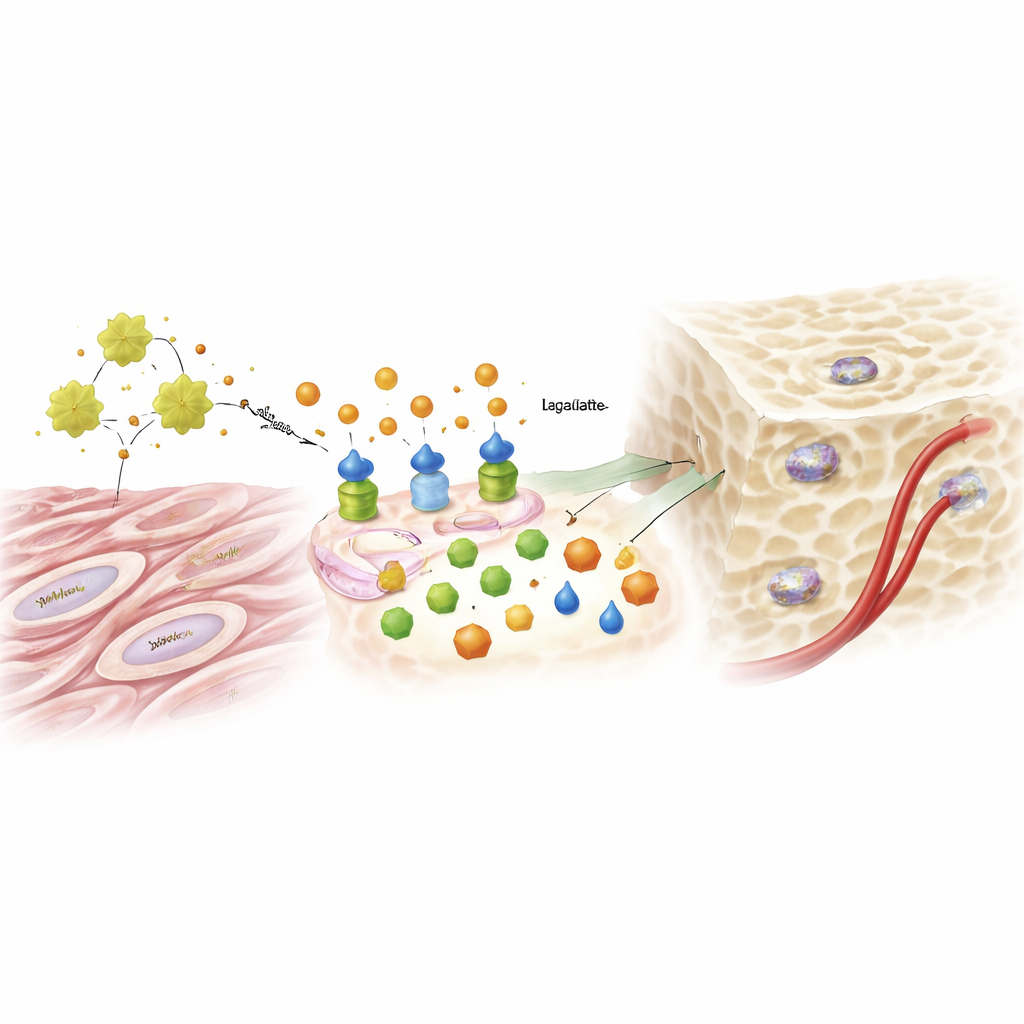
Van suikervijproduct naar genetisch signaal
Lactaat, lang afgedaan als metabool afval, speelde een verrassende hoofdrol. Toen glycolyse onder invloed van ADAM12 en IGF1 toenam, stegen de lactaatniveaus en begonnen ze de manier waarop DNA in de celkern is verpakt te beïnvloeden. De onderzoekers ontdekten dat lactaat specifieke histonen — de eiwitten die DNA organiseren — voorzag van een chemische markering genaamd lactylatie. Deze markering maakte DNA-regio’s die gekoppeld zijn aan botvorming losser, waardoor belangrijke factoren werden geactiveerd die een cel in de richting van een osteoblast duwen. Het toedienen van extra lactaat kon het vermogen tot botvorming herstellen in cellen waarin ADAM12 was geremd, terwijl het blokkeren van glycolyse of het enzym dat lactaat maakt de stimulans door extra ADAM12 uitwiste. Dezelfde ADAM12-gedreven route verhoogde ook signalen die bloedvatgroei aanmoedigen, waardoor nutriëntenvoorziening naar het nieuwe bot verbeterde.
Nieuwe wegen naar niet-chirurgische behandeling
Alles bij elkaar schetst de studie een helder ketenverloop: een toename van het enzym ADAM12 in spinale ligamenten ontgrendelt extra IGF1, wat een groeiprogramma activeert dat de suikerhuishouding van cellen herbedraad. Deze suikerstroom produceert lactaat, dat vervolgens de activiteit van botgerelateerde genen herschrijft en helpt zowel bot als bloedvaten op plaatsen te bouwen waar ze niet thuishoren. Door IGF1-signaleringsroutes of glycolyse te blokkeren, konden de onderzoekers dit proces afzwakken of omkeren in celkweken en muismodellen. Voor patiënten suggereert dit werk dat het richten op de ADAM12–IGF1–glycolyse-as mogelijk op termijn een medicamenteuze manier biedt om OPLL te vertragen of te voorkomen, waardoor de noodzaak voor risicovolle wervelkolomchirurgie afneemt en mobiliteit en zenuwfunctie behouden kunnen blijven.
Bronvermelding: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Trefwoorden: verkalking van spinale ligamenten, celmetabolisme, glycolyse, groeifactor signalering, botvorming