Clear Sky Science · pt
Reprogramação glicolítica mediada pelo eixo ADAM12/IGF1 promove a ossificação do ligamento longitudinal posterior
Quando uma Banda de Sustentação da Coluna se Transforma em Osso
Nas profundezas da coluna, uma faixa resistente de tecido chamada ligamento longitudinal posterior ajuda a manter as vértebras alinhadas. Em algumas pessoas, especialmente no Leste Asiático, essa tira flexível gradualmente se transforma em osso, comprimindo a medula espinhal e causando dor, fraqueza ou até paralisia. Essa condição, conhecida como OPLL, geralmente exige cirurgia arriscada e atualmente não tem tratamento medicamentoso. O estudo resumido aqui faz uma pergunta simples, porém poderosa: e se a forma como essas células usam açúcar for o motor oculto que impulsiona esse crescimento ósseo indesejado?
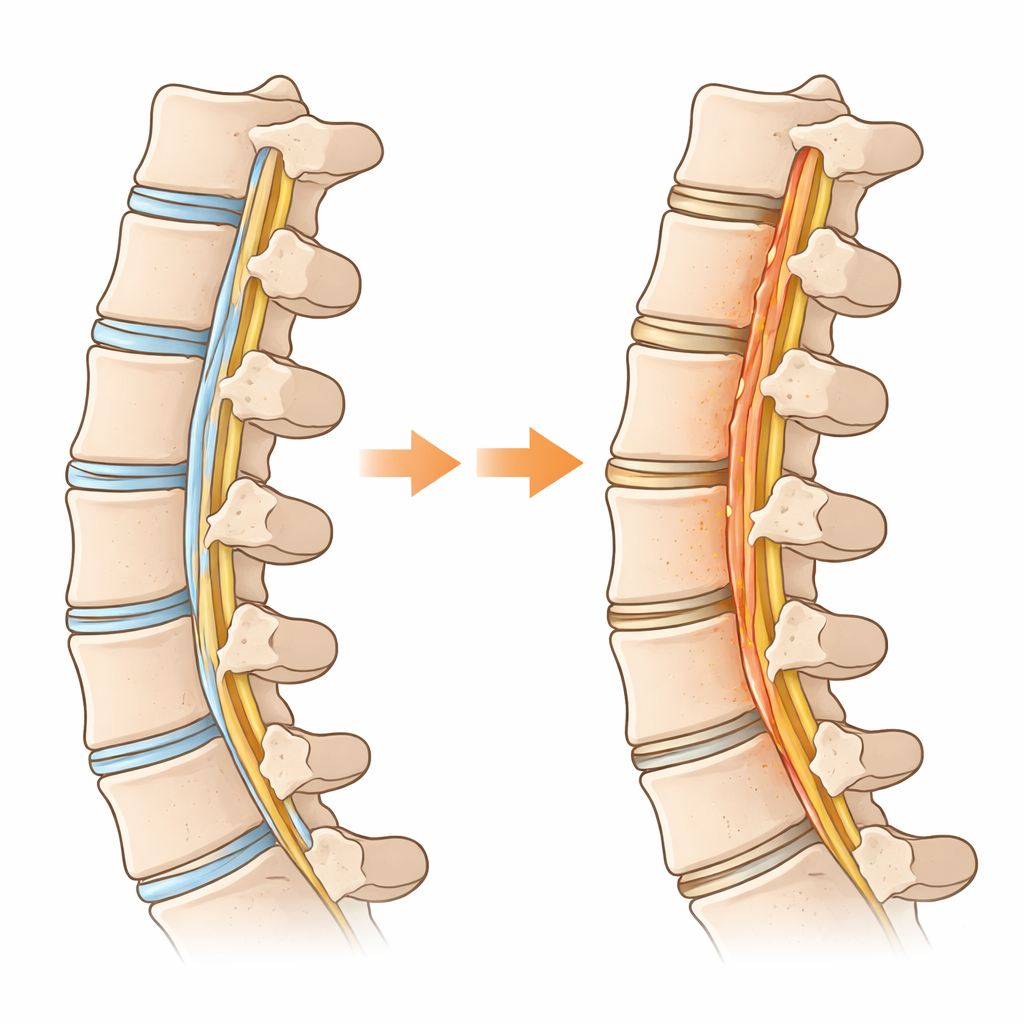
Por que um Ligamento Espinhal Começa a se Comportar como Osso
Os pesquisadores compararam tecido ligamentar doente de pessoas com OPLL com ligamento normal de pacientes com outros problemas cervicais. Utilizando análises genômicas em larga escala e de célula única, mapearam quais tipos celulares estavam presentes e o que cada célula estava fazendo. Eles descobriram que um subconjunto de células do ligamento, que normalmente atuam como “progenitores” prontos para reparo, vinha seguindo um caminho rumo à diferenciação em células formadoras de osso. Ao longo desse trajeto, as células mudaram sua estratégia energética: em vez de principalmente queimar combustível nas mitocôndrias, deslocaram-se para uma quebra rápida de açúcar, um estilo de metabolismo frequentemente observado em cânceres e tecidos em crescimento. Essa mudança para uso acelerado da glicose — chamada glicólise — foi especialmente forte nas células que realmente estavam formando osso dentro do ligamento.
Queima de Açúcar como Combustível para o Crescimento Ósseo Fora de Controle
Para testar se essa mudança metabólica era mero espectador ou um motor da doença, a equipe isolou células do ligamento de pacientes e as observou enquanto eram induzidas a se tornar osteoblastos em laboratório. Células de pacientes com OPLL absorveram mais glicose, produziram mais subprodutos formadores de ácido como o lactato e mostraram atividade mitocondrial mais fraca do que células normais. Quando os cientistas bloquearam a glicólise com um fármaco chamado 2-DG, a capacidade das células de se transformar em formadoras de osso caiu drasticamente, e os depósitos minerais que normalmente formavam foram muito reduzidos. Em camundongos, o mesmo fármaco diminuiu massas ósseas induzidas artificialmente e reduziu o número de células ósseas em estágios iniciais e maduras, mostrando que cortar essa via de queima de açúcar pode retardar ou atenuar o processo de ossificação em animais vivos.
Um Interruptor Oculto: a Reação em Cadeia ADAM12–IGF1
Aprofundando-se, os pesquisadores buscaram por chaves mestras que pudessem estar direcionando as células a esse modo de alta glicólise. Uma molécula, ADAM12, destacou-se. Estava fortemente elevada no tecido OPLL e era mais ativa nas células ligamentares em trajetória de formação óssea. ADAM12 é uma enzima que cliva proteínas e atua fora das células, e aqui parece cortar proteínas transportadoras que prendem um sinal de crescimento chamado IGF1. Ao aparar uma dessas transportadoras, IGFBP5, o ADAM12 libera mais IGF1 para ativar receptores nas células ligamentares. Isso, por sua vez, aciona uma via de crescimento bem conhecida dentro da célula (PI3K–AKT–mTOR), que impulsiona a maquinaria para degradar glicose e produzir lactato. Quando o ADAM12 foi aumentado nas células, a glicólise e a produção de lactato dispararam; quando foi silenciado ou sua capacidade de clivagem foi desativada, ambos caíram.
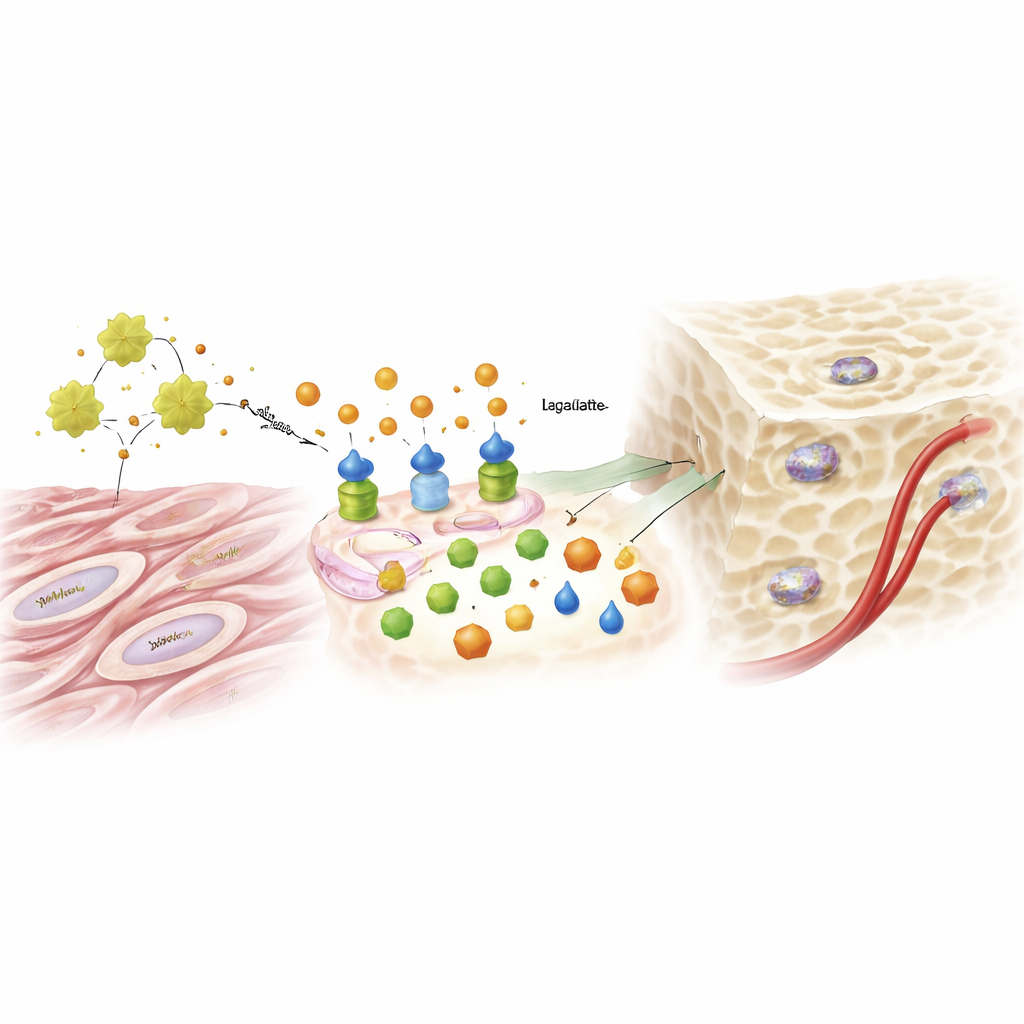
Do Subproduto Glicídico ao Sinal Genético
O lactato, por muito tempo descartado como resíduo metabólico, desempenhou um papel surpreendente. Conforme a glicólise aumentava sob a influência de ADAM12 e IGF1, os níveis de lactato subiam e começaram a influenciar a forma como o DNA é embalado no núcleo celular. Os pesquisadores descobriram que o lactato decorava histonas específicas — as proteínas que organizam o DNA — com uma marca química chamada lactilação. Essa marca afrouxou regiões do DNA ligadas a genes formadores de osso, ajudando a ativar fatores-chave que empurram uma célula a se tornar um osteoblasto. Fornecer lactato adicional poderia resgatar a capacidade de formar osso em células onde o ADAM12 havia sido silenciado, enquanto bloquear a glicólise ou a enzima que produz lactato eliminava o impulso causado pelo excesso de ADAM12. A mesma via dirigida por ADAM12 também aumentou sinais que incentivam o crescimento de vasos sanguíneos, ajudando a suprir nutrientes ao novo osso.
Novos Caminhos Rumo a Tratamento Não Cirúrgico
Em conjunto, o estudo delineia uma cadeia clara de eventos: o aumento da enzima ADAM12 nos ligamentos espinhais desbloqueia IGF1 extra, que ativa um programa de crescimento que reconfigura o uso de açúcar pelas células. Essa explosão de açúcar produz lactato, que então reescreve a atividade de genes relacionados ao osso e ajuda a construir tanto osso quanto vasos sanguíneos em locais onde não deveriam estar. Ao bloquear a sinalização do IGF1 ou a glicólise, os pesquisadores conseguiram atenuar ou reverter esse processo em culturas celulares e em modelos murinos. Para os pacientes, esse trabalho sugere que mirar no eixo ADAM12–IGF1–glicólise poderá, um dia, oferecer uma abordagem medicamentosa para desacelerar ou prevenir a OPLL, reduzindo a necessidade de cirurgias espinhais de alto risco e preservando mobilidade e função nervosa.
Citação: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Palavras-chave: ossificação do ligamento espinhal, metabolismo celular, glicólise, sinalização por fatores de crescimento, formação óssea