Clear Sky Science · sv
Glykolytisk omprogrammering medierad av ADAM12/IGF1-axeln främjar förbening av den posteriora longitudinella ligamentet
När ett stödband i ryggraden blir ben
Djupt inne i ryggraden hjälper en seg vävnadsremsa, det posteriora longitudinella ligamentet, till att hålla våra kotor i linje. Hos vissa människor, särskilt i Östasien, omvandlas denna flexibla remsa gradvis till ben, vilket trycker på ryggmärgen och orsakar smärta, svaghet eller till och med förlamning. Detta tillstånd, känt som OPLL, kräver ofta riskfylld kirurgi och saknar i dag läkemedelsbehandling. Studien som sammanfattas här ställer en enkel men kraftfull fråga: vad om sättet dessa celler använder socker på är den dolda motorn bakom denna oönskade bennybildning?
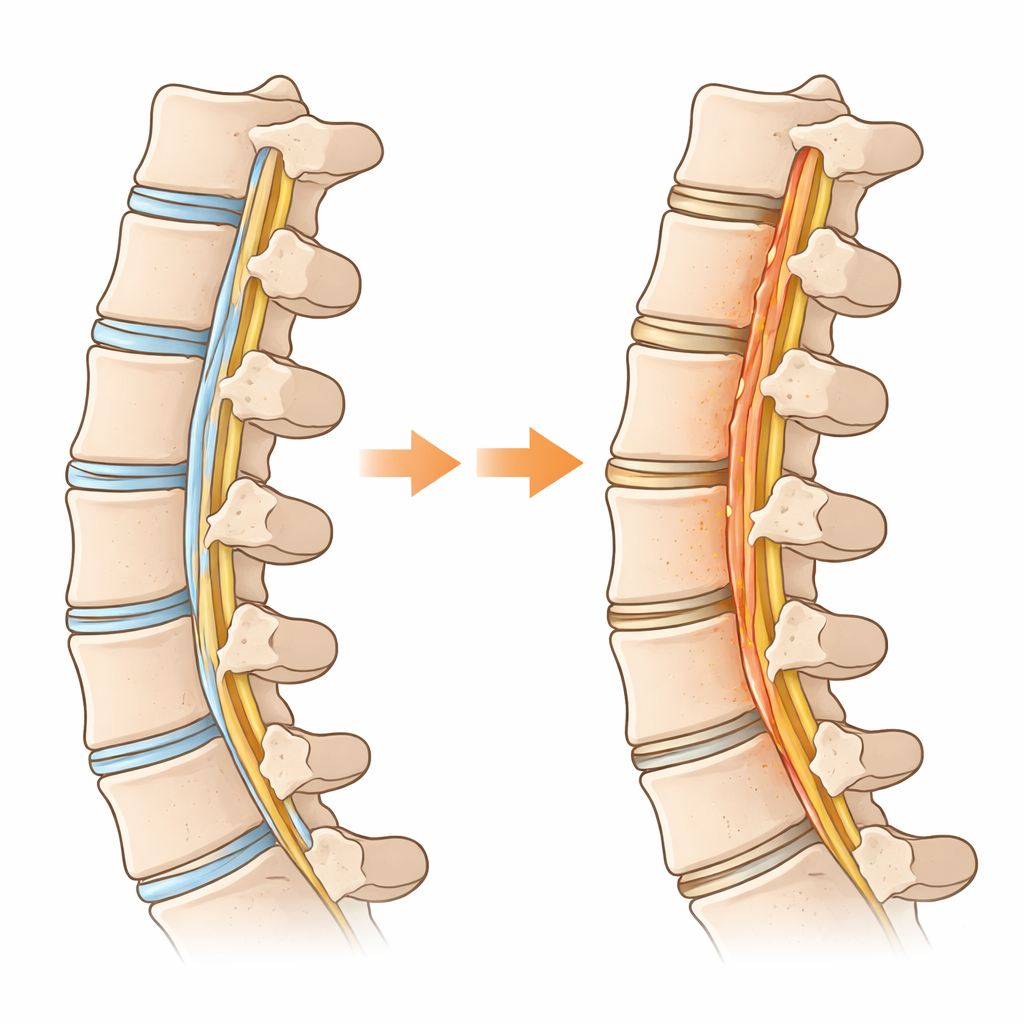
Varför ett spinalt ligament börjar uppträda som ben
Forskarna jämförde sjuklig ligamentvävnad från personer med OPLL med normalt ligament från patienter med andra nackproblem. Med hjälp av storskaliga genanalyser och enkelcellsteknik kartlade de vilka celltyper som fanns och vad varje cell gjorde. De fann att en delmängd av ligamentcellerna, som normalt fungerar som reparationsberedda ”progenitorer”, följde en bana mot att bli bennybildande celler. Längs denna bana bytte cellerna energistrategi: istället för att huvudsakligen bränna bränsle i sina mitokondrier skiftade de mot snabb nedbrytning av socker, en typ av metabolism som ofta ses i cancer och växande vävnader. Denna växling till högaktiv sockeranvändning—kallad glykolys—var särskilt stark i de celler som faktiskt bildade ben inne i ligamentet.
Sockerförbränning som bränsle för felriktad bennybildning
För att undersöka om denna metabola förändring bara var en åskådare eller en drivkraft i sjukdomen isolerade teamet ligamentceller från patienter och följde dem när de stimulerades att bli bennybildande celler i laboratoriet. Celler från OPLL-patienter tog upp mer glukos, producerade fler syrabildande biprodukter såsom laktat, och visade svagare mitokondrieaktivitet än normala celler. När forskarna blockerade glykolys med ett läkemedel kallat 2-DG sjönk cellernas förmåga att differentiera till bennybildande celler kraftigt, och de mineralavlagringar de normalt lade ner minskade avsevärt. Hos möss krympte samma läkemedel konstgjorda benmassor och minskade antalet tidiga och mogna benceller, vilket visar att avstängning av denna sockerförbränningsväg kan bromsa eller mildra förbeningsprocessen i levande djur.
En dold brytare: ADAM12–IGF1-kedjereaktionen
Genom att gräva djupare letade forskarna efter huvudsakliga brytare som kan sätta cellerna i detta högglykolytiska läge. En molekyl, ADAM12, stack ut. Den var starkt förhöjd i OPLL-vävnad och mest aktiv i ligamentceller som var på väg att bli ben. ADAM12 är ett protein-klövande enzym som befinner sig utanför cellerna, och här verkar det skära upp bärarproteiner som håller kvar en tillväxtsignal kallad IGF1. Genom att trimma ett av dessa bärarproteiner, IGFBP5, frigör ADAM12 mer IGF1 så att det kan aktivera receptorer på ligamentcellerna. Det triggar i sin tur en välkänd tillväxtväg inne i cellen (PI3K–AKT–mTOR), som förstärker maskineriet för att bryta ner glukos och producera laktat. När ADAM12 ökades i celler steg glykolys och laktatproduktion; när det tystades eller dess klyvningsförmåga inaktiverades minskade båda.
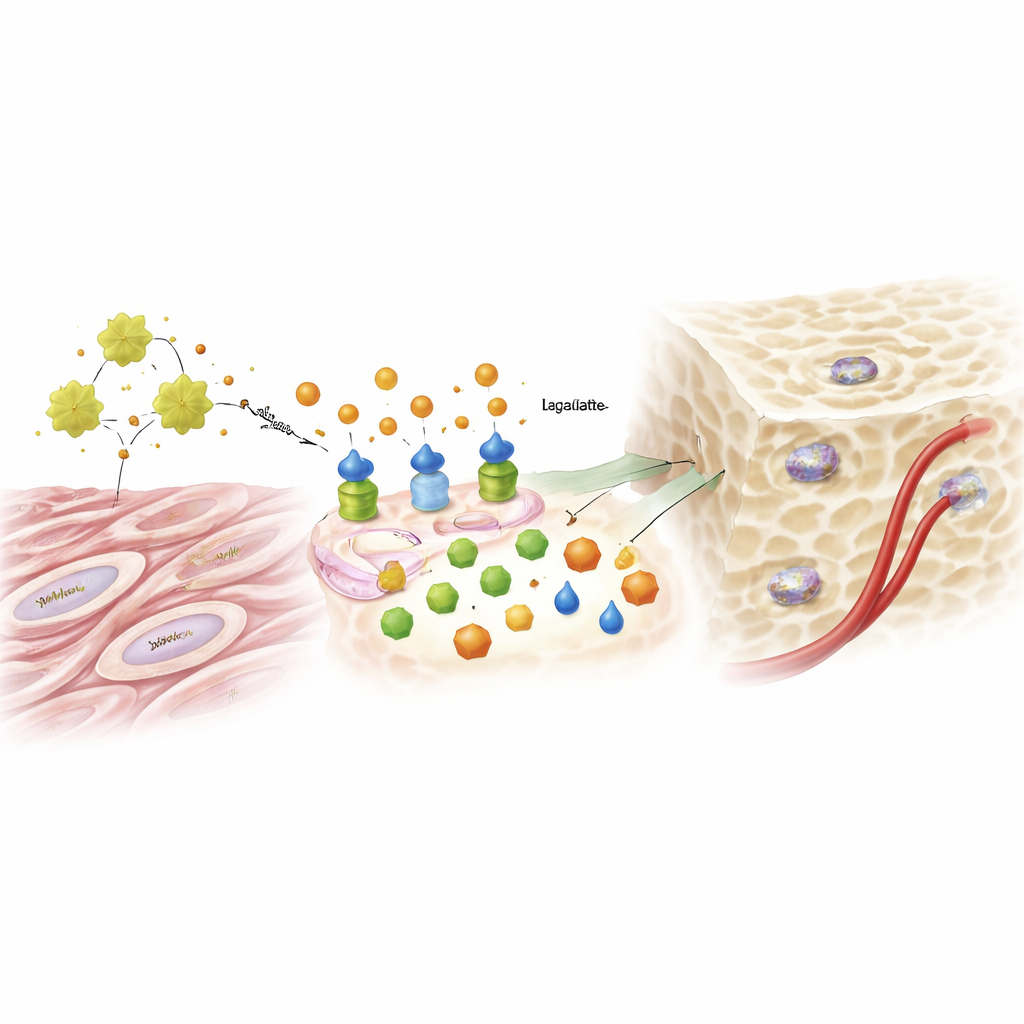
Från sockerbiprodukt till genetisk signal
Laktat, länge avfärdat som metabolt avfall, spelade en överraskande huvudroll. När glykolysen ökade under påverkan av ADAM12 och IGF1 steg laktatnivåerna och började påverka hur DNA packas inne i cellkärnan. Forskarna fann att laktat dekorerade specifika histoner—proteinerna som organiserar DNA—med en kemisk märkning kallad laktolylering. Denna märkning luckrade upp DNA-regioner kopplade till bennybildande gener, vilket hjälpte till att slå på nyckelfaktorer som pressar en cell att bli en osteoblast. Tillskott av extra laktat kunde återställa bennybildande förmåga i celler där ADAM12 hade tystats, medan blockering av glykolys eller enzymet som gör laktat utplånade effekten av extra ADAM12. Samma ADAM12-drivna väg ökade också signaler som uppmuntrar blodkärlstillväxt och bidrog därigenom till att förse det nya benet med näring.
Nya vägar mot icke-kirurgisk behandling
Tillsammans målar studien upp en tydlig händelsekedja: en ökning av enzymet ADAM12 i spinala ligament frigör extra IGF1, vilket aktiverar ett tillväxtprogram som omprogrammerar hur celler använder socker. Denna sockerökning producerar laktat, som sedan omskriver aktiviteten hos benrelaterade gener och hjälper till att bygga både ben och blodkärl på platser där de inte hör hemma. Genom att blockera IGF1-signalering eller glykolys kunde forskarna dämpa eller vända denna process i cellkulturer och musmodeller. För patienter antyder detta arbete att inriktning på ADAM12–IGF1–glykolys-axeln en dag skulle kunna erbjuda en läkemedelsbaserad metod för att bromsa eller förebygga OPLL, minska behovet av hög-riskryggkirurgi och bevara rörlighet och nervfunktion.
Citering: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Nyckelord: förbening av spinala ligament, cellmetabolism, glykolys, tillväxtfaktor-signalering, bennybildning