Clear Sky Science · ru
Гликолитическая перепрограммировка, опосредованная осью ADAM12/IGF1, способствует окостенению задней позвонковой связки
Когда поддерживающая лента в позвоночнике превращается в кость
Глубоко в позвоночнике прочная полоса ткани, называемая задней позвонковой связкой, помогает удерживать позвонки в правильной линии. У некоторых людей, особенно в Восточной Азии, эта гибкая лента постепенно превращается в кость, сдавливая спинной мозг и вызывая боль, слабость или даже паралич. Это состояние, известное как OPLL, обычно требует рискованной операции и в настоящее время не имеет лекарственного лечения. В исследовании, изложенном здесь, поставлен простой, но важный вопрос: не является ли способ использования клетками сахара скрытым двигателем этого нежелательного роста кости?
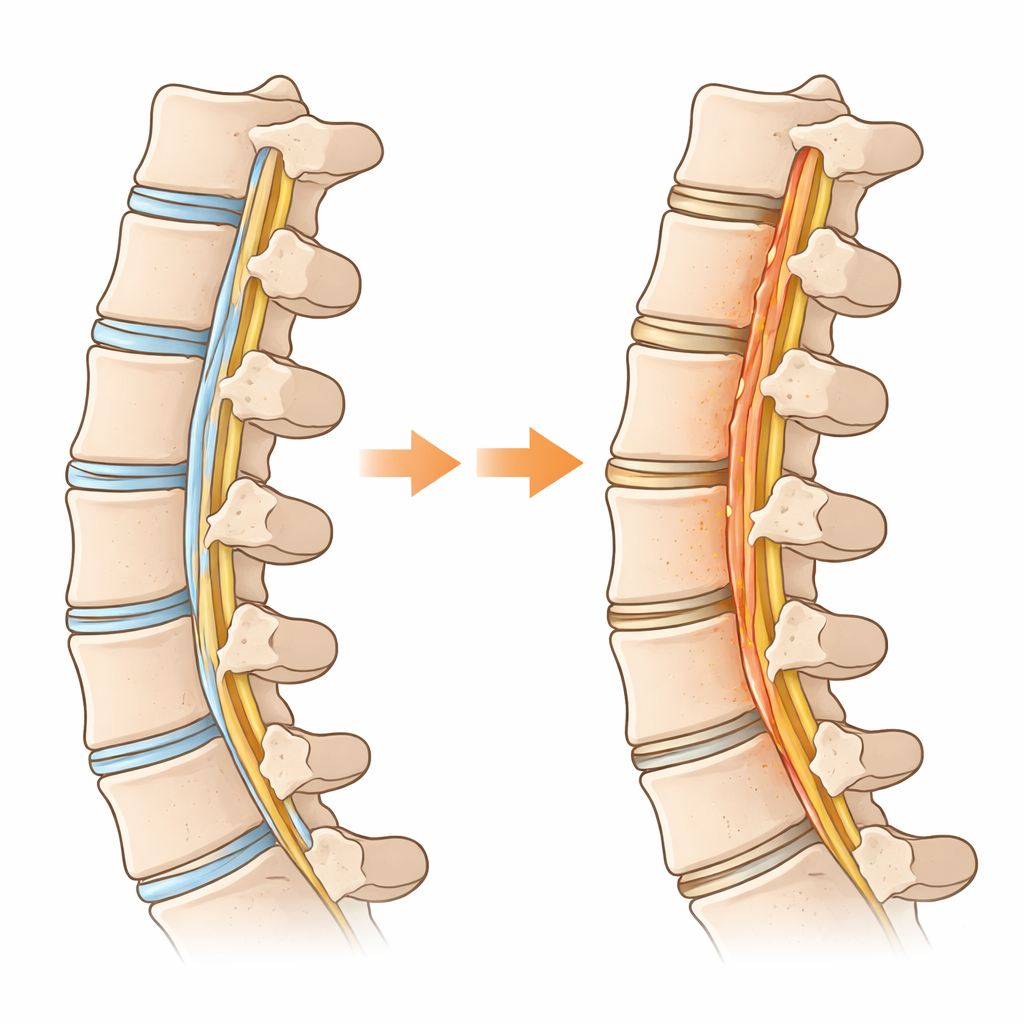
Почему позвонковая связка начинает вести себя как кость
Исследователи сравнили поражённую ткань связки у пациентов с OPLL с нормальной связкой у больных с другими шейными заболеваниями. С помощью масштабных геномных и одно-клеточных анализов они нанесли на карту, какие типы клеток присутствуют и чем каждая из них занимается. Они обнаружили, что подмножество клеток связки, которые в норме служат «прогениторами», готовыми к ремонту, направляется по пути становления клетками, формирующими кость. По ходу этого пути клетки сменили энергетическую стратегию: вместо преимущественного использования митохондрий они переключились на быстрый разбор сахара — тип метаболизма, часто наблюдаемый в опухолях и растущих тканях. Этот переход к высокоскоростному потреблению сахара — гликолиз — был особенно выражен в клетках, которые фактически образовывали кость внутри связки.
Сжигание сахара как топливо для «бунтарского» образования кости
Чтобы проверить, является ли это метаболическое изменение просто сопутствующим явлением или же движущим фактором болезни, команда выделила клетки связки у пациентов и наблюдала за ними, когда их побуждали превращаться в остеобласты в лаборатории. Клетки из пациентов с OPLL поглощали больше глюкозы, производили больше кислотообразующих побочных продуктов, таких как лактат, и демонстрировали ослабленную митохондриальную активность по сравнению с нормальными клетками. Когда учёные блокировали гликолиз препаратом 2‑DG, способность клеток дифференцироваться в остеобласты резко падала, а минеральные отложения, которые они обычно формировали, значительно уменьшались. В мышиной модели тот же препарат уменьшал искусственно индуцированные костные массы и снижал число ранних и зрелых костных клеток, показывая, что прерывание пути сжигания сахара может замедлить или смягчить процесс окостенения в живом организме.
Скрытый переключатель: каскад ADAM12–IGF1
Копнув глубже, исследователи искали «мастер‑переключатели», которые могли бы переводить клетки в режим высокого гликолиза. Одна молекула, ADAM12, выделилась особенно сильно. Она была значительно повышена в ткани OPLL и наиболее активна в клетках связки, направляющихся к остеогенезу. ADAM12 — это внеклеточная протеиназа, и, по-видимому, здесь она разрезает носительные белки, удерживающие сигнальный фактор роста IGF1. Подрезая один из таких переносчиков, IGFBP5, ADAM12 освобождает больше IGF1 для активации рецепторов на клетках связки. Это, в свою очередь, включает известный внутриклеточный сигнальный путь (PI3K–AKT–mTOR), который усиливает механизмы разложения глюкозы и производства лактата. При повышении экспрессии ADAM12 гликолиз и выработка лактата возрастали; при его заглушении или утрате протеазной активности оба процесса снижались.
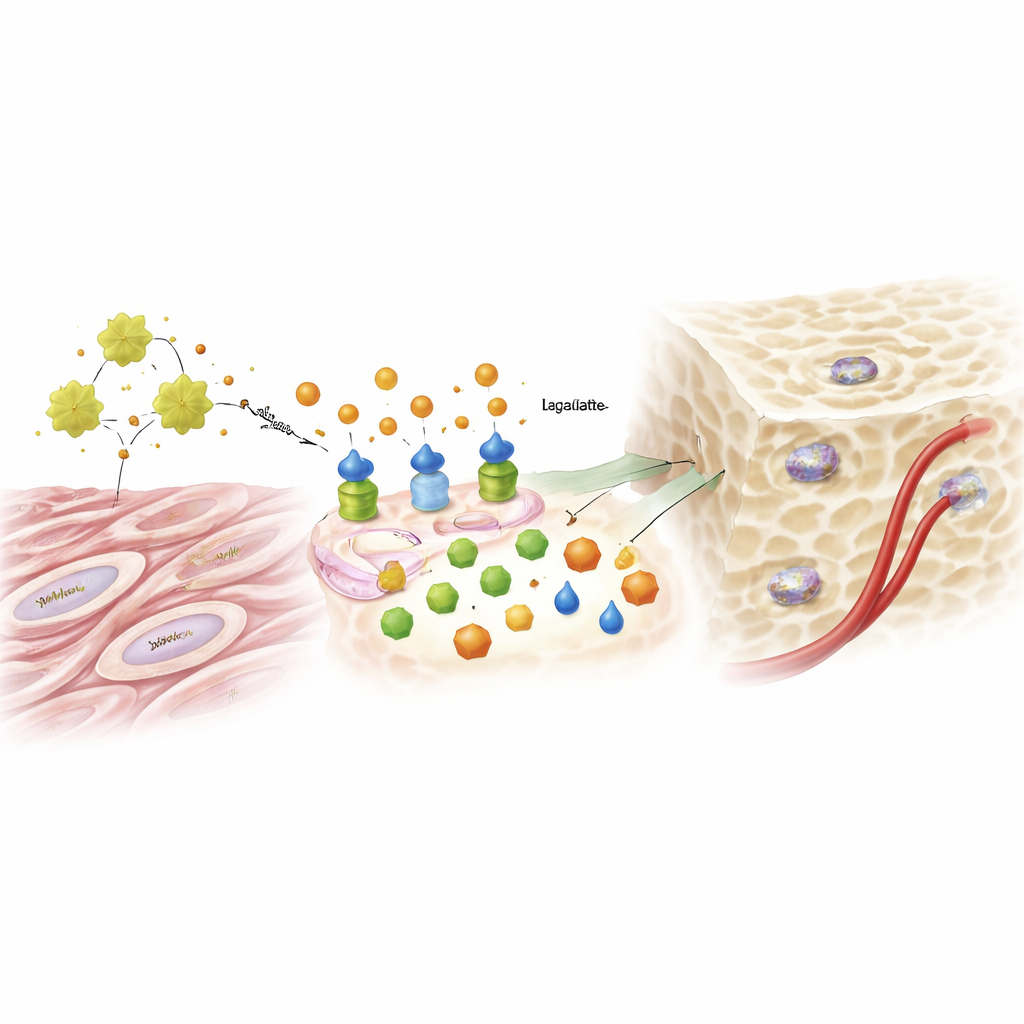
От побочного продукта сахара к генетическому сигналу
Лактат, долгие годы считающийся метаболическим «мусором», сыграл неожиданно важную роль. По мере того как гликолиз усиливался под влиянием ADAM12 и IGF1, уровень лактата поднимался и начал влиять на упаковку ДНК в ядре клетки. Исследователи обнаружили, что лактат модифицирует специфические гистоны — белки, организующие ДНК — с помощью метки, называемой лактиляцией. Эта метка разрыхляла участки ДНК, связанные с генами остеогенеза, способствуя включению ключевых факторов, направляющих клетку к становлению остеобластом. Добавление лишнего лактата могло восстановить способность к образованию кости в клетках с пониженной экспрессией ADAM12, тогда как блокирование гликолиза или фермента, синтезирующего лактат, стирало эффект от увеличения ADAM12. Тот же путь, запущенный ADAM12, также усиливал сигналы, способствующие росту сосудов, помогая снабдить новую кость питательными веществами.
Новые пути к нехирургическому лечению
В совокупности исследование рисует ясную цепочку событий: повышение уровня фермента ADAM12 в позвоночных связках освобождает дополнительный IGF1, который включает программу роста, переписывающую клеточный сахарный обмен. Этот прилив метаболизма производит лактат, который затем перепрограммирует активность генов, связанных с образованием кости, и способствует построению кости и сосудов в тех местах, где им не место. Блокируя сигнальную передачу IGF1 или гликолиз, исследователи смогли ослабить или обратить этот процесс в культурах клеток и на мышиных моделях. Для пациентов это исследование указывает на то, что таргетирование оси ADAM12–IGF1–гликолиз однажды может предложить фармакологический способ замедлить или предотвратить OPLL, снизив потребность в высокорискованных операциях на позвоночнике и сохранив подвижность и функцию нервов.
Цитирование: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Ключевые слова: окостенение позвоночной связки, клеточный метаболизм, гликолиз, сигналы факторов роста, образование кости