Clear Sky Science · de
Glykolytische Umprogrammierung vermittelt durch die ADAM12/IGF1-Achse fördert die Ossifikation des hinteren Längsbandes
Wenn ein Stützband in der Wirbelsäule zu Knochen wird
Tief im Inneren der Wirbelsäule sorgt ein zähes Gewebeband, das hintere Längsband, dafür, dass unsere Wirbel ausgerichtet bleiben. Bei manchen Menschen, vor allem in Ostasien, verwandelt sich dieses flexible Band im Laufe der Zeit in Knochen und drückt auf das Rückenmark, was Schmerzen, Schwäche oder sogar Lähmungen verursachen kann. Diese Erkrankung, bekannt als OPLL, erfordert meist riskante Operationen und hat derzeit keine medikamentöse Behandlung. Die hier zusammengefasste Studie stellt eine einfache, aber wirkungsvolle Frage: Könnte die Art und Weise, wie diese Zellen Zucker verwerten, der verborgene Motor für dieses unerwünschte Knochenwachstum sein?
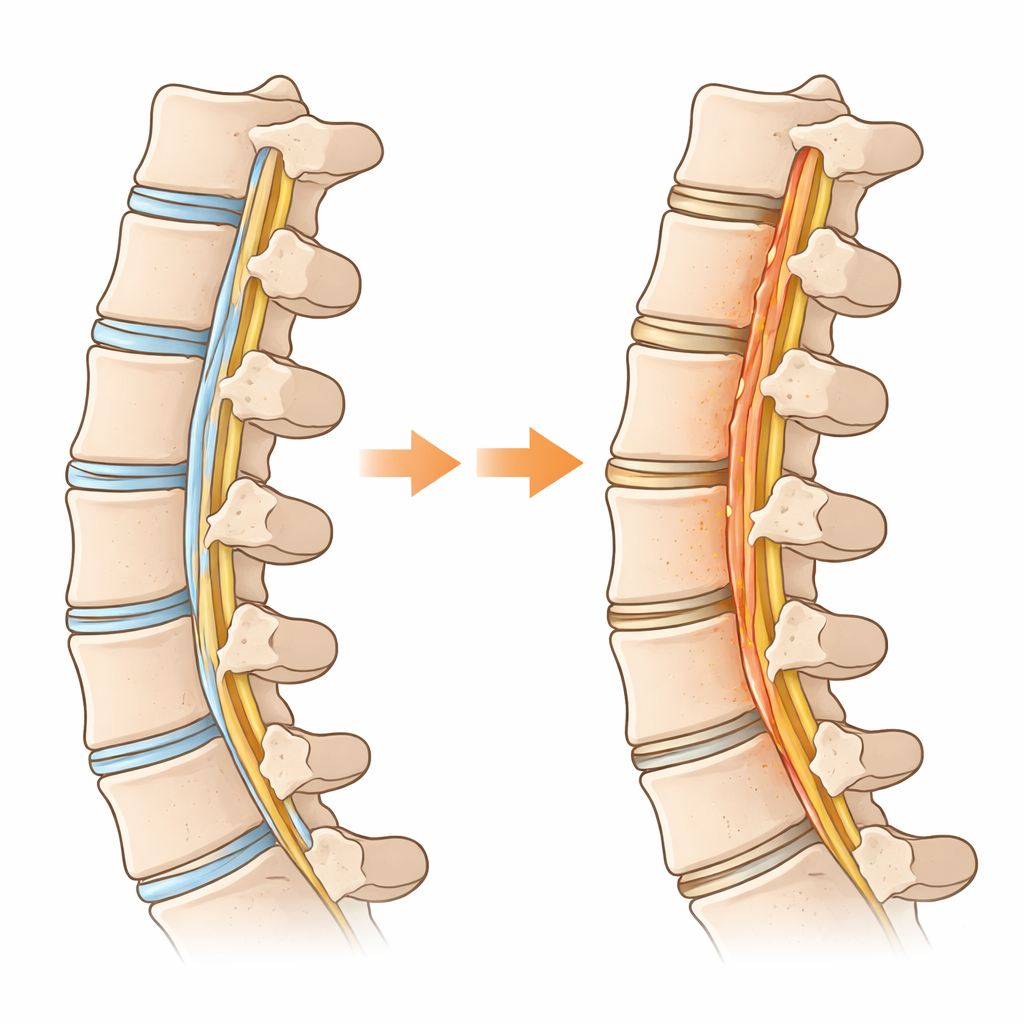
Warum ein Wirbelsäulenband sich wie Knochen verhält
Die Forschenden verglichen erkranktes Bandgewebe von OPLL-Patienten mit normalem Bandgewebe von Patientinnen und Patienten mit anderen Nackenproblemen. Mit groß angelegten Gen- und Einzelzelldaten kartierten sie, welche Zelltypen vorhanden waren und was jede Zelle tat. Sie fanden heraus, dass eine Untergruppe von Bandzellen, die normalerweise als reparaturbereite „Progenitoren“ fungiert, auf dem Weg war, knochenbildende Zellen zu werden. Auf diesem Weg wechselten die Zellen ihre Energieverwendung: Anstatt hauptsächlich in den Mitochondrien zu oxidieren, verlagerten sie sich zu schnellem Zuckerabbau, einer Stoffwechselweise, die oft in Krebs und in wachsenden Geweben zu sehen ist. Dieser Wechsel zu verstärkter Zuckerverbrennung — Glykolyse genannt — war besonders ausgeprägt in den Zellen, die tatsächlich Knochen im Band bildeten.
Zuckerverbrennung als Treibstoff für abweichendes Knochenwachstum
Um zu prüfen, ob dieser Stoffwechselumschlag nur ein Nebeneffekt oder ein Krankheitsmotor ist, isolierte das Team Bandzellen von Patientinnen und Patienten und beobachtete sie, während sie im Labor zur Knochenbildung angeregt wurden. Zellen aus OPLL-Gewebe nahmen mehr Glukose auf, produzierten mehr säurebildende Nebenprodukte wie Laktat und zeigten geringere mitochondriale Aktivität als normale Zellen. Wenn die Wissenschaftler die Glykolyse mit einem Wirkstoff namens 2-DG blockierten, sank die Fähigkeit der Zellen, zu knochenbildenden Zellen zu werden, deutlich, und die normalerweise abgelagerten Mineralien wurden stark reduziert. Bei Mäusen verkleinerte derselbe Wirkstoff künstlich induzierte Knochenwucherungen und verringerte die Zahl früher und reifer Knochenzellen, was zeigt, dass das Abschneiden dieses Zuckerabbauwegs die Ossifikation in lebenden Tieren verlangsamen oder abschwächen kann.
Ein verborgener Schalter: die ADAM12–IGF1-Kettenreaktion
Bei tiefergehender Suche nach Master-Reglern, die die Zellen in diesen high-Glykolyse-Modus versetzen könnten, stach ein Molekül besonders hervor: ADAM12. Es war in OPLL-Gewebe stark erhöht und am aktivsten in den Bandzellen, die sich in Richtung Knochenentwicklung bewegten. ADAM12 ist eine außerhalb der Zelle wirkende Protein-spaltende Enzymfamilie, und hier scheint es Bindungsproteine zu zerschneiden, die ein Wachstumssignal namens IGF1 festhalten. Durch das Abschneiden eines solchen Trägerproteins, IGFBP5, befreit ADAM12 mehr IGF1, sodass dieses an Rezeptoren der Bandzellen binden kann. Das aktiviert wiederum einen bekannten Wachstumsweg im Zellinneren (PI3K–AKT–mTOR), der die Maschinerie für Glukoseabbau und Laktatproduktion hochfährt. Wenn ADAM12 in Zellen erhöht war, stiegen Glykolyse und Laktatproduktion; wurde es stillgelegt oder seine Spaltfunktion deaktiviert, fielen beide ab.
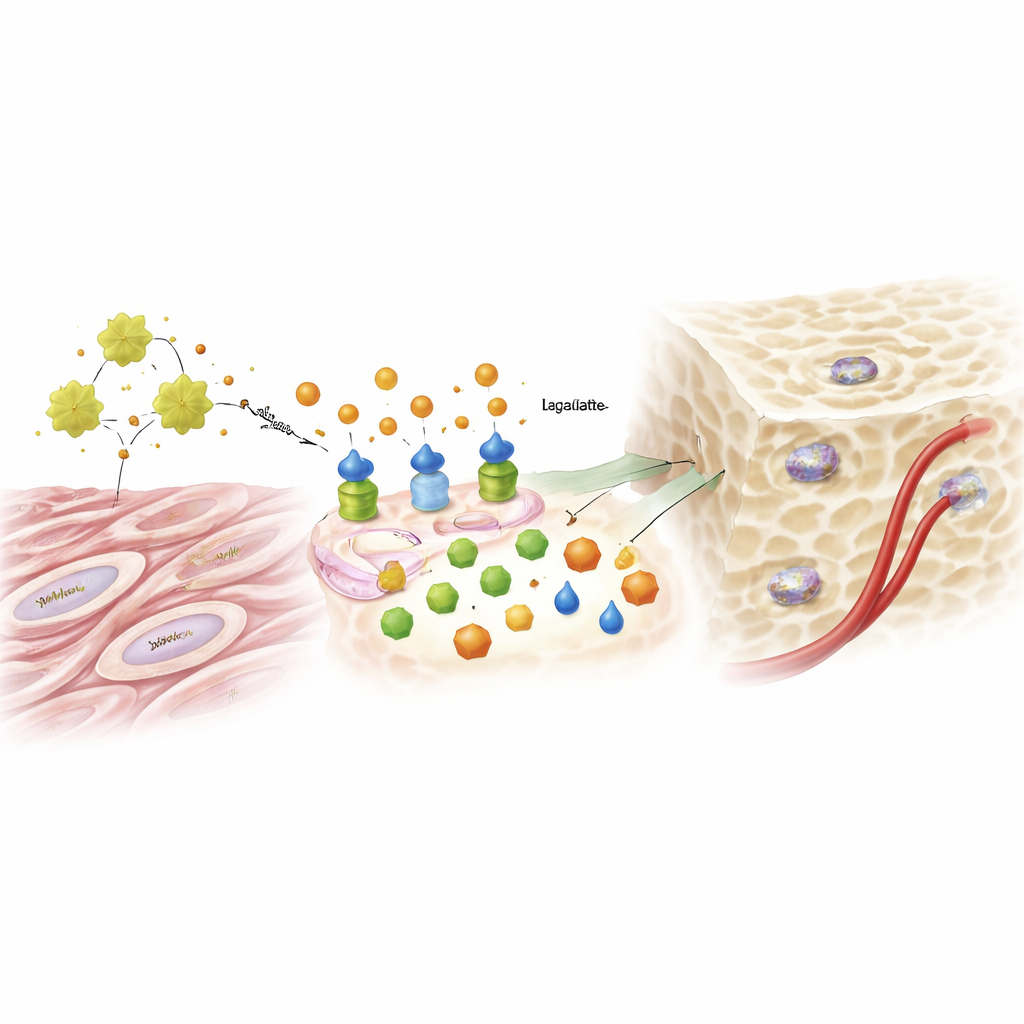
Vom Zucker-Nebenprodukt zum genetischen Signal
Laktat, lange als bloßer Stoffwechselabfall abgetan, spielte eine überraschend zentrale Rolle. Als die Glykolyse unter dem Einfluss von ADAM12 und IGF1 anstieg, stiegen die Laktatspiegel und begannen, die Art und Weise zu beeinflussen, wie die DNA im Zellkern verpackt ist. Die Forschenden fanden, dass Laktat bestimmte Histone — die Proteine, die die DNA organisieren — mit einer chemischen Markierung namens Laktylierung versieht. Diese Markierung lockerte DNA-Regionen, die mit knochenbildenden Genen verknüpft sind, und half so, Schlüsselfaktoren zu aktivieren, die eine Zelle in Richtung Osteoblast treiben. Extra zugeführtes Laktat konnte die knochenbildende Fähigkeit in Zellen wiederherstellen, bei denen ADAM12 herunterreguliert worden war, während das Blockieren der Glykolyse oder des Enzyms, das Laktat produziert, den Effekt von zusätzlichem ADAM12 aufhob. Derselbe ADAM12-getriebene Weg verstärkte zudem Signale, die das Wachstum von Blutgefäßen fördern und so die Versorgung des neuen Knochengewebes unterstützen.
Neue Wege zu nicht-chirurgischen Behandlungen
In der Gesamtschau zeichnet die Studie eine klare Abfolge: Ein Anstieg des Enzyms ADAM12 in Wirbelsäulenbändern setzt zusätzliches IGF1 frei, das ein Wachstumsprogramm einschaltet und die zelluläre Zuckerverwaltung umprogrammiert. Dieser Zuckerrausch erzeugt Laktat, das wiederum die Aktivität knochenbezogener Gene umschreibt und sowohl Knochen als auch Blutgefäße an Orten aufbaut, wo sie nicht hingehören. Durch das Blockieren der IGF1-Signalgebung oder der Glykolyse konnten die Forschenden diesen Prozess in Zellkulturen und Mäusemodellen dämpfen oder umkehren. Für Patientinnen und Patienten deutet diese Arbeit darauf hin, dass das Anvisieren der ADAM12–IGF1–Glykolyse-Achse eines Tages eine medikamentöse Möglichkeit bieten könnte, OPLL zu verlangsamen oder zu verhindern, den Bedarf an risikoreichen Wirbelsäulenoperationen zu senken und Mobilität sowie Nervfunktion zu erhalten.
Zitation: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Schlüsselwörter: Verknöcherung der Wirbelsäulenbänder, Zellstoffwechsel, Glykolyse, Wachstumsfaktor-Signalgebung, Knochenbildung