Clear Sky Science · pl
Reprogramowanie glikolityczne pośredniczone przez oś ADAM12/IGF1 sprzyja kostnieniu tylnego więzadła podłużnego
Kiedy oporowy pas w kręgosłupie zamienia się w kość
Głęboko w kręgosłupie twardy pas tkanki zwany tylnym więzadłem podłużnym pomaga utrzymać wyrównanie kręgów. U niektórych osób, szczególnie we wschodniej Azji, ten elastyczny pas stopniowo zamienia się w kość, uciskając rdzeń kręgowy i powodując ból, osłabienie, a nawet porażenie. Schorzenie to, znane jako OPLL, zazwyczaj wymaga ryzykownej operacji i obecnie nie ma leczenia farmakologicznego. Opisane tu badanie stawia proste, ale istotne pytanie: co jeśli sposób, w jaki te komórki wykorzystują cukier, jest ukrytym motorem napędzającym to niechciane tworzenie kości?
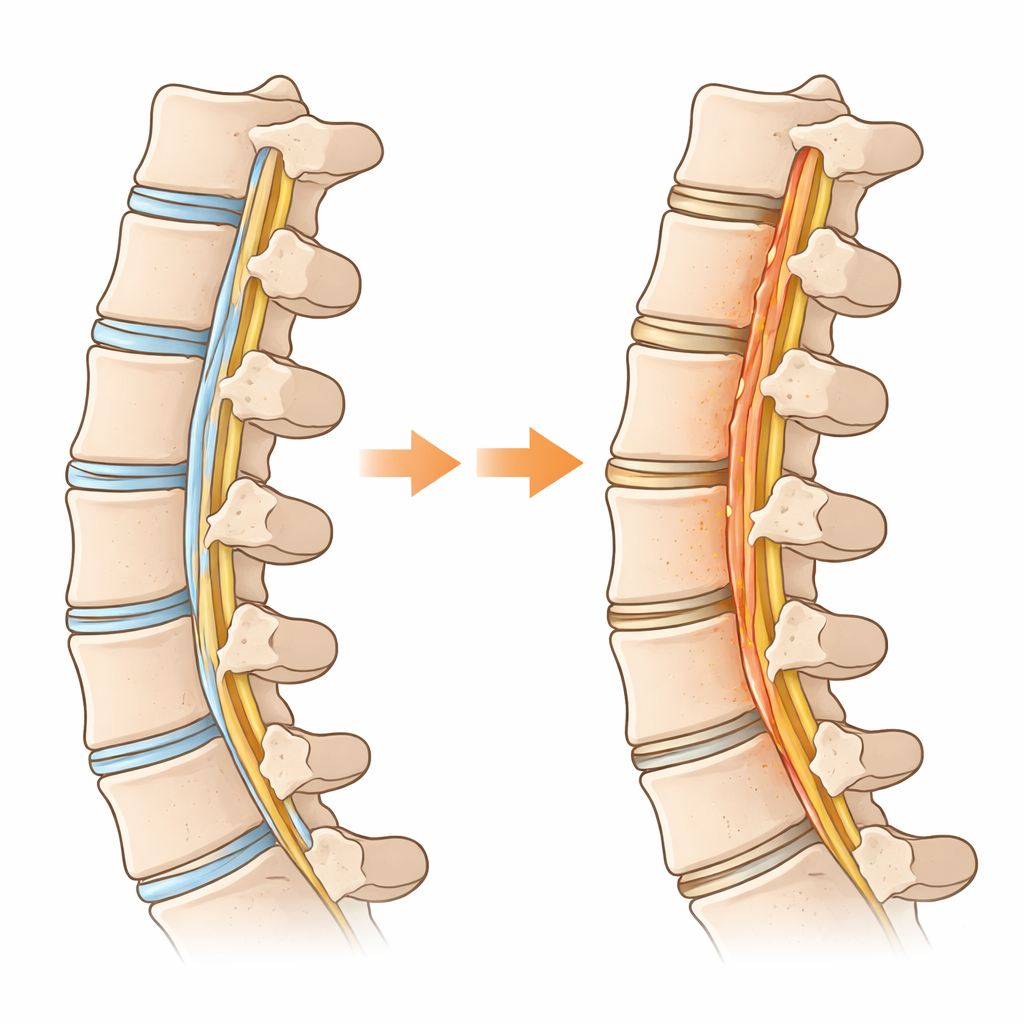
Dlaczego więzadło kręgosłupa zaczyna zachowywać się jak kość
Naukowcy porównali chore tkanki więzadła od osób z OPLL z prawidłowymi więzadłami pobranymi od pacjentów z innymi schorzeniami szyi. Wykorzystując analizy na dużą skalę ekspresji genów oraz analizy pojedynczych komórek, zmapowali, jakie typy komórek występują i czym każda z nich się zajmuje. Odkryli, że podzbiór komórek więzadła, które normalnie pełnią rolę „progenitorów” gotowych do naprawy, podążał ścieżką w kierunku stania się komórkami tworzącymi kość. Wzdłuż tej drogi komórki zmieniły strategię energetyczną: zamiast głównie spalać paliwo w mitochondriach, przestawiły się na szybkie rozkładanie cukrów — typ metabolizmu często obserwowany w nowotworach i rozwijających się tkankach. Ta zmiana w kierunku intensywnego wykorzystania glukozy — zwana glikolizą — była szczególnie silna w komórkach, które faktycznie tworzyły kość wewnątrz więzadła.
Spalanie cukru jako paliwo dla zbuntowanego tworzenia kości
Aby sprawdzić, czy ta zmiana metaboliczna jest jedynie towarzyszem czy też napędem choroby, zespół wyizolował komórki więzadła od pacjentów i obserwował je, gdy w laboratorium pobudzano je do różnicowania w kierunku komórek kostotwórczych. Komórki od pacjentów z OPLL pobierały więcej glukozy, produkowały więcej kwaśnych produktów ubocznych, takich jak mleczan, i wykazywały słabszą aktywność mitochondrialną niż komórki prawidłowe. Gdy naukowcy zablokowali glikolizę lekiem 2-DG, zdolność tych komórek do przekształcania się w osteoblasty gwałtownie spadła, a odkładane przez nie złogi mineralne były znacznie ograniczone. U myszy ten sam lek zmniejszył sztucznie wywołane masy kostne i obniżył liczbę komórek kostnych we wczesnym i dojrzałym stadium, co pokazuje, że odcięcie tej ścieżki spalania cukru może spowolnić lub złagodzić proces kostnienia u żywych zwierząt.
Ukryty przełącznik: reakcja łańcuchowa ADAM12–IGF1
Zagłębiając się bardziej, badacze poszukiwali głównych przełączników, które mogłyby wprawiać komórki w ten stan wysokiej glikolizy. Jeden z czynników, ADAM12, wyróżnił się. Był silnie podwyższony w tkance OPLL i najbardziej aktywny w komórkach więzadła zmierzających w kierunku kostnienia. ADAM12 to enzym przecinający białka znajdujący się poza komórką, który tutaj wydaje się rozcinać białka nośnikowe wiążące sygnał wzrostowy IGF1. Poprzez przycinanie jednego z tych nośników, IGFBP5, ADAM12 uwalnia więcej IGF1, które może aktywować receptory na komórkach więzadła. To z kolei uruchamia dobrze znany wewnątrzkomórkowy szlak wzrostu (PI3K–AKT–mTOR), który zwiększa aparat do rozkładu glukozy i produkcji mleczanu. Gdy ADAM12 był zwiększany w komórkach, glikoliza i produkcja mleczanu wzrastały; gdy był wyciszany lub jego zdolność do cięcia była unieszkodliwiona, oba procesy malały.
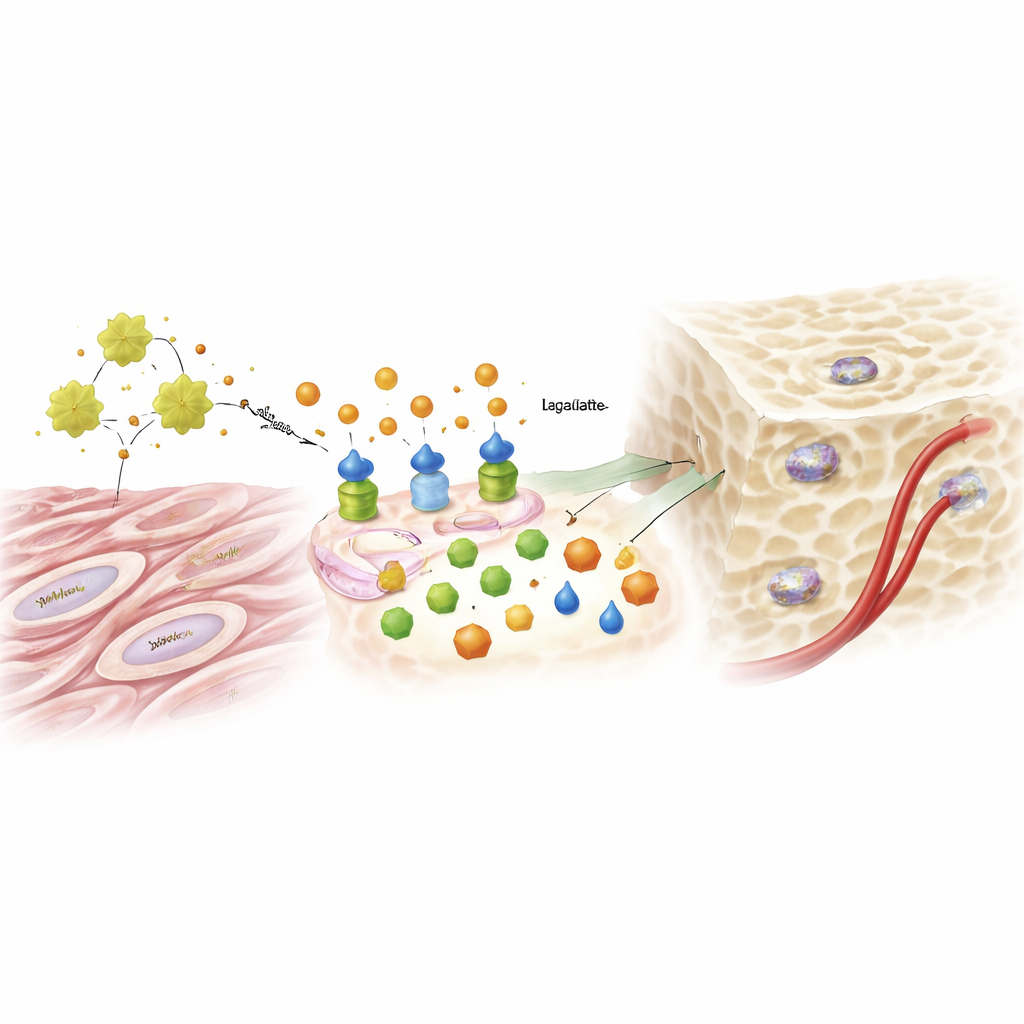
Od produktu ubocznego cukru do sygnału genetycznego
Mleczan, długo lekceważony jako odpad metaboliczny, odegrał zaskakująco istotną rolę. W miarę jak glikoliza nasilała się pod wpływem ADAM12 i IGF1, poziomy mleczanu rosły i zaczynały wpływać na sposób, w jaki DNA jest upakowane w jądrze komórkowym. Badacze odkryli, że mleczan ozdabia konkretne histony — białka organizujące DNA — chemiczną modyfikacją zwaną laktylacją. Ta modyfikacja rozluźniała rejony DNA powiązane z genami kostotwórczymi, pomagając włączyć kluczowe czynniki, które popychają komórkę do stania się osteoblastem. Dostarczenie dodatkowego mleczanu mogło przywrócić zdolność tworzenia kości w komórkach, gdzie ADAM12 było przytłumione, podczas gdy blokowanie glikolizy lub enzymu wytwarzającego mleczan usuwało efekt dodatkowego ADAM12. Ten sam szlak napędzany przez ADAM12 zwiększał też sygnały sprzyjające rozwojowi naczyń krwionośnych, dostarczając składników odżywczych do nowo powstającej tkanki kostnej.
Nowe drogi do leczenia niechirurgicznego
Podsumowując, badanie układa jasny łańcuch zdarzeń: wzrost enzymu ADAM12 w więzadłach kręgosłupa uwalnia dodatkowe IGF1, które uruchamia program wzrostowy przebudowujący sposób wykorzystania cukru przez komórki. Ta „burza cukrowa” wytwarza mleczan, który następnie przepisuje aktywność genów związanych z kością i pomaga budować zarówno kość, jak i naczynia krwionośne w miejscach, gdzie nie powinny powstawać. Poprzez blokowanie sygnalizacji IGF1 lub glikolizy, badacze byli w stanie osłabić lub odwrócić ten proces w hodowlach komórkowych i modelach mysich. Dla pacjentów praca ta sugeruje, że celowanie w oś ADAM12–IGF1–glikoliza mogłoby pewnego dnia zaoferować farmakologiczny sposób spowolnienia lub zapobiegania OPLL, zmniejszając potrzebę ryzykownych operacji kręgosłupa i zachowując sprawność oraz funkcje nerwowe.
Cytowanie: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Słowa kluczowe: kostnienie więzadła kręgosłupa, metabolizm komórkowy, glikoliza, sygnalizacja czynników wzrostu, tworzenie kości