Clear Sky Science · ar
إعادة برمجة التحلل السكري بواسطة محور ADAM12/IGF1 تعزز تكلس الرباط الطولي الخلفي
عندما يتحول شريط دعم في العمود الفقري إلى عظم
في عمق العمود الفقري، يوجد شريط نسيجي قوي يُسمى الرباط الطولي الخلفي يساعد في إبقاء فقراتنا مصطفة. عند بعض الأشخاص، لا سيما في شرق آسيا، يتحول هذا الحزام المرن تدريجياً إلى عظم، ما يضغط على الحبل الشوكي ويسبب ألماً وضعفاً أو حتى شللاً. تُعرف هذه الحالة باسم OPLL، وغالباً ما تتطلب جراحة محفوفة بالمخاطر ولا يوجد علاج دوائي حالي لها. تسأل الدراسة المُوجزة هنا سؤالاً بسيطاً لكنه قوي: ماذا لو كان أسلوب استخدام هذه الخلايا للسكر هو المحرك الخفي لهذا النمو العظمي غير المرغوب؟
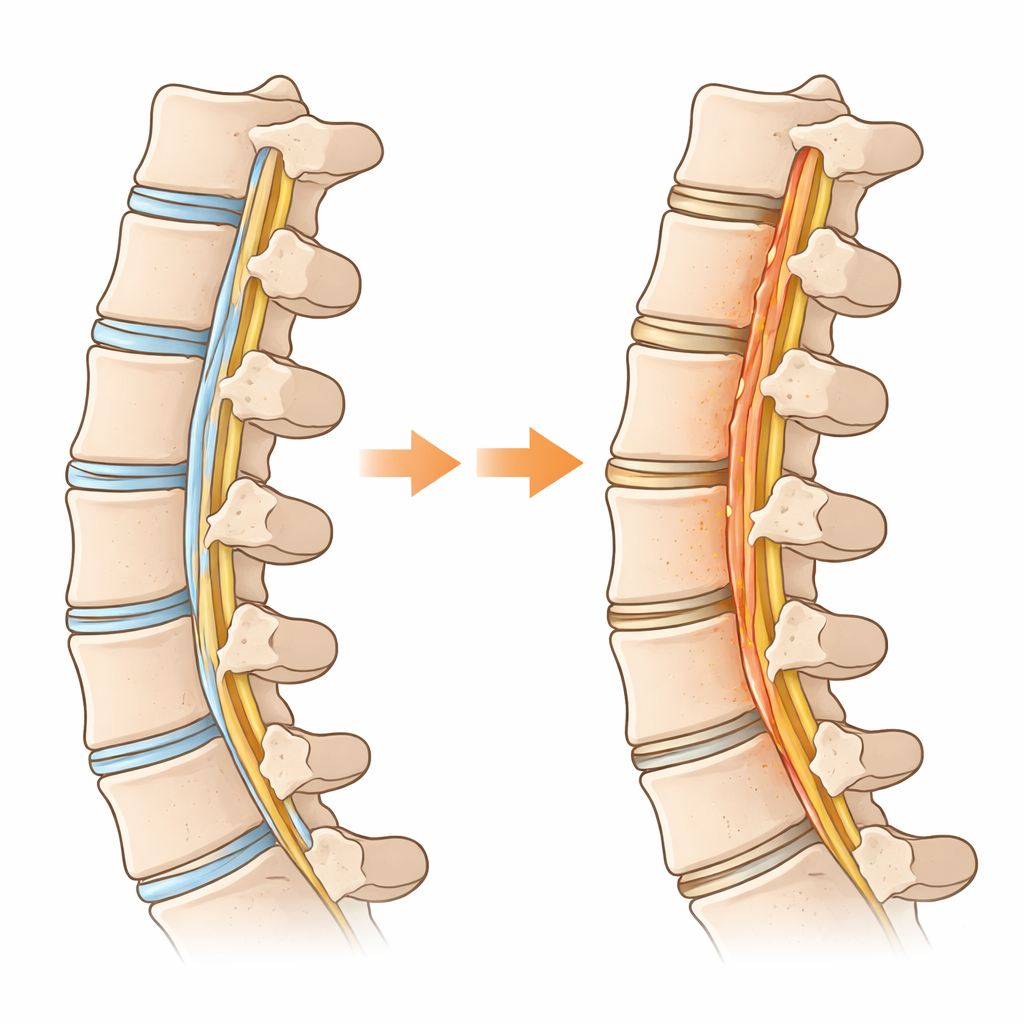
لماذا يبدأ الرباط الشوكي في التصرف مثل العظم
قارن الباحثون نسيج الرباط المريض من أشخاص مصابين بـ OPLL مع أربطة طبيعية من مرضى يعانون مشاكل عنق أخرى. باستخدام تحليلات جينية واسعة النطاق وتحليلات خلية مفردة، رسموا خريطة لأنواع الخلايا الحاضرة وما الذي تفعله كل خلية. وجدوا أن مجموعة فرعية من خلايا الرباط، التي تعمل عادةً كـ "خلايا سلفية" جاهزة للإصلاح، كانت تسلك مساراً نحو أن تصبح خلايا مُشكِّلة للعظم. على طول هذا المسار غيّرت الخلايا استراتيجيتها الطاقية: بدلاً من الاعتماد بشكل رئيسي على حرق الوقود في الميتوكوندريا، تحولت إلى تكسير سريع للسكر، وهو نمط أيضي يُرى كثيراً في السرطان والأنسجة النامية. كان هذا التحول إلى استخدام سكري عالي السرعة — المسمى التحلل السكري — قوياً بشكل خاص في الخلايا التي كانت فعلاً تُكوِّن عظاماً داخل الرباط.
حرق السكر كوقود للنمو العظمي الخارج عن المألوف
لاختبار ما إذا كان هذا التحول الأيضي مجرد مرافق أم محرك للمرض، عزَل الفريق خلايا الرباط من المرضى وراقبها أثناء دفعها لتتحول إلى خلايا مُشكِّلة للعظم في المختبر. امتصت خلايا مرضى OPLL المزيد من الغلوكوز، وأنتجت نواتج حمضية مثل اللاكتات بكميات أكبر، وأظهرت نشاطاً ميتوكوندرياً أضعف من الخلايا الطبيعية. عندما عطّل العلماء التحلل السكري بواسطة دواء يُدعى 2-DG، انخفضت قدرة الخلايا على التحول إلى خلايا مكوِّنة للعظم بشكل حاد، وتقلصت الترسبات المعدنية التي كانت تضعها عادةً. في الفئران، قلّص نفس الدواء الكتل العظمية المحفزة اصطناعياً وقلّل عدد الخلايا العظمية المبكرة والناضجة، مما يُظهر أن قطع هذا المسار الحارق للسكر يمكن أن يبطئ أو يلطّف عملية التكلس في الحيوانات الحية.
مفتاح مخفي: سلسلة التفاعل ADAM12–IGF1
بالتعمق أكثر، بحث الباحثون عن مفاتيح رئيسية قد تُحوِّل الخلايا إلى وضعية التحلل السكري العالي. برز جزيء واحد، ADAM12. كان مرتفعاً بقوة في نسيج OPLL وكان أكثر نشاطاً في خلايا الرباط التي تسير في طريق التحول إلى عظم. ADAM12 هو إنزيم يقطع البروتينات ويطفو خارج الخلايا، ويبدو هنا أنه يقطع بروتينات حاملة تحتجز إشارة نمو تسمى IGF1. عن طريق تقليم أحد هذه الحوامل، IGFBP5، يطلق ADAM12 المزيد من IGF1 ليُفعّل المستقبلات على خلايا الرباط. هذا بدوره يشغّل مسار نمو معروف داخل الخلية (PI3K–AKT–mTOR)، الذي يعزّز الآليات المسؤولة عن تكسير الغلوكوز وإنتاج اللاكتات. عندما زاد وجود ADAM12 في الخلايا، ارتفع التحلل السكري وإنتاج اللاكتات؛ وعندما تم إسكات ADAM12 أو تعطيل قدرته على القطع، انخفض كلاهما.
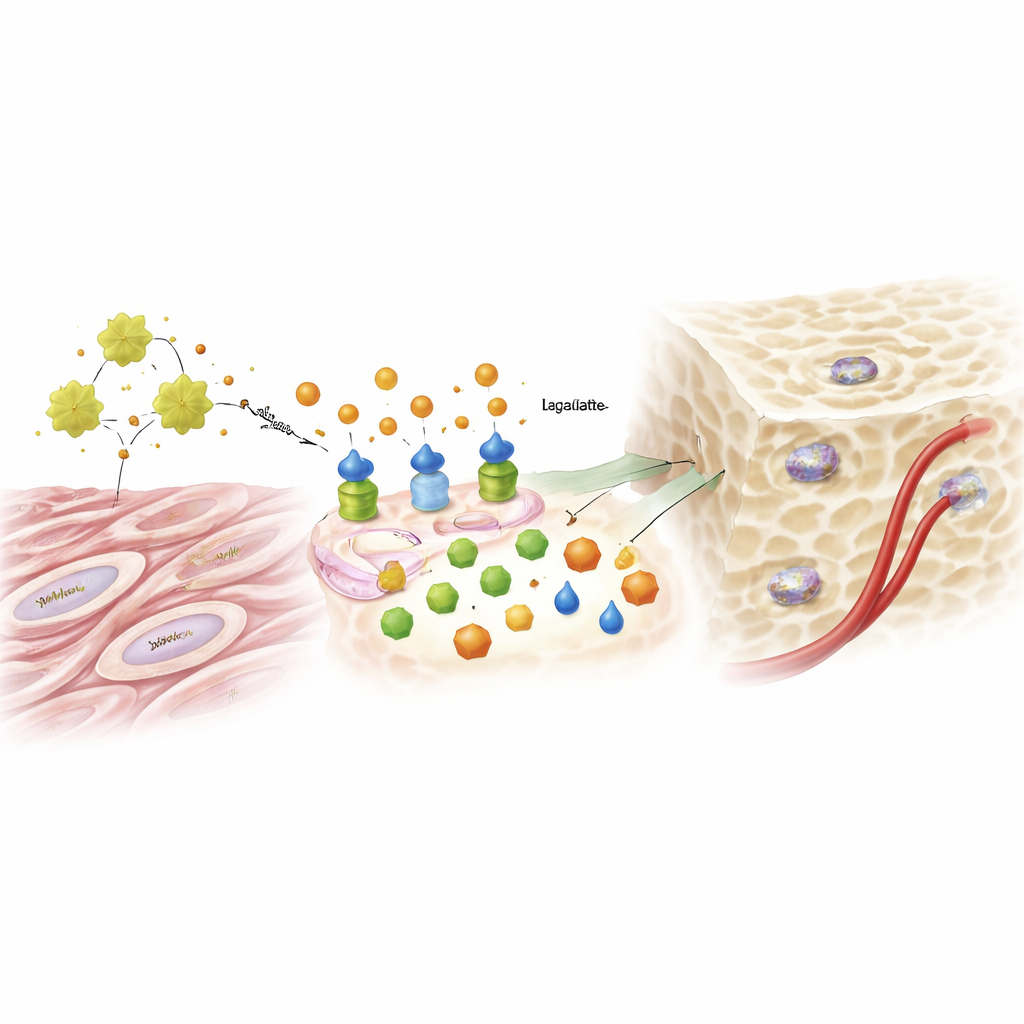
من ناتج سُكري إلى إشارة جينية
لعب اللاكتات، الذي طالما اعتُبر ناتجاً أيضياً مهدوراً، دوراً مفاجئاً ومحورياً. مع زيادة التحلل السكري تحت تأثير ADAM12 وIGF1، ارتفعت مستويات اللاكتات وبدأت تؤثر في طريقة تنظيم الحمض النووي داخل نواة الخلية. وجد الباحثون أن اللاكتات تُزيّن هستونات محددة — البروتينات التي تنظم الحمض النووي — بعلامة كيميائية تسمى اللاكتلة (lactylation). هذه العلامة أرخَت مناطق من الحمض النووي المرتبطة بجينات تكوين العظم، مما ساعد على تشغيل عوامل رئيسية تدفع الخلية لتصبح أُسْتيوبلَاست (خَلايا مُشكِّلة للعظم). إن توفير لاكتات إضافية استطاع استعادة القدرة على تكوين العظم في خلايا تم إسكات ADAM12 فيها، بينما أدى حجب التحلل السكري أو الإنزيم الذي يصنع اللاكتات إلى محو التأثير الناتج عن زيادة ADAM12. وزاد نفس المسار المدفوع بـ ADAM12 أيضاً إشارات تشجّع نمو الأوعية الدموية، مما يساعد في تزويد العظم الجديد بالمواد الغذائية.
مسارات جديدة نحو علاج غير جراحي
بالمجمل، ترسم الدراسة سلسلة واضحة من الأحداث: ارتفاع إنزيم ADAM12 في أربطة العمود الفقري يطلق المزيد من IGF1، الذي يشغّل برنامج نمو يُعيد توصيل استهلاك الخلايا للسكر. هذه الطفرة السكرية تنتج اللاكتات، التي تعيد كتابة نشاط الجينات المرتبطة بالعظم وتساعد في بناء كل من العظام والأوعية الدموية في أماكن لا يجب أن تتواجد فيها. من خلال حجب إشارة IGF1 أو التحلل السكري، استطاع الباحثون كبح هذا المسار أو عكسه في زراعات خلوية ونماذج فئران. بالنسبة للمرضى، تشير هذه النتائج إلى أن استهداف محور ADAM12–IGF1–التحلل السكري قد يوفر يوماً ما وسيلة دوائية لإبطاء أو منع OPLL، ما يقلل الحاجة إلى جراحات العمود الفقري عالية المخاطر ويحافظ على الحركة ووظيفة الأعصاب.
الاستشهاد: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
الكلمات المفتاحية: تكلس أربطة العمود الفقري, تمثيل الخلايا للطاقة, التحلل السكري, إشارة عوامل النمو, تكوين العظام