Clear Sky Science · fr
Le reprogrammation glycolytique médiée par l’axe ADAM12/IGF1 favorise l’ossification du ligament longitudinal postérieur
Quand une bande de soutien de la colonne vertébrale se transforme en os
Au cœur de la colonne vertébrale, une bande de tissu résistante appelée ligament longitudinal postérieur aide à maintenir l’alignement des vertèbres. Chez certaines personnes, en particulier en Asie de l’Est, cette sangle flexible se transforme progressivement en os, comprimant la moelle épinière et provoquant douleur, faiblesse, voire paralysie. Cette affection, connue sous le nom d’OPLL, nécessite généralement une chirurgie risquée et ne dispose actuellement d’aucun traitement médicamenteux. L’étude résumée ici pose une question simple mais puissante : et si la manière dont ces cellules utilisent le sucre était le moteur caché de cette croissance osseuse indésirable ?
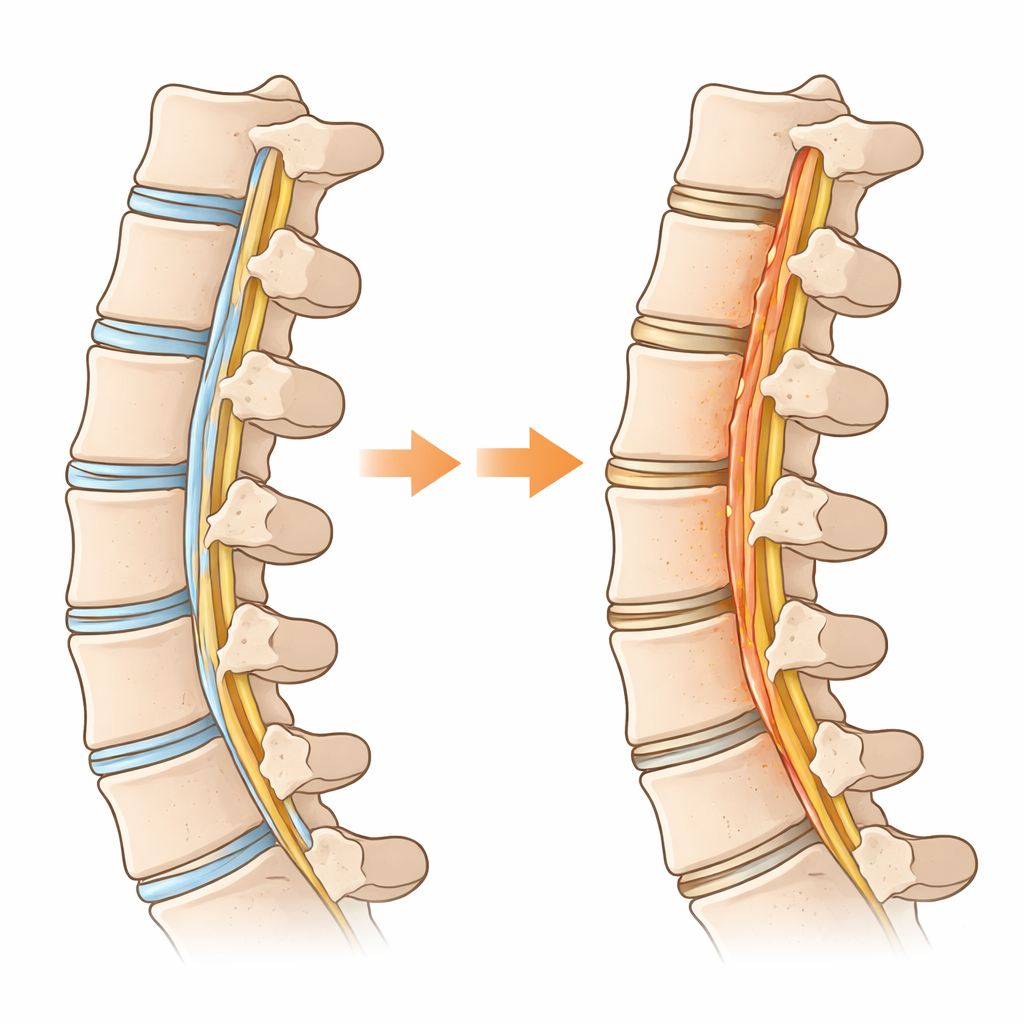
Pourquoi un ligament rachidien commence à se comporter comme de l’os
Les chercheurs ont comparé des tissus ligamentaires malades issus de personnes atteintes d’OPLL à des ligaments normaux prélevés chez des patients présentant d’autres problèmes cervicaux. Grâce à des analyses génomiques à grande échelle et à l’échelle d’une seule cellule, ils ont cartographié les types cellulaires présents et l’activité de chacune. Ils ont constaté qu’un sous-ensemble de cellules ligamentaires, qui servent normalement de « progéniteurs » prêts à réparer, empruntait une trajectoire vers des cellules formatrices d’os. Sur ce trajet, les cellules ont changé de stratégie énergétique : au lieu de principalement brûler du carburant dans leurs mitochondries, elles se sont orientées vers une décomposition rapide du sucre, un mode métabolique souvent observé dans le cancer et les tissus en croissance. Ce basculement vers une utilisation intensive du glucose — la glycolyse — était particulièrement marqué dans les cellules qui formaient effectivement de l’os à l’intérieur du ligament.
La combustion du sucre comme carburant de la croissance osseuse hors norme
Pour déterminer si ce changement métabolique n’était que corrélatif ou s’il conduisait la maladie, l’équipe a isolé des cellules ligamentaires de patients et les a observées lorsqu’on les poussait à devenir ostéoblastes en laboratoire. Les cellules provenant de patients OPLL absorbaient davantage de glucose, produisaient plus de sous-produits acidifiants comme le lactate, et présentaient une activité mitochondriale réduite par rapport aux cellules normales. Lorsque les scientifiques ont bloqué la glycolyse avec une molécule nommée 2-DG, la capacité des cellules à se différencier en ostéoblastes a chuté fortement, et les dépôts minéraux qu’elles formaient ont été fortement réduits. Chez la souris, le même médicament a réduit des masses osseuses artificiellement induites et diminué le nombre de cellules osseuses précoces et matures, montrant que couper cette voie de combustion du sucre peut ralentir ou atténuer le processus d’ossification in vivo.
Un interrupteur caché : la réaction en chaîne ADAM12–IGF1
En creusant plus avant, les chercheurs ont cherché des commutateurs maîtres susceptibles de basculer les cellules vers ce mode de haute glycolyse. Une molécule, ADAM12, s’est imposée. Elle était fortement augmentée dans les tissus OPLL et particulièrement active dans les cellules ligamentaires en cours de transformation en os. ADAM12 est une enzyme clivant des protéines qui se trouve à l’extérieur des cellules ; ici, elle semble couper des protéines porteuses qui retiennent un signal de croissance appelé IGF1. En taillant l’un de ces transporteurs, IGFBP5, ADAM12 libère davantage d’IGF1 pour activer les récepteurs des cellules ligamentaires. Cela déclenche ensuite une voie de croissance intracellulaire bien connue (PI3K–AKT–mTOR), qui renforce la machinerie de dégradation du glucose et de production de lactate. Lorsque ADAM12 était surexprimée dans les cellules, la glycolyse et la production de lactate augmentaient fortement ; lorsqu’elle était réduite ou que son activité protéolytique était désactivée, les deux diminuaient.
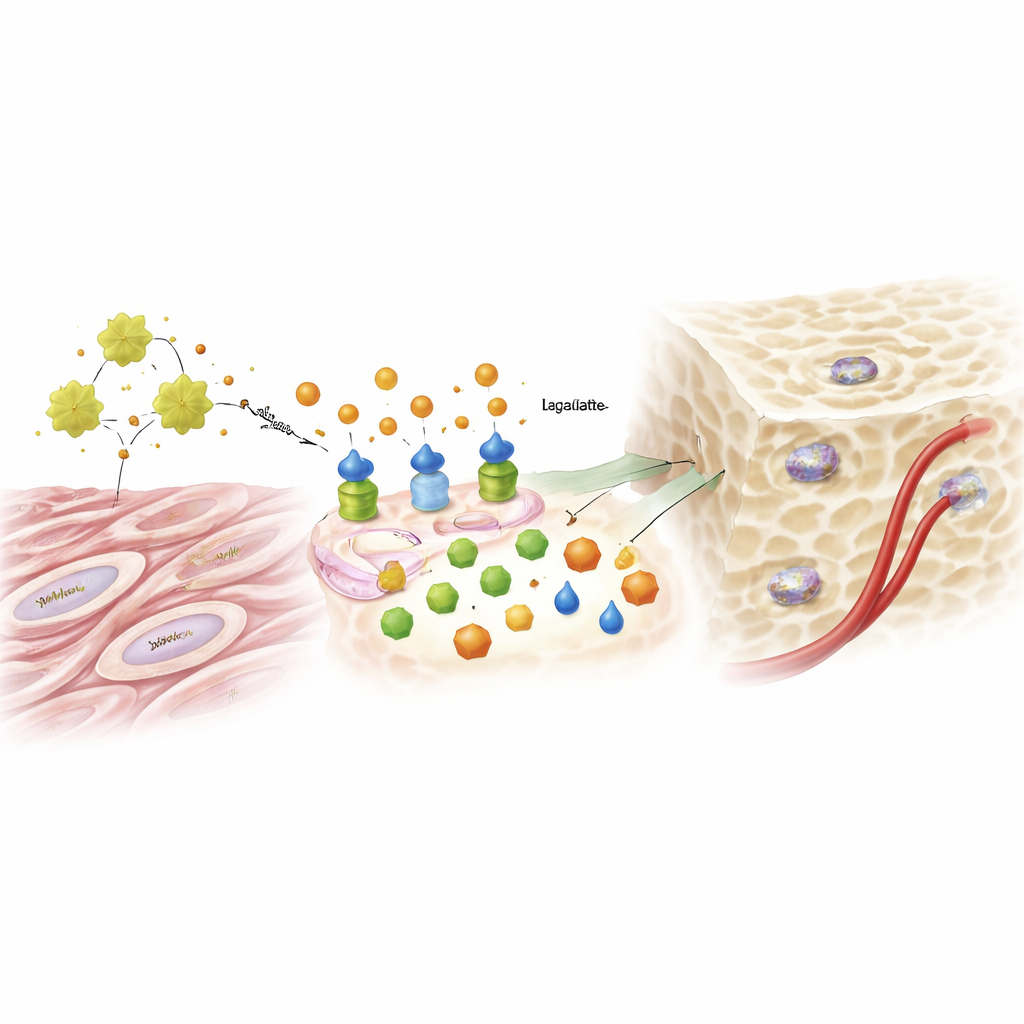
Du sous-produit sucré au signal génétique
Le lactate, longtemps considéré comme un déchet métabolique, a joué un rôle central et surprenant. À mesure que la glycolyse augmentait sous l’influence d’ADAM12 et d’IGF1, les niveaux de lactate montaient et commençaient à influencer la manière dont l’ADN est emballé dans le noyau cellulaire. Les chercheurs ont montré que le lactate ajoutait une marque chimique — la lactylation — sur des histones, les protéines qui organisent l’ADN. Cette marque assouplissait des régions d’ADN liées aux gènes ostéogéniques, contribuant à activer des facteurs clés qui poussent une cellule à devenir un ostéoblaste. Fournir du lactate supplémentaire pouvait restaurer la capacité de formation osseuse chez des cellules dont ADAM12 avait été réduit, tandis que bloquer la glycolyse ou l’enzyme qui produit le lactate annulait l’effet de l’augmentation d’ADAM12. La même voie activée par ADAM12 augmentait aussi des signaux favorisant la croissance des vaisseaux sanguins, aidant à alimenter en nutriments le nouvel os.
De nouvelles voies vers un traitement non chirurgical
Ensemble, ces résultats décrivent une chaîne d’événements claire : une augmentation de l’enzyme ADAM12 dans les ligaments spinaux libère plus d’IGF1, ce qui active un programme de croissance qui reprogramme l’utilisation du sucre par les cellules. Cette frénésie glycolytique produit du lactate, qui réécrit ensuite l’activité des gènes liés à l’os et favorise la formation d’os et de vaisseaux dans des zones où ils n’ont pas leur place. En bloquant la signalisation IGF1 ou la glycolyse, les chercheurs ont pu atténuer ou inverser ce processus dans des cultures cellulaires et des modèles murins. Pour les patients, ces travaux suggèrent que cibler l’axe ADAM12–IGF1–glycolyse pourrait un jour offrir une stratégie médicamenteuse pour ralentir ou prévenir l’OPLL, réduisant le besoin de chirurgies rachidiennes à haut risque et préservant mobilité et fonction nerveuse.
Citation: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Mots-clés: ossification des ligaments spinaux, métabolisme cellulaire, glycolyse, signalisation par facteurs de croissance, formation osseuse