Clear Sky Science · it
Riprogrammazione glicolitica mediata dall’asse ADAM12/IGF1 promuove l’ossificazione del legamento longitudinale posteriore
Quando una fascia di sostegno della colonna vertebrale si trasforma in osso
In profondità nella colonna, una robusta fascia di tessuto chiamata legamento longitudinale posteriore aiuta a mantenere allineate le vertebre. In alcune persone, soprattutto in Asia orientale, questa cinghia flessibile si trasforma gradualmente in osso, comprimendo il midollo spinale e causando dolore, debolezza o persino paralisi. Questa condizione, nota come OPLL, di solito richiede un intervento chirurgico rischioso e attualmente non ha terapia farmacologica. Lo studio qui riassunto pone una domanda semplice ma potente: se il modo in cui queste cellule utilizzano lo zucchero fosse il motore nascosto che guida questa crescita ossea indesiderata?
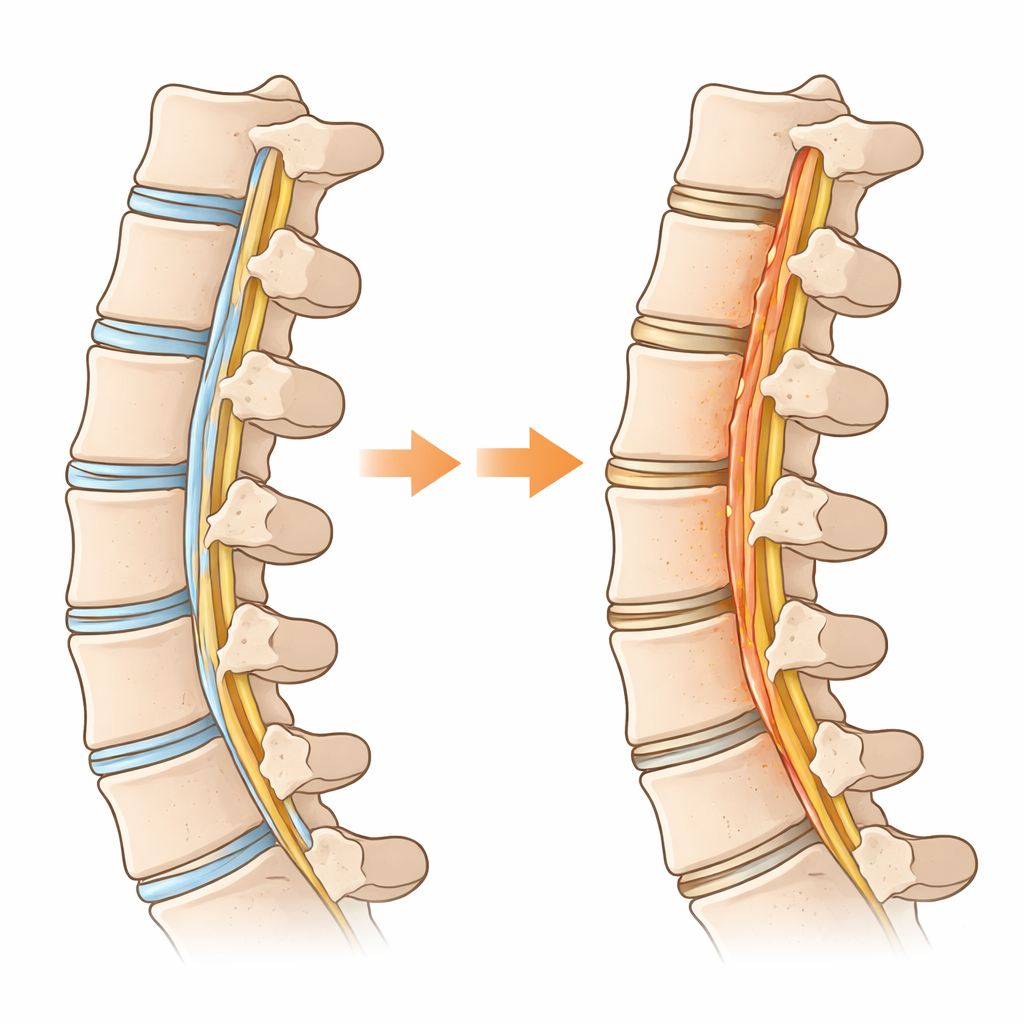
Perché un legamento spinale inizia a comportarsi come osso
I ricercatori hanno confrontato tessuto legamentoso malato di persone con OPLL con legamento normale di pazienti affetti da altri problemi cervicali. Usando analisi genomiche su larga scala e studi a singola cellula, hanno mappato quali tipi cellulari erano presenti e cosa faceva ciascuna cellula. Hanno scoperto che un sottoinsieme di cellule legamentose, che normalmente agiscono come «progenitrici» pronte alla riparazione, seguiva un percorso verso la trasformazione in cellule formatrici di osso. Lungo questo percorso le cellule hanno ribaltato la loro strategia energetica: invece di bruciare principalmente carburante nei mitocondri, si sono spostate verso una rapida degradazione degli zuccheri, uno stile metabolico spesso osservato nei tumori e nei tessuti in crescita. Questo passaggio verso un uso elevato di zucchero — chiamato glicolisi — era particolarmente marcato nelle cellule che stavano effettivamente formando osso all’interno del legamento.
La combustione dello zucchero come carburante per la crescita ossea fuorviante
Per verificare se questo spostamento metabolico fosse solo un fenomeno accessorio o un driver della malattia, il team ha isolato cellule del legamento da pazienti e le ha osservate mentre venivano indotte a diventare cellule osteogeniche in laboratorio. Le cellule dei pazienti con OPLL assorbivano più glucosio, producevano più sottoprodotti acidificanti come il lattato e mostravano un’attività mitocondriale più debole rispetto alle cellule normali. Quando gli scienziati hanno bloccato la glicolisi con un farmaco chiamato 2-DG, la capacità delle cellule di differenziarsi in osteoblasti è diminuita drasticamente e i depositi minerali che normalmente formavano si sono ridotti notevolmente. Nei topi, lo stesso farmaco ha ridotto masse ossee indotte artificialmente e ha diminuito il numero di cellule ossee in fase iniziale e matura, mostrando che interrompere questa via di combustione degli zuccheri può rallentare o attenuare il processo di ossificazione negli animali viventi.
Un interruttore nascosto: la reazione a catena ADAM12–IGF1
Approfondendo, i ricercatori hanno cercato interruttori principali che potessero spingere le cellule in questa modalità ad alta glicolisi. Una molecola, ADAM12, è emersa con evidenza. Era fortemente aumentata nei tessuti OPLL ed era più attiva nelle cellule legamentose in via di trasformazione verso l’osteogenesi. ADAM12 è un enzima che taglia proteine e si trova all’esterno delle cellule; qui sembra recidere proteine di trasporto che trattengono un segnale di crescita chiamato IGF1. Tagliando uno di questi carrier, IGFBP5, ADAM12 libera più IGF1 per attivare i recettori sulle cellule del legamento. Questo, a sua volta, innesca una nota via di crescita all’interno della cellula (PI3K–AKT–mTOR), che potenzia il macchinario per la degradazione del glucosio e la produzione di lattato. Quando ADAM12 era aumentata nelle cellule, glicolisi e produzione di lattato salivano; quando veniva silenziata o la sua attività di taglio disattivata, entrambe diminuivano.
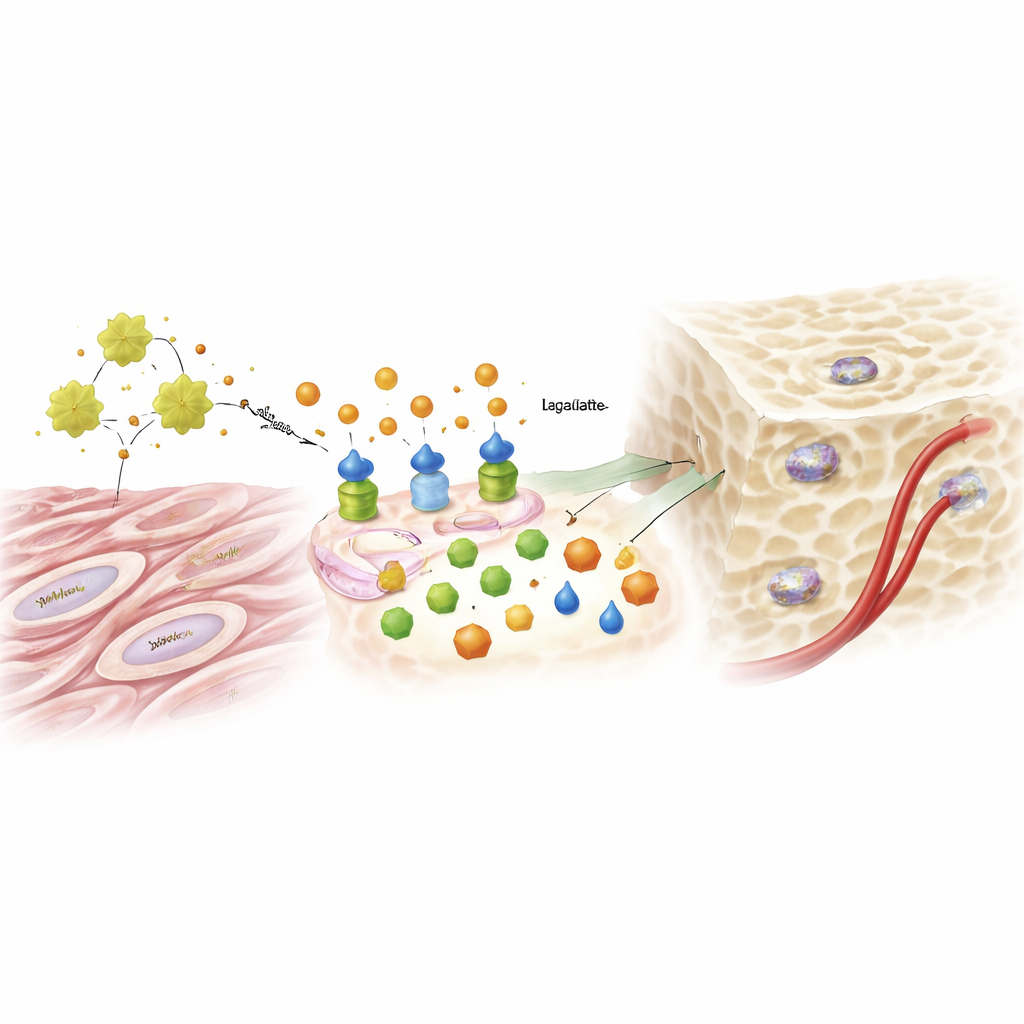
Dal sottoprodotto zuccherino al segnale genetico
Il lattato, a lungo considerato un rifiuto metabolico, ha avuto un ruolo sorprendente da protagonista. Con l’aumento della glicolisi sotto l’influenza di ADAM12 e IGF1, i livelli di lattato salivano e cominciavano a influenzare il modo in cui il DNA è impacchettato nel nucleo cellulare. I ricercatori hanno riscontrato che il lattato decorava specifici istoni — le proteine che organizzano il DNA — con un segno chimico chiamato lattilazione. Questo segno allentava regioni di DNA legate a geni osteogenici, favorendo l’attivazione di fattori chiave che spingono una cellula a diventare un osteoblasto. Fornire lattato supplementare poteva ripristinare la capacità osteogenica in cellule in cui ADAM12 era stato ridotto, mentre bloccare la glicolisi o l’enzima che produce lattato eliminava l’effetto positivo dell’aumento di ADAM12. La stessa via guidata da ADAM12 aumentava anche segnali che promuovono la formazione di vasi sanguigni, aiutando a fornire nutrienti al nuovo osso.
Nuove strade verso trattamenti non chirurgici
Nel complesso, lo studio delinea una catena di eventi: un aumento dell’enzima ADAM12 nei legamenti spinali libera IGF1 in eccesso, che accende un programma di crescita che riorienta l’uso dello zucchero nelle cellule. Questa ondata di zucchero produce lattato, che poi riscrive l’attività dei geni legati all’osso e contribuisce a costruire sia osso che vasi sanguigni in sedi dove non dovrebbero esserci. Bloccando la segnalazione IGF1 o la glicolisi, i ricercatori sono riusciti ad attenuare o invertire questo processo in colture cellulari e modelli murini. Per i pazienti, questo lavoro suggerisce che mirare all’asse ADAM12–IGF1–glicolisi potrebbe un giorno offrire una via farmacologica per rallentare o prevenire l’OPLL, riducendo la necessità di interventi chirurgici spinali ad alto rischio e preservando mobilità e funzione nervosa.
Citazione: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Parole chiave: ossificazione dei legamenti spinali, metabolismo cellulare, glicolisi, segnalazione dei fattori di crescita, formazione ossea