Clear Sky Science · tr
ADAM12/IGF1 ekseni tarafından aracılık edilen glikolitik yeniden programlanma, posterior longitudinal ligamentin ossifikasyonunu teşvik eder
Omurgadaki Destek Bantı Kemikleştiğinde
Omurganın derinliklerinde, posterior longitudinal ligament adı verilen dayanıklı bir doku bandı omurlarımızın hizalanmasına yardımcı olur. Bazı insanlarda, özellikle Doğu Asya’da, bu esnek bant zamanla kemiğe dönüşür, omuriliğe baskı yapar ve ağrı, güçsüzlük veya hatta felce yol açabilir. OPLL olarak bilinen bu durum genellikle riskli cerrahi gerektirir ve şu anda bir ilaç tedavisi yoktur. Burada özetlenen çalışma basit ama güçlü bir soruyu ele alır: ya bu hücrelerin şekeri kullanma biçimi, istenmeyen bu kemikleşmeyi sürükleyen gizli motor ise?
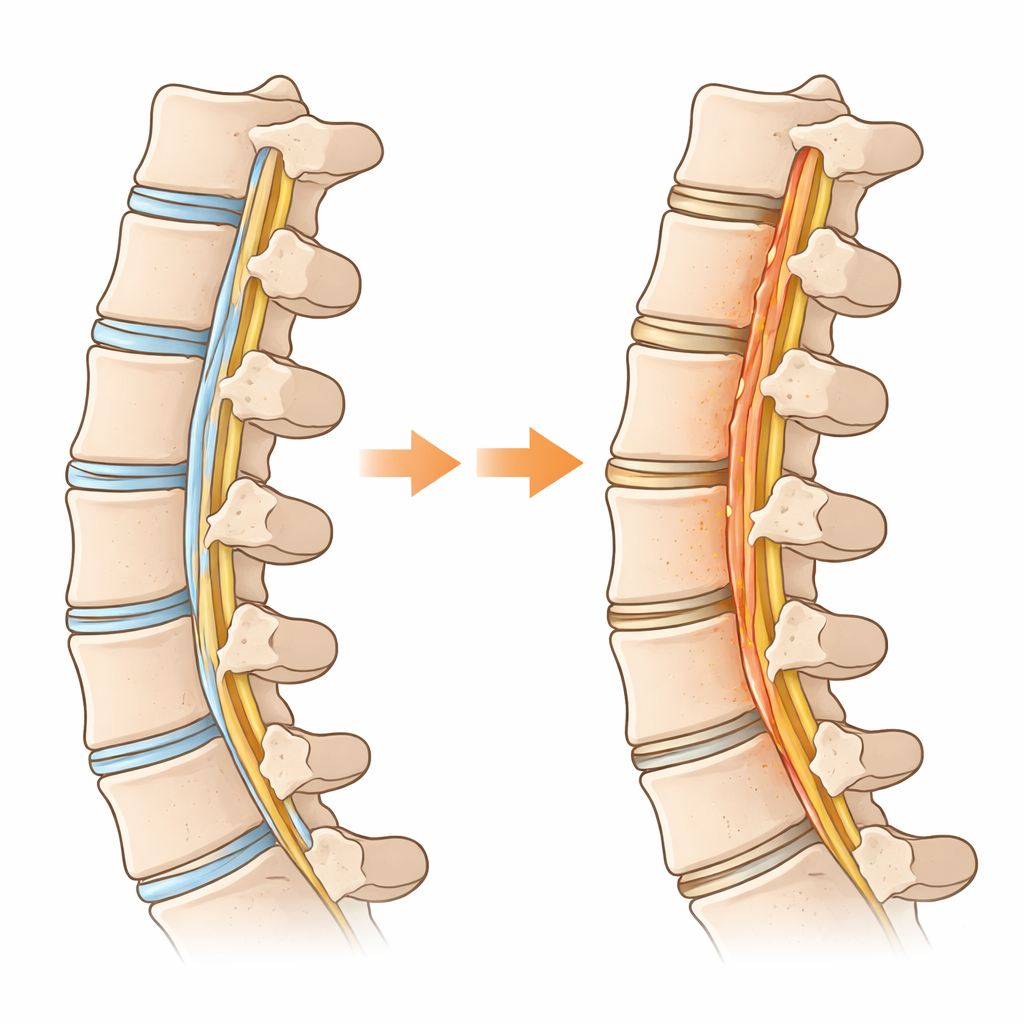
Bir Omurga Bağı Neden Kemik Gibi Davranmaya Başlar
Araştırmacılar OPLL’li kişilerden alınan hastalıklı ligament dokusunu, boyunla ilgili diğer sorunları olan hastalardaki normal ligamentle karşılaştırdı. Büyük ölçekli gen ve tek hücre analizleri kullanarak hangi hücre tiplerinin bulunduğunu ve her bir hücrenin ne yaptığını haritaladılar. Normalde onarıma hazır “progenitör” gibi davranan ligament hücrelerinin bir alt kümesinin kemik oluşturan hücrelere dönüşme yolunu izlediğini buldular. Bu yol boyunca hücreler enerji stratejilerini değiştirdi: esas olarak mitokondrilerinde yakıt yakmak yerine hızlı şeker yıkımına, kanser ve büyüyen dokularda sık görülen bir metabolizma tarzına kaydılar. Bu yüksek hızlı şeker kullanımı—glikoliz adı verilen değişim—özellikle ligament içinde gerçek anlamda kemik oluşturan hücrelerde belirgindi.
Kaçak Kemik Büyümesi İçin Yakıt Olarak Şeker Yakımı
Bu metabolik kaymanın sadece eşlik edeni mi yoksa hastalığın sürükleyicisi mi olduğunu test etmek için ekip, hastalardan ligament hücrelerini izole etti ve laboratuvarda osteoblastlara dönüşmeleri için yönlendirdi. OPLL hastalarından alınan hücreler daha fazla glukoz aldı, laktat gibi asit oluşturan yan ürünler daha fazla üretti ve normal hücrelere göre mitokondriyal aktiviteleri zayıftı. Bilim insanları 2-DG adlı bir ilaçla glikolizi engellediklerinde, hücrelerin kemik oluşturan hücrelere dönüşme yeteneği keskin biçimde düştü ve normalde bıraktıkları mineral birikimleri büyük ölçüde azaldı. Farelerde, aynı ilaç yapay olarak oluşturulmuş kemik kitlelerini küçülttü ve erken ile olgun kemik hücrelerinin sayısını azalttı; bu da bu şeker yakma yolunu kesmenin canlılarda ossifikasyon sürecini yavaşlatabileceğini ya da yumuşatabileceğini gösterdi.
Gizli Bir Anahtar: ADAM12–IGF1 Zincirleme Reaksiyonu
Daha derine indiklerinde, hücreleri bu yüksek glikoliz moduna geçiren anahtarları aradılar. ADAM12 adlı bir molekül öne çıktı. OPLL dokusunda belirgin biçimde yükselmişti ve kemikleşme yolundaki ligament hücrelerinde en aktif olanıydı. ADAM12, hücrelerin dışında yüzen ve proteinleri kesen bir enzimdir ve burada IGF1 adlı bir büyüme sinyalini tutan taşıyıcı proteinleri parçalayarak etki ediyor gibi görünmektedir. Bu taşıyıcılardan biri olan IGFBP5’i kestiğinde ADAM12, daha fazla IGF1’in ligament hücrelerindeki reseptörleri aktifleştirmesini serbest bırakıyor. Bu da hücre içinde iyi bilinen bir büyüme yolunu (PI3K–AKT–mTOR) tetikliyor ve glukozu parçalama ile laktat üretimini artıran mekanizmaları güçlendiriyor. ADAM12 hücrelerde arttırıldığında glikoliz ve laktat üretimi yükseldi; susturulduğunda veya kesme yeteneği devre dışı bırakıldığında her ikisi de düştü.
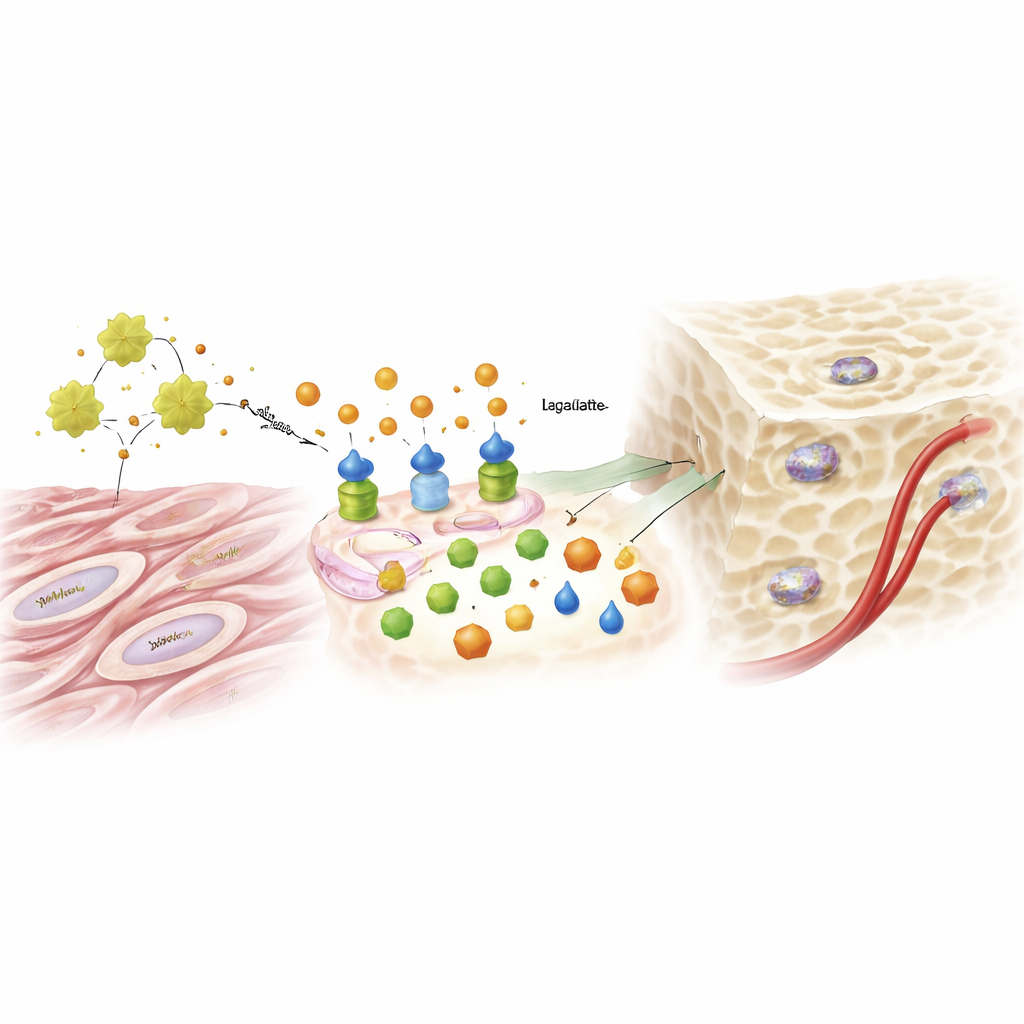
Şeker Yan Ürününden Genetik Sinyale
Uzun süre metabolik atık olarak önemsenen laktat, şaşırtıcı bir başrol oynadı. ADAM12 ve IGF1 etkisi altında glikoliz artarken laktat seviyeleri yükseldi ve hücre çekirdeğinde DNA’nın paketlenme biçimini etkilemeye başladı. Araştırmacılar, laktatın DNA’yı organize eden histonları belirli bir kimyasal işaretle—laktileasyon—süslediğini buldular. Bu işaret, kemik oluşumuyla ilişkili genlerin bulunduğu DNA bölgelerini gevşetti ve bir hücrenin osteoblasta dönüşmesini destekleyen anahtar faktörlerin açılmasına yardımcı oldu. Ek laktat sağlanması, ADAM12 susturulmuş hücrelerde kemik oluşturma yeteneğini geri kazandırabiliyordu; glikolizi veya laktatı yapan enzimi engellemek ise ekstra ADAM12’nin verdiği desteği ortadan kaldırdı. Aynı ADAM12 kaynaklı yol ayrıca kan damarlarının büyümesini teşvik eden sinyalleri artırdı ve yeni kemiğe besin sağlanmasına yardımcı oldu.
Cerrahi Olmayan Tedavilere Yeni Yollar
Bir arada değerlendirildiğinde çalışma açık bir olay zinciri çiziyor: omurga ligamentlerindeki ADAM12 enziminin yükselmesi ekstra IGF1’i serbest bırakıyor, bu da hücrelerin şekeri kullanma biçimini yeniden düzenleyen bir büyüme programını başlatıyor. Bu şeker patlaması laktat üretiyor; laktat ise kemikle ilişkili genlerin etkinliğini yeniden yazıyor ve kemik ile kan damarlarının olması gereken yerler dışında inşa edilmesine yardımcı oluyor. IGF1 sinyalini veya glikolizi engelleyerek araştırmacılar bu süreci hücre kültürlerinde ve fare modellerinde körleştirebildi ya da tersine çevirebildi. Hastalar için bu çalışma, ADAM12–IGF1–glikoliz eksenini hedeflemenin bir gün OPLL’yi yavaşlatan veya önleyen ilaç tabanlı bir yol sunabileceğini, yüksek riskli spinal cerrahi ihtiyacını azaltarak hareket kabiliyeti ve sinir fonksiyonunu koruyabileceğini düşündürür.
Atıf: Zhao, Q., Wu, H., Xie, D. et al. Glycolytic reprogramming mediated by the ADAM12/IGF1 axis promotes ossification of the posterior longitudinal ligament. Cell Death Discov. 12, 178 (2026). https://doi.org/10.1038/s41420-026-03044-8
Anahtar kelimeler: omurga bağ dokusu ossifikasyonu, hücre metabolizması, glikoliz, büyüme faktörü sinyalleşmesi, kemik oluşumu