Clear Sky Science · zh
亚致死性DNA损伤关闭RA-FLS-PBMC共培养体系中的B细胞效应程序
抑制过度活跃的免疫反应
类风湿性关节炎部分由攻击自身关节的免疫细胞驱动,导致疼痛、肿胀和长期损伤。许多现有药物通过清除整类免疫细胞来发挥作用,这会使患者更易感染。该研究探讨了一个更为细致的思路:是否可以用一剂极小、受控的DNA损伤短暂关闭某些有害免疫细胞(尤其是B细胞)的活性——而不至于杀死大多数细胞。如果可行,这一方法可能指向更温和的治疗策略,在保持免疫系统大部分功能的同时平抑疾病。
为什么B细胞是特别的脆弱点
B细胞以产生抗体著称,但在类风湿性关节炎中,它们也维持炎症并在关节内组织免疫“热点”。为精细调整其产生的抗体,活化的B细胞会有意切割并重新连接自身的DNA。这种不寻常的行为使它们比许多其他细胞对额外损伤更为敏感。研究者推测,一次小幅的额外DNA“推力”,低于引起大规模细胞死亡的阈值,可能利用这一脆弱性选择性压制B细胞活性。同时,他们也希望避免广泛毒害免疫细胞或损伤构成关节衬里结构的细胞。
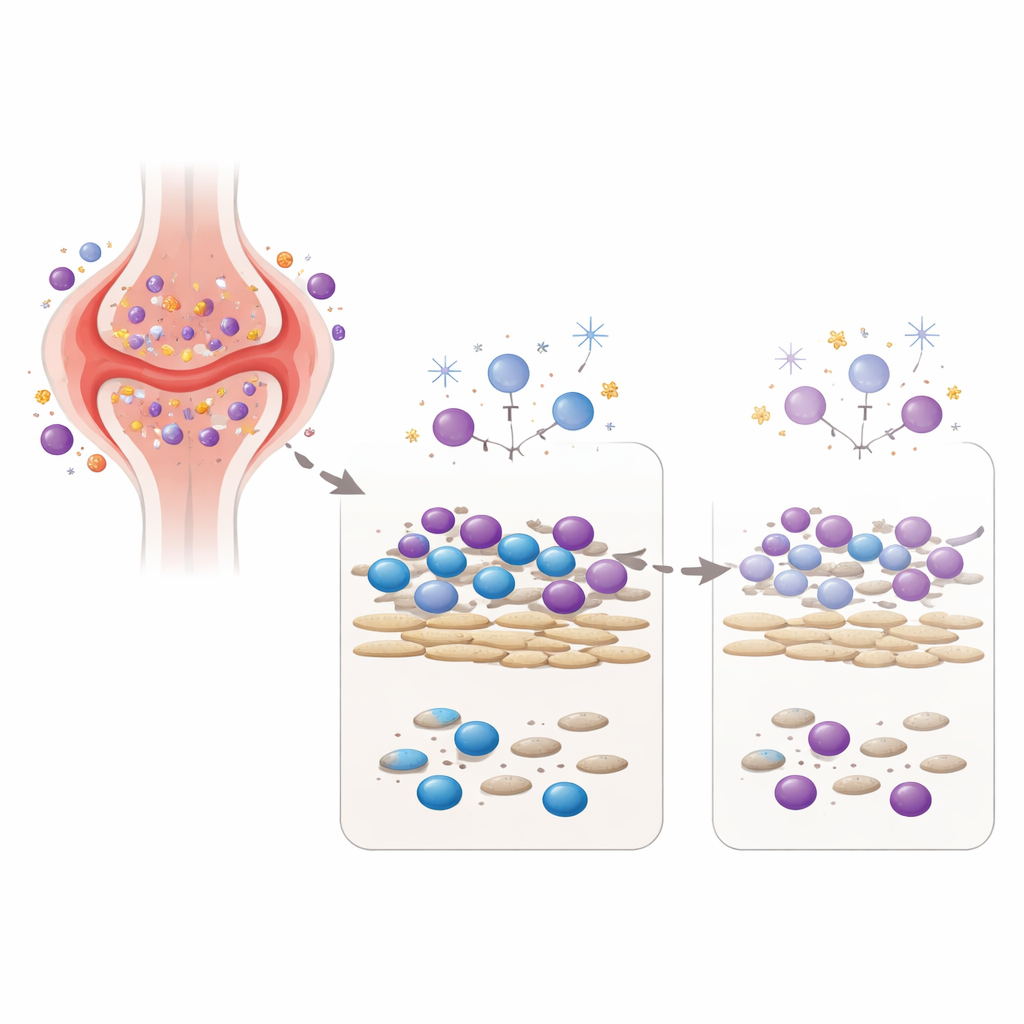
在体外重建关节的炎性环境
为验证这一概念,团队建立了一个实验室模型,将关节中的两个关键成分结合在一起:来自类风湿性关节炎患者的类成纤维样滑膜细胞(纤维母细胞样滑膜细胞)和来自健康志愿者的外周血免疫细胞。在这种共培养中,纤维母细胞提供维持免疫细胞存活与活化的信号,类似于发炎关节内的环境。随后,研究者对这一混合细胞群施加一次精心选择的低剂量三种不同DNA损伤源:低剂量伽马照射、过氧化氢(也存在于炎性组织中的活性氧)以及与环磷酰胺相关的药物代谢物(一种用于严重自身免疫病的化疗药物)。他们不仅测量了细胞的存活率,还在数天后评估细胞产生的抗体与细胞因子(免疫信使分子)的量。
关闭功能而非大量细胞丧失
在三种损伤源中出现了相似的规律:在仍保留大部分细胞存活的剂量下,B细胞功能显著下降。例如,在适度剂量的伽马照射后,总体细胞存活率仍高于80%,但诸如抗炎细胞因子IL-10和若干类抗体的水平下降了约一半或更多。过氧化氢和化疗代谢物在抑制抗体与细胞因子产生方面显示出相似甚至更强的效果,有时在仍有超过三分之二细胞存活的情况下发生。换言之,基因毒性“冲击”将免疫活性与细胞存活解耦——细胞仍在,但它们驱动炎症的能力被显著降低。
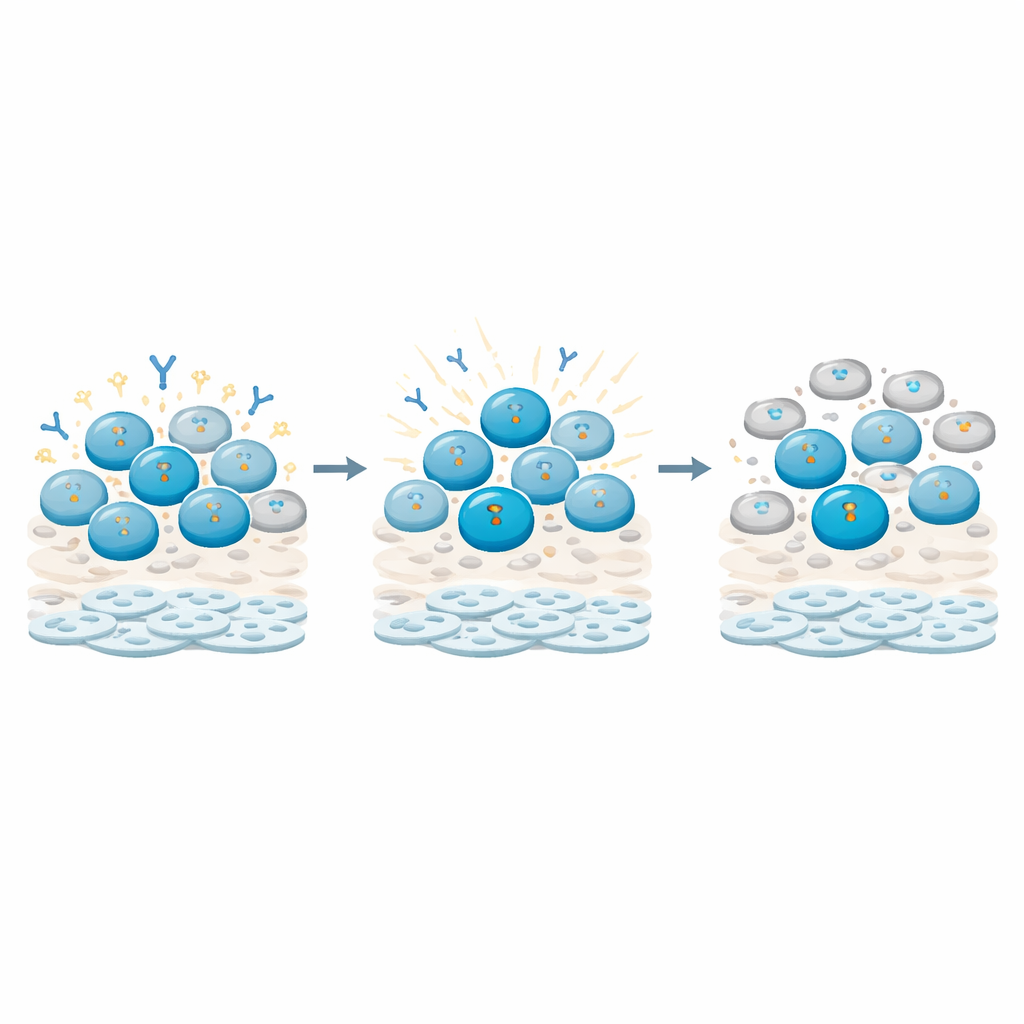
B细胞如何感知损伤并踩刹车
深入分析时,研究者追踪了不同免疫细胞类型内DNA损伤的分子标志。他们发现,尤其是记忆B细胞(由既往暴露被激活的那类),相比T细胞积累了更强且更持久的DNA损伤信号。这些信号触发了检查点,使B细胞的细胞周期停滞,让它们停留在静止期而非活跃分裂与分化。同时,与抗体产生和B细胞成熟相关的基因活性发生重塑:一些主控调节因子和抗体链转录本呈现上调或下调的模式,暗示这些细胞被置于“先修复、后功能”的状态。相比之下,T细胞表现出更短暂的反应并在很大程度上恢复了增殖行为。
对更温和自身免疫疗法的新思路
总体而言,该研究表明一次低水平的DNA损伤冲击可以在类关节炎环境中选择性地安静B细胞程序,同时保留大多数T细胞和关节衬里细胞。与其彻底清除B细胞,这种方法更像是将其推入检查点状态,使它们停止释放炎性分子和抗体。对患者而言,这一想法仍处于理论阶段,但它提示经过精确调控的短暂辐射或基因毒性药物暴露未来或可用于不通过直接杀灭细胞而暂时沉默最麻烦的细胞。这类策略可作为现有治疗的补充,原则上有望以更少的免疫系统附带损害来驯服慢性自身免疫性炎症。
引用: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
关键词: 类风湿性关节炎, B细胞, DNA损伤, 免疫调节, 自身免疫性疾病