Clear Sky Science · fr
Des lésions d’ADN sous-létales coupent les programmes effecteurs des cellules B dans une co-culture RA-FLS-PBMC
Calmer une réponse immunitaire trop active
La polyarthrite rhumatoïde est en partie causée par des cellules du système immunitaire qui attaquent les articulations du corps, provoquant douleur, gonflement et dommages à long terme. De nombreux médicaments actuels agissent en éliminant des groupes entiers de cellules immunitaires, ce qui peut rendre les patients vulnérables aux infections. Cette étude explore une idée plus subtile : une toute petite dose contrôlée de lésions d’ADN pourrait temporairement désactiver l’activité nocive de certaines cellules immunitaires — en particulier les cellules B — sans tuer la plupart d’entre elles. Si cela fonctionne, cette approche pourrait ouvrir la voie à des traitements plus doux qui calment la maladie tout en préservant une grande partie du système immunitaire.
Pourquoi les cellules B constituent une faiblesse particulière
Les cellules B sont surtout connues pour produire des anticorps, mais dans la polyarthrite rhumatoïde elles contribuent aussi à maintenir l’inflammation et à organiser des « foyers » immunitaires au sein de l’articulation. Pour affiner les anticorps qu’elles produisent, les cellules B activées coupent et recousent délibérément leur propre ADN. Ce comportement inhabituel les rend plus sensibles à des dommages supplémentaires que beaucoup d’autres cellules. Les chercheurs ont émis l’hypothèse qu’un petit « coup de pouce » supplémentaire de lésions de l’ADN, en dessous du seuil provoquant une mort cellulaire massive, pourrait exploiter cette vulnérabilité et réduire sélectivement l’activité des cellules B. Dans le même temps, ils voulaient éviter d’empoisonner largement les cellules immunitaires ou d’endommager les cellules structurelles qui forment la membrane synoviale.
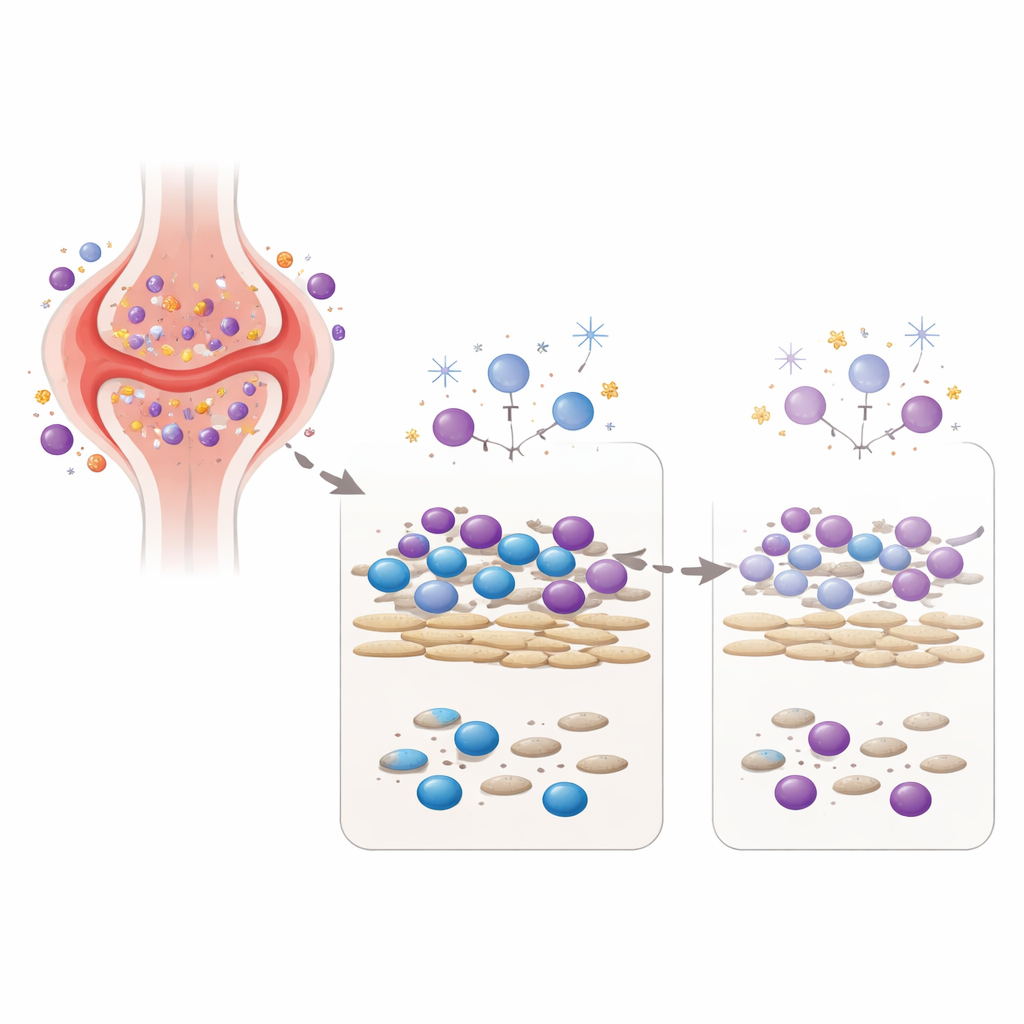
Recréer l’articulation arthritique en éprouvette
Pour tester ce concept, l’équipe a mis en place un modèle de laboratoire réunissant deux acteurs clés de l’articulation : des synoviocytes de type fibroblaste, des cellules du tissu conjonctif issues de patients atteints de polyarthrite rhumatoïde, et des cellules immunitaires sanguines provenant de donneurs sains. Dans cette co-culture, les fibroblastes fournissent des signaux qui maintiennent les cellules immunitaires en vie et actives, un peu comme l’environnement à l’intérieur d’une articulation enflammée. Les chercheurs ont ensuite exposé cette communauté cellulaire mixte à une seule dose soigneusement choisie de trois agents délétères pour l’ADN : une irradiation gamma à faible dose, du peroxyde d’hydrogène (une espèce réactive de l’oxygène également présente dans les tissus enflammés), et un métabolite médicamenteux lié à la cyclophosphamide, une chimiothérapie utilisée dans les formes sévères de maladies auto-immunes. Ils ont mesuré non seulement la survie cellulaire, mais aussi la quantité d’anticorps et de cytokines — ces molécules messagères du système immunitaire — produites par les cellules plusieurs jours plus tard.
Couper la fonction sans perte cellulaire massive
Avec les trois agents, un schéma net est apparu : les fonctions des cellules B étaient fortement réduites à des doses qui laissaient encore la plupart des cellules vivantes. Par exemple, après une dose modeste d’irradiation gamma, la survie cellulaire globale restait supérieure à 80 %, et pourtant des signaux clés comme la cytokine anti-inflammatoire IL-10 et plusieurs classes d’anticorps chutaient d’environ la moitié ou plus. Le peroxyde d’hydrogène et le métabolite de chimiothérapie montraient une atténuation similaire voire plus marquée de la production d’anticorps et de cytokines, parfois alors que plus des deux tiers des cellules étaient encore viables. Autrement dit, le « coup » génotoxique a dissocié l’activité immunitaire de la survie cellulaire : les cellules étaient présentes, mais leur capacité à alimenter l’inflammation était nettement réduite.
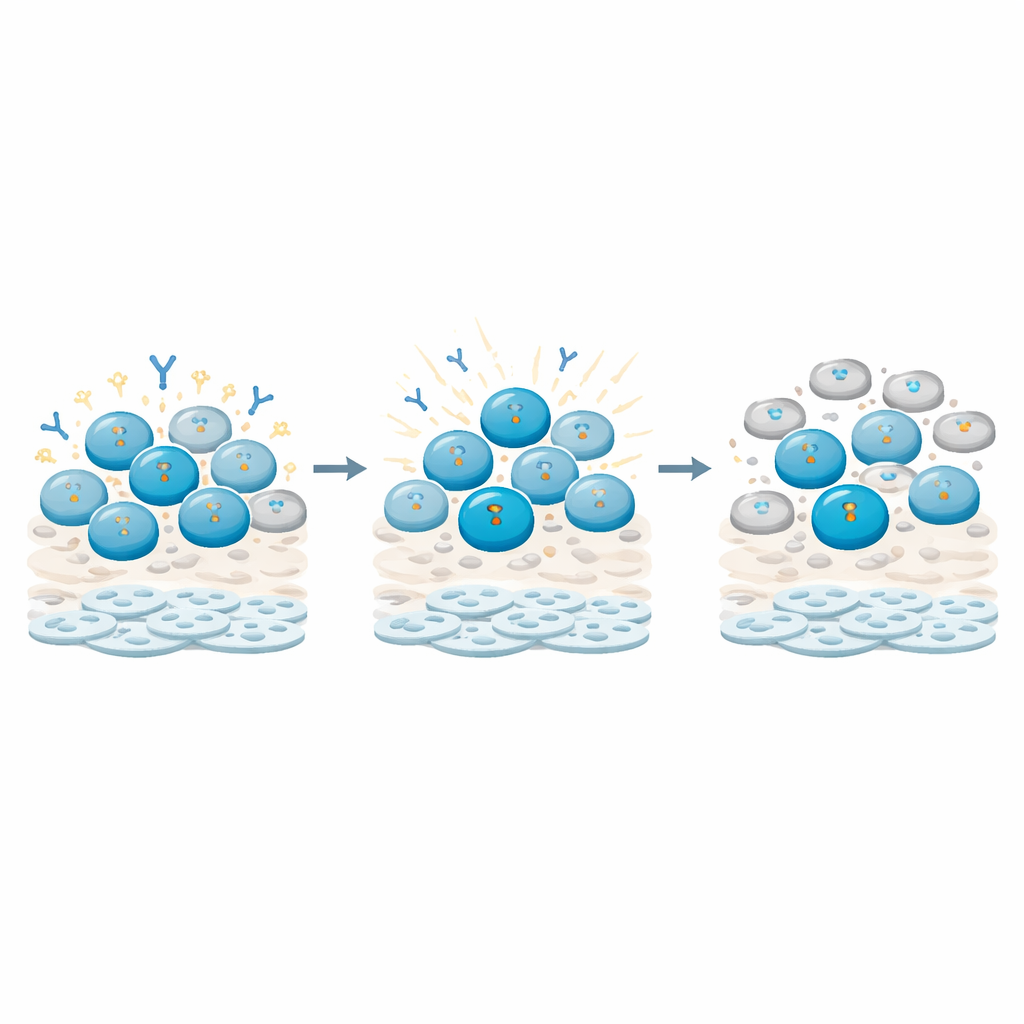
Comment les cellules B détectent les dommages et freinent leur activité
En approfondissant, les investigateurs ont suivi des signes moléculaires de dommages à l’ADN dans différents types de cellules immunitaires. Ils ont constaté que les cellules B, en particulier les cellules B mémoire (celles primées par des rencontres antérieures), accumulaient des signaux de lésions d’ADN particulièrement forts et durables par rapport aux cellules T. Ces signaux alimentaient des points de contrôle qui arrêtaient le cycle cellulaire des cellules B, les maintenant dans une phase quiescente plutôt que de se diviser et de se différencier activement. Parallèlement, l’activité génique liée à la production d’anticorps et à la maturation des cellules B était remodelée : certains régulateurs maîtres et des transcrits de chaînes d’anticorps augmentaient ou diminuaient selon des schémas suggérant que les cellules étaient maintenues dans un état « réparer d’abord, fonctionner plus tard ». Les cellules T, en revanche, présentaient des réponses plus transitoires et retrouvaient en grande partie leur cycle.
Une nouvelle approche pour des thérapies auto-immunes plus douces
Globalement, l’étude montre qu’une unique poussée de lésions d’ADN à faible intensité peut calmer sélectivement les programmes des cellules B dans un environnement de type arthritique tout en laissant la plupart des cellules T et des cellules de la membrane articulaire intactes. Plutôt que d’éradiquer les cellules B, cette approche les pousse dans un état de point de contrôle où elles cessent de sécréter des molécules inflammatoires et des anticorps. Pour les patients, l’idée reste théorique, mais elle suggère que des expositions précisément réglées et de courte durée à la radiation ou à des médicaments génotoxiques pourraient un jour être utilisées non pas pour tuer les cellules, mais pour silencier temporairement les plus problématiques. De telles stratégies pourraient compléter les thérapies existantes et, en principe, offrir un moyen d’endiguer l’inflammation auto-immune chronique avec moins de dommages collatéraux pour le système immunitaire.
Citation: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Mots-clés: polyarthrite rhumatoïde, cellules B, lésions de l’ADN, modulation immunitaire, maladie auto-immune