Clear Sky Science · sv
Subletalt DNA‑skada stänger av B‑cells effektorprogram i en RA‑FLS‑PBMC‑samsättning
Dämpa ett överaktivt immunsvar
Reumatoid artrit drivs delvis av immunceller som angriper kroppens egna leder och orsakar smärta, svullnad och bestående skador. Många av dagens läkemedel fungerar genom att eliminera hela grupper av immunceller, vilket kan göra patienterna mer mottagliga för infektioner. Denna studie undersöker en mer subtil idé: om en mycket liten, noggrant kontrollerad dos DNA‑skada tillfälligt kan stänga av den skadliga aktiviteten hos vissa immunceller—särskilt B‑celler—utan att faktiskt döda majoriteten av dem. Om det visar sig fungera kan angreppssättet peka mot mildare behandlingar som lugnar sjukdomen samtidigt som större delen av immunsystemet förblir intakt.
Varför B‑celler är ett särskilt svagt punkt
B‑celler är mest kända för att bilda antikroppar, men vid reumatoid artrit bidrar de också till att upprätthålla inflammation och organisera immunologiska ”hot spots” i leden. För att finslipa de antikroppar de producerar skär aktiverade B‑celler medvetet i sitt eget DNA och syr sedan ihop det igen. Detta ovanliga beteende gör dem mer känsliga för ytterligare skador än många andra celltyper. Forskarna antog att en liten extra ”knuff” av DNA‑skada, under den nivå som orsakar massdöd, skulle kunna utnyttja denna sårbarhet och selektivt tysta B‑cellsaktivitet. Samtidigt ville de undvika att brett förgifta immunceller eller skada de strukturella cellerna som bildar ledens hinna.
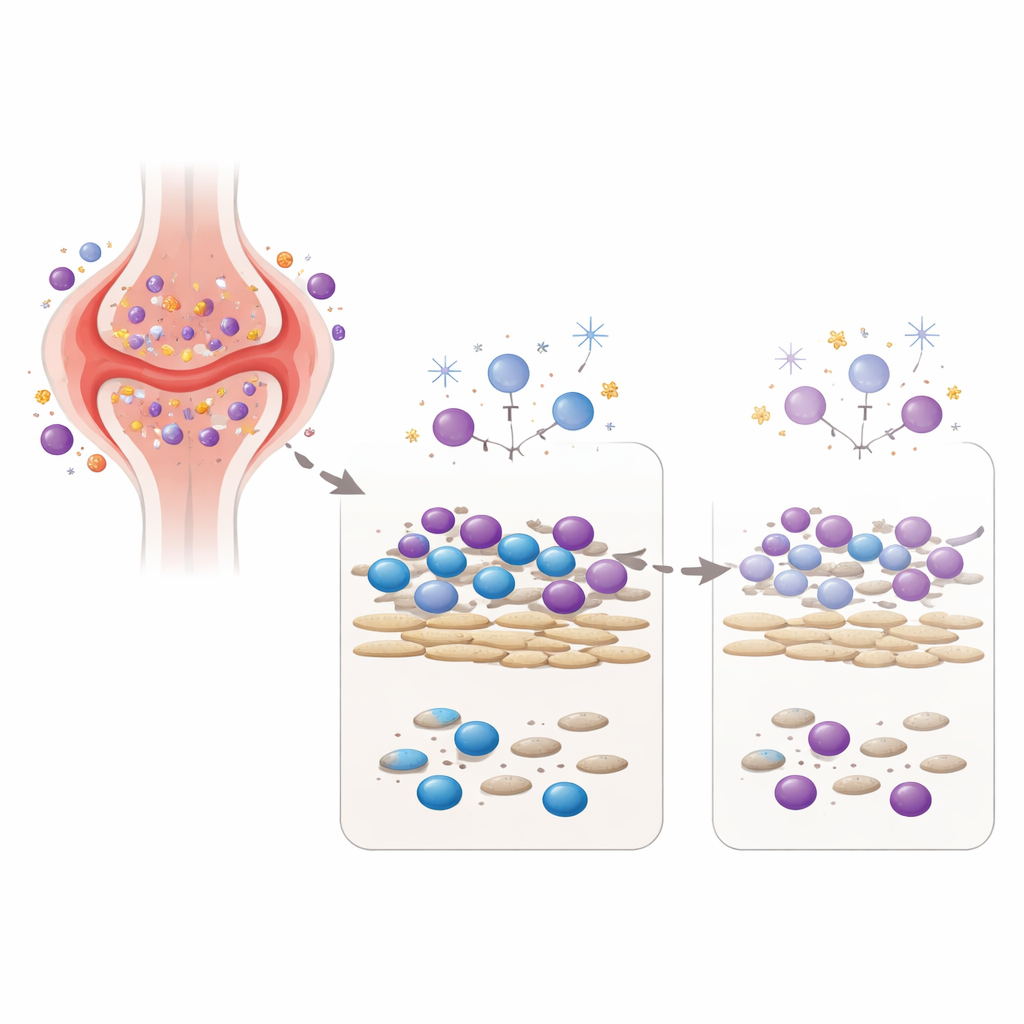
Återskapa den artritdrabbade leden i en skål
För att testa konceptet satte teamet upp en laboratoriemodell som för samman två nyckelspelare från leden: fibroblastliknande synoviocyter, som är bindvävsceller från patienter med reumatoid artrit, och blodets immunceller från friska volontärer. I denna samsättning ger fibroblasterna signaler som håller immuncellerna vid liv och aktiva, ungefär som miljön inne i en inflammerad led. Forskarna exponerade sedan denna blandade cellgemenskap för en enkel, noggrant utvald dos av tre olika DNA‑skadande medel: lågdos gamma‑bestrålning, väteperoxid (en reaktiv syreart som också finns i inflammerad vävnad) och en läkemedelsmetabolit relaterad till cyklofosfamid, en cytostatika som används vid svåra autoimmuna sjukdomar. De mätte inte bara hur många celler som överlevde, utan också hur mycket antikroppar och cytokin—immunsignal‑molekyler—cellerna producerade flera dagar senare.
Stänga av funktion utan massiv cellförlust
Över alla tre medel framträdde ett tydligt mönster: B‑cellsfunktioner reducerades kraftigt vid doser som fortfarande lämnade de flesta celler vid liv. Till exempel, efter en måttlig dos gamma‑bestrålning höll den övergripande cellöverlevnaden sig över 80 procent, ändå minskade viktiga signaler som den antiinflammatoriska cytokin IL‑10 och flera antikroppstyper med ungefär hälften eller mer. Väteperoxid och läkemedelsmetaboliten visade liknande eller ännu starkare dämpning av antikropps‑ och cytokinproduktion, ibland samtidigt som mer än två tredjedelar av cellerna fortfarande var livsdugliga. Med andra ord skiljde den genotoxiska ”träffen” immunaktivitet från cellöverlevnad—cellerna var närvarande, men deras förmåga att driva inflammation var kraftigt nedskruvad.
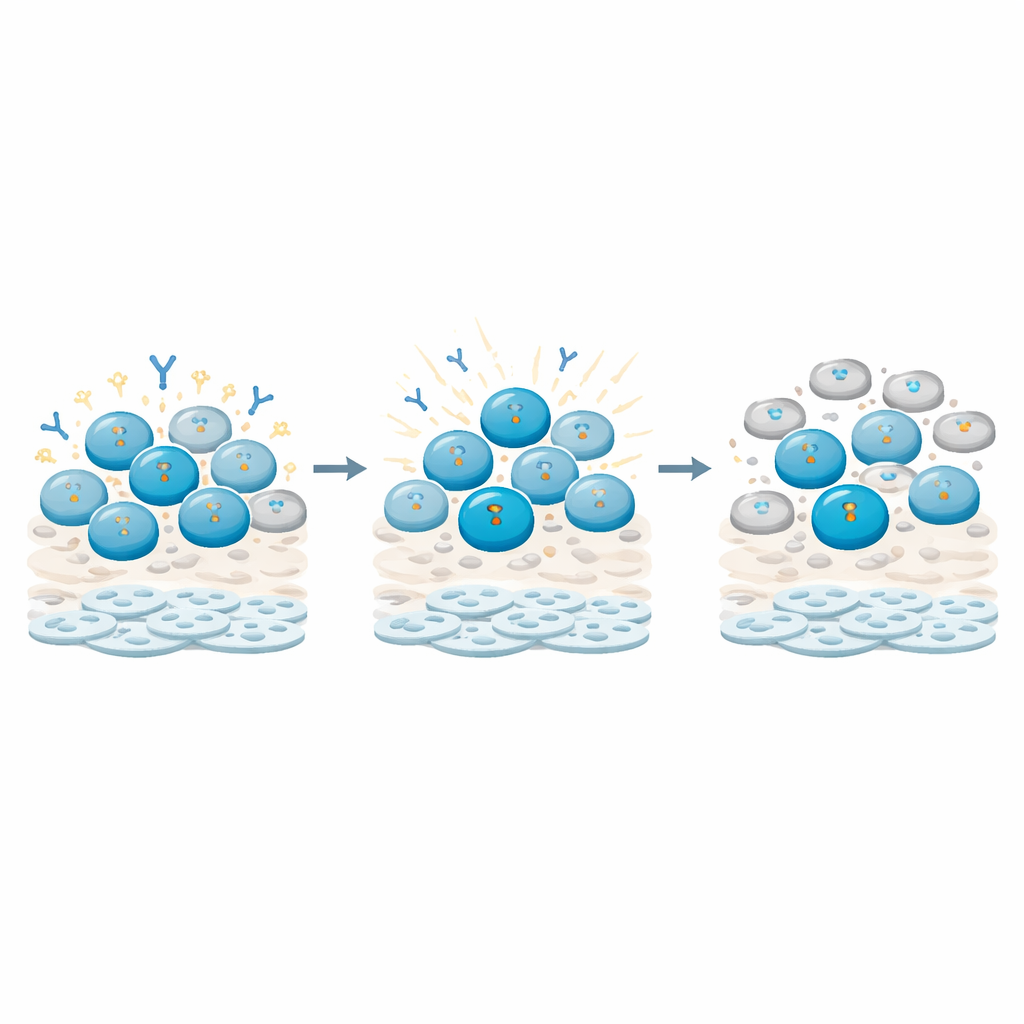
Hur B‑celler känner av skada och trycker på bromsen
Genom att gå djupare följde forskarna molekylära tecken på DNA‑skada i olika immuncellstyper. De fann att B‑celler, särskilt minneselement (de som är förberedda av tidigare möten), ackumulerade särskilt starka och långvariga signaler för DNA‑skada jämfört med T‑celler. Dessa signaler kopplades till kontrollpunkter som stoppade B‑cellernas cellcykel och höll dem fast i en vilofas snarare än i aktiv delning och differentiering. Samtidigt omformades genaktivitet kopplad till antikroppsproduktion och B‑cellsmognad: vissa huvudregulatorer och transkript av antikroppskedjor steg eller sjönk i mönster som tyder på att cellerna hölls i ett ”reparera först, fungera senare”‑tillstånd. T‑celler visade däremot mer övergående svar och återhämtade i stort sett sin cykling.
En ny vinkel på mjukare autoimmuna terapier
Sammantaget visar studien att en enda, lågintensiv puls av DNA‑skada kan selektivt tysta B‑cellsprogram i en artritliknande miljö samtidigt som de flesta T‑celler och ledhinnans celler förblir intakta. Istället för att utplåna B‑celler skjutsar detta angreppssätt dem in i ett kontrollpunktstillstånd där de slutar producera inflammatoriska molekyler och antikroppar. För patienter är idén fortfarande teoretisk, men den antyder att precis avvägda, kortvariga exponeringar för strålning eller genotoxiska läkemedel en dag skulle kunna användas inte bara för att döda celler utan för att temporärt tysta de mest besvärliga. Sådana strategier skulle kunna komplettera befintliga terapier och i princip erbjuda ett sätt att tygla kronisk autoimmun inflammation med mindre kollateral skada på immunsystemet.
Citering: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Nyckelord: reumatoid artrit, B‑celler, DNA‑skada, immunsmodulering, autoimmun sjukdom