Clear Sky Science · nl
Subletale DNA-schade schakelt B-cel effectorprogramma’s uit in een RA-FLS-PBMC co-cultuur
Een overdreven immuunrespons terugschakelen
Reumatoïde artritis wordt deels aangedreven door immuuncellen die de eigen gewrichten van het lichaam aanvallen, wat leidt tot pijn, zwelling en blijvende schade. Veel huidige geneesmiddelen werken door hele groepen immuuncellen uit te schakelen, waardoor patiënten vatbaarder kunnen worden voor infecties. Deze studie onderzoekt een subtieler idee: of een kleine, zorgvuldig gecontroleerde dosis DNA-schade de schadelijke activiteit van bepaalde immuuncellen — in het bijzonder B-cellen — tijdelijk kan uitschakelen zonder de meeste van deze cellen daadwerkelijk te doden. Als dat lukt, zou deze benadering kunnen wijzen op mildere behandelingen die de ziekte tot rust brengen terwijl een groot deel van het immuunsysteem behouden blijft.
Waarom B-cellen een bijzondere kwetsbaarheid zijn
B-cellen staan vooral bekend om het maken van antilichamen, maar bij reumatoïde artritis helpen ze ook de ontsteking in stand te houden en immuunchakels binnen het gewricht te organiseren. Om de antilichamen die ze produceren bij te stellen, knippen en herverbinden geactiveerde B-cellen bewust hun eigen DNA. Dit ongebruikelijke gedrag maakt ze gevoeliger voor extra schade dan veel andere cellen. De onderzoekers redeneerden dat een kleine extra "duw" van DNA-schade, onder het niveau dat massale celdood veroorzaakt, deze kwetsbaarheid zou kunnen exploiteren en selectief de B-celactiviteit stilleggen. Tegelijkertijd wilden ze breed vergiftigen van immuuncellen of schade aan de structurele cellen van het gewrichtsslijmvlies vermijden.
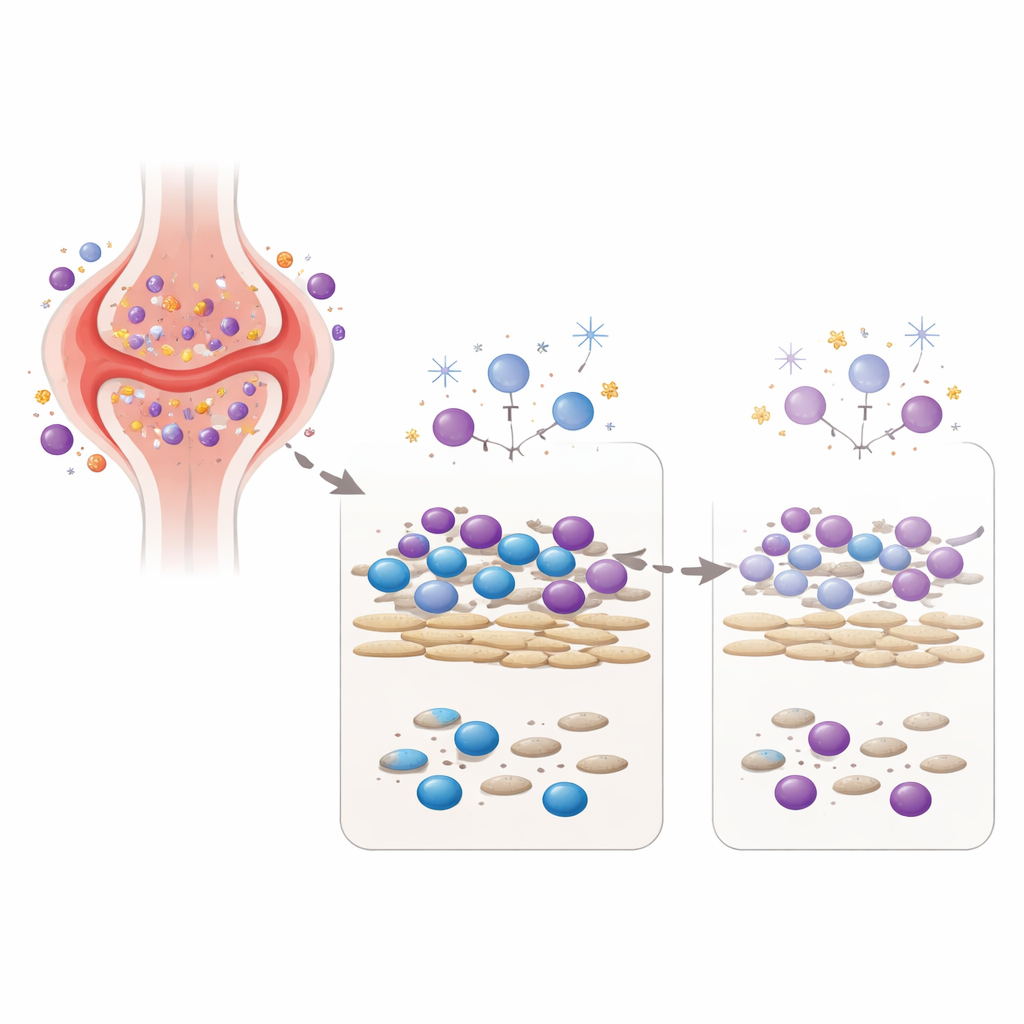
Het artritische gewricht nabootsen in een schaaltje
Om dit concept te testen, zette het team een laboratoriummodel op dat twee sleutelfiguren uit het gewricht samenbrengt: fibroblastachtige synoviocyten, bindweefselcellen van patiënten met reumatoïde artritis, en bloedimmuuncellen van gezonde vrijwilligers. In deze co-cultuur geven de fibroblasten signalen die immuuncellen levend en actief houden, enigszins vergelijkbaar met de omgeving binnen een ontstoken gewricht. De onderzoekers stelden deze gemengde celpopulatie vervolgens bloot aan een enkele, zorgvuldig gekozen dosis van drie verschillende DNA-schadigende middelen: lage dosis gammastraling, waterstofperoxide (een reactieve zuurstofsoort die ook in ontstoken weefsel voorkomt) en een geneesmiddelmetaboliet verwant aan cyclofosfamide, een chemotherapeuticum dat gebruikt wordt bij ernstige auto-immuunziekten. Ze maten niet alleen hoeveel cellen overleefden, maar ook hoeveel antilichamen en cytokinen — immuunboodschappermoleculen — de cellen dagen later produceerden.
Functie uitschakelen zonder massaal celverlies
Bij alle drie de middelen verscheen een duidelijk patroon: B-celfuncties werden sterk gereduceerd bij doses die de meeste cellen nog in leven lieten. Bijvoorbeeld, na een bescheiden dosis gammastraling bleef de algehele celdoorleving boven de 80 procent, maar belangrijke signalen zoals het ontstekingsremmende cytokine IL-10 en meerdere antilichaamtypen daalden met ongeveer de helft of meer. Waterstofperoxide en de chemotherapiemetaboliet lieten vergelijkbare of zelfs sterkere demping van antilichaam- en cytokineproductie zien, soms terwijl nog meer dan twee derde van de cellen levensvatbaar bleef. Met andere woorden, de genotoxische "slag" ontkoppelde immuunactiviteit van celdoorleving — de cellen waren aanwezig, maar hun vermogen om ontsteking aan te jagen was scherp teruggeschroefd.
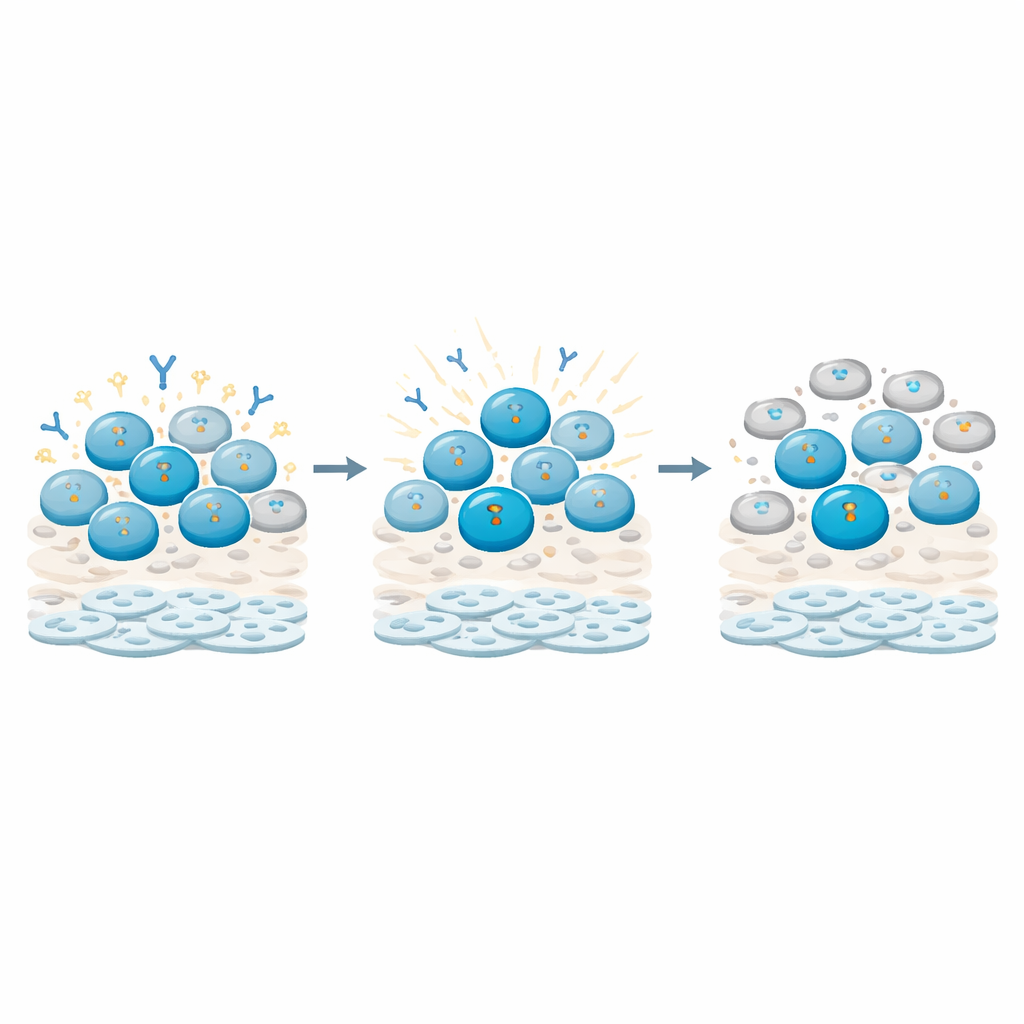
Hoe B-cellen schade waarnemen en op de rem trappen
Dieper gravend volgden de onderzoekers moleculaire tekenen van DNA-schade in verschillende immuunceltypen. Ze vonden dat B-cellen, vooral geheugen-B-cellen (die geprimed zijn door eerdere ontmoetingen), bijzonder sterke en blijvende signalen van DNA-letsel ophoopten vergeleken met T-cellen. Deze signalen voedden checkpoints die de celdeling van B-cellen stopzetten, waardoor ze vastzaten in een rustfase in plaats van actief te delen en te differentiëren. Tegelijkertijd werd de genactiviteit gekoppeld aan antilichaamproductie en B-celmaturatie herschikt: enkele hoofdregulatoren en antilichaamketentranscripten stegen of daalden in patronen die erop wezen dat de cellen in een "eerst repareren, later functioneren"-staat werden gehouden. T-cellen daarentegen toonden meer voorbijgaande reacties en herstelden grotendeels hun delingsgedrag.
Een nieuw perspectief op zachtere auto-immuuntherapieën
Al met al laat de studie zien dat een enkele, laag-niveau uitstoot van DNA-schade selectief B-celprogramma’s kan dempen in een artritisachtige omgeving, terwijl de meeste T-cellen en gewrichtsslijmvliescellen intact blijven. In plaats van B-cellen te vernietigen, duwt deze benadering ze in een checkpointstaat waarin ze stoppen met het pompen van ontstekingsmoleculen en antilichamen. Voor patiënten blijft het idee theoretisch, maar het suggereert dat precies afgestelde, kortdurende blootstellingen aan straling of genotoxische geneesmiddelen op termijn gebruikt zouden kunnen worden om niet alleen cellen te doden, maar tijdelijk de meest problematische te laten zwijgen. Dergelijke strategieën zouden bestaande therapieën kunnen aanvullen en in principe een manier bieden om chronische auto-immuunontsteking te temmen met minder nevenschade aan het immuunsysteem.
Bronvermelding: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Trefwoorden: reumatoïde artritis, B-cellen, DNA-schade, immuunmodulatie, auto-immuunziekte