Clear Sky Science · it
Il danno al DNA subletale spegne i programmi effettrici delle cellule B in una co-coltura RA-FLS-PBMC
Abbassare una risposta immunitaria iperattiva
L’artrite reumatoide è guidata in parte da cellule del sistema immunitario che attaccano le articolazioni dell’organismo, causando dolore, gonfiore e danni a lungo termine. Molti farmaci attuali agiscono eliminando interi gruppi di cellule immunitarie, il che può rendere i pazienti vulnerabili alle infezioni. Questo studio esplora un’idea più sottile: se una piccola dose, controllata con precisione, di danno al DNA possa temporaneamente disattivare l’attività dannosa di certe cellule immunitarie—soprattutto le cellule B—senza però uccidere la maggior parte di esse. Se efficace, questo approccio potrebbe indicare terapie più delicate che calmerebbero la malattia mantenendo gran parte del sistema immunitario intatto.
Perché le cellule B sono un punto debole particolare
Le cellule B sono note soprattutto per produrre anticorpi, ma nell’artrite reumatoide contribuiscono anche a sostenere l’infiammazione e a organizzare “punti caldi” immunitari all’interno dell’articolazione. Per perfezionare gli anticorpi che producono, le cellule B attivate tagliano e riannodano deliberatamente il proprio DNA. Questo comportamento insolito le rende più sensibili a danni aggiuntivi rispetto a molte altre cellule. I ricercatori hanno ipotizzato che una piccola «spinta» aggiuntiva di danno al DNA, al di sotto della soglia che provoca una morte cellulare di massa, potrebbe sfruttare questa vulnerabilità e mettere selettivamente a tacere l’attività delle cellule B. Allo stesso tempo, volevano evitare di avvelenare in modo diffuso le cellule immunitarie o danneggiare le cellule strutturali che formano il rivestimento delle articolazioni.
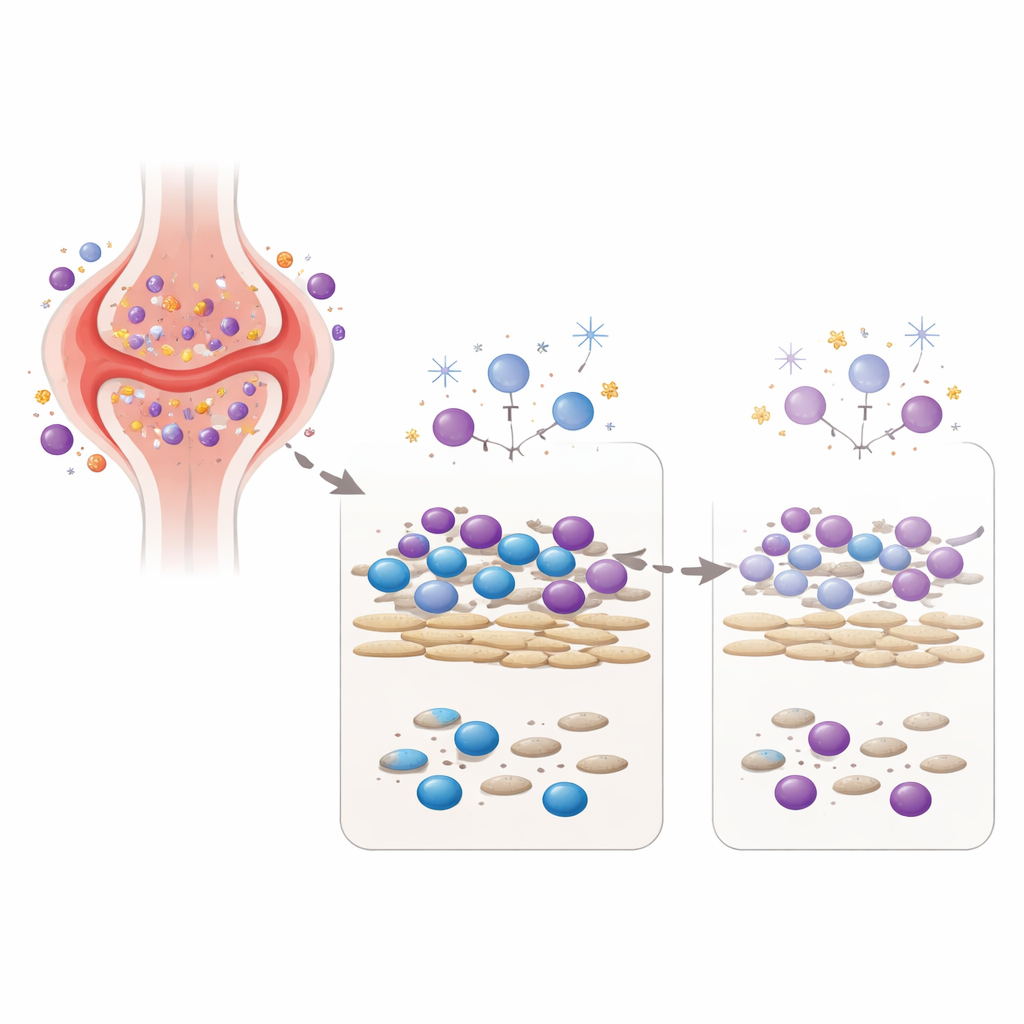
Ricreare l’articolazione artritica in una piastra
Per mettere alla prova questo concetto, il gruppo ha allestito un modello di laboratorio che mette insieme due attori chiave dell’articolazione: fibroblasti sinoviali simili a quelli dei pazienti con artrite reumatoide e cellule immunitarie del sangue provenienti da volontari sani. In questa co-coltura, i fibroblasti forniscono segnali che mantengono vive e attive le cellule immunitarie, in modo analogo all’ambiente presente in un’articolazione infiammata. I ricercatori hanno quindi esposto questa comunità cellulare mista a una singola dose, scelta con cura, di tre diversi agenti che danneggiano il DNA: radiazioni gamma a basso dosaggio, perossido di idrogeno (una specie reattiva dell’ossigeno presente anche nei tessuti infiammati) e un metabolita di un farmaco correlato alla ciclofosfamide, una chemioterapia usata nelle malattie autoimmuni severe. Hanno misurato non solo quante cellule sopravvivevano, ma anche quanto anticorpo e quante citochine—molecole messaggere del sistema immunitario—le cellule producevano nei giorni successivi.
Spegnere la funzione senza una perdita cellulare massiva
Con tutti e tre gli agenti è emerso uno schema chiaro: le funzioni delle cellule B sono risultate fortemente ridotte a dosi che lasciavano comunque la maggior parte delle cellule vive. Per esempio, dopo una dose modesta di radiazioni gamma, la sopravvivenza cellulare complessiva rimaneva oltre l’80 percento, eppure segnali chiave come la citochina anti-infiammatoria IL-10 e diversi tipi di anticorpi calavano di circa la metà o più. Il perossido di idrogeno e il metabolita chemioterapico mostrarono un effetto attenuante simile o anche più marcato sulla produzione di anticorpi e citochine, talvolta mentre più dei due terzi delle cellule erano ancora vitali. In altre parole, il «colpo» genotossico ha disaccoppiato l’attività immunitaria dalla sopravvivenza cellulare—le cellule erano presenti, ma la loro capacità di alimentare l’infiammazione era nettamente ridotta.
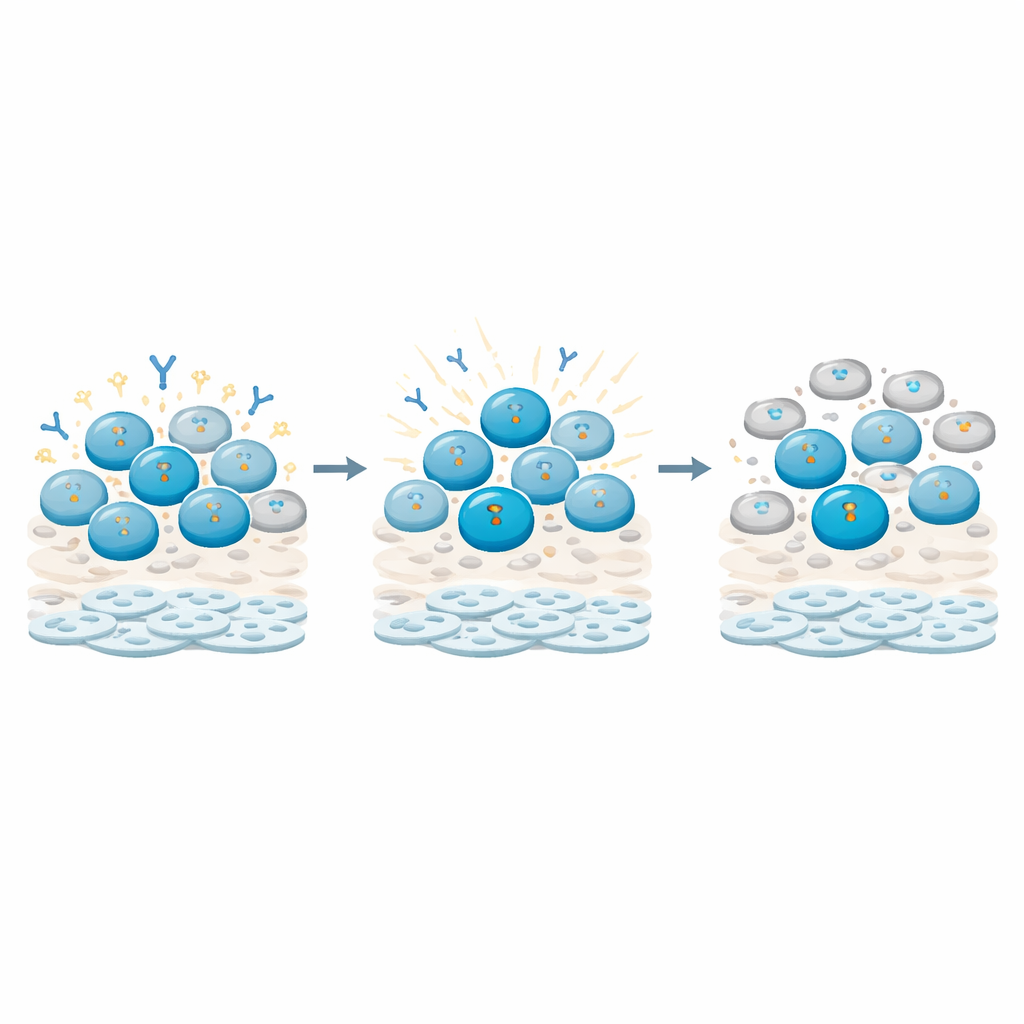
Come le cellule B percepiscono il danno e tirano il freno
Analizzando più in profondità, gli investigatori hanno seguito i segni molecolari del danno al DNA all’interno dei diversi tipi di cellule immunitarie. Hanno osservato che le cellule B, in particolare le cellule B della memoria (quelle preimpostate da incontri precedenti), accumulavano segnali di danno al DNA particolarmente forti e duraturi rispetto alle cellule T. Questi segnali alimentavano checkpoint che fermavano il ciclo cellulare delle cellule B, mantenendole bloccate in una fase di quiescenza invece di dividersi e differenziarsi attivamente. Allo stesso tempo, l’attività genica legata alla produzione di anticorpi e alla maturazione delle cellule B veniva rimodellata: alcuni regolatori principali e trascritti delle catene anticorpali aumentavano o diminuivano secondo schemi che suggerivano che le cellule venissero tenute in uno stato di «ripara prima, funzione dopo». Le cellule T, al contrario, mostravano risposte più transitorie e recuperavano in gran parte il loro comportamento di ciclo.
Un nuovo approccio a terapie più morbide per le malattie autoimmuni
Nel complesso, lo studio dimostra che un singolo episodio a basso livello di danno al DNA può mettere selettivamente a tacere i programmi delle cellule B in un ambiente simile a quello dell’artrite, lasciando intatte la maggior parte delle cellule T e le cellule del rivestimento articolare. Piuttosto che annientare le cellule B, questo approccio le spinge in uno stato di checkpoint in cui cessano di produrre molecole infiammatorie e anticorpi. Per i pazienti, l’idea rimane per ora teorica, ma suggerisce che esposizioni brevi e calibrate a radiazioni o a farmaci genotossici potrebbero un giorno essere usate non solo per uccidere le cellule, ma per silenziare temporaneamente quelle più problematiche. Tali strategie potrebbero integrare le terapie esistenti e, in linea di principio, offrire un modo per domare l’infiammazione autoimmune cronica con meno danni collaterali al sistema immunitario.
Citazione: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Parole chiave: artrite reumatoide, cellule B, danno al DNA, modulazione immunitaria, malattia autoimmune