Clear Sky Science · pt
Dano de DNA subletal desliga programas efetores de células B em uma co-cultura RA-FLS-PBMC
Reduzindo uma resposta imune hiperativa
A artrite reumatoide é impulsionada em parte por células do sistema imunológico que atacam as próprias articulações do corpo, causando dor, inchaço e danos a longo prazo. Muitos medicamentos atuais atuam eliminando grupos inteiros de células imunes, o que pode deixar os pacientes mais vulneráveis a infecções. Este estudo explora uma ideia mais sutil: se uma pequena dose cuidadosamente controlada de dano ao DNA poderia temporariamente desligar a atividade prejudicial de certas células imunes — especialmente as células B — sem realmente matar a maioria delas. Se bem-sucedida, essa abordagem poderia apontar para tratamentos mais suaves que acalmem a doença mantendo boa parte do sistema imunológico intacta.
Por que as células B são um ponto fraco especial
As células B são mais conhecidas por produzir anticorpos, mas na artrite reumatoide elas também ajudam a sustentar a inflamação e a organizar “pontos quentes” imunes dentro da articulação. Para aperfeiçoar os anticorpos que produzem, células B ativadas deliberadamente cortam e religam seu próprio DNA. Esse comportamento incomum as torna mais sensíveis a danos adicionais do que muitas outras células. Os pesquisadores supuseram que um pequeno “empurrão” extra de dano ao DNA, abaixo do nível que causa morte celular em massa, poderia explorar essa vulnerabilidade e calar seletivamente a atividade das células B. Ao mesmo tempo, queriam evitar envenenar amplamente as células imunes ou prejudicar as células estruturais que formam o revestimento da articulação.
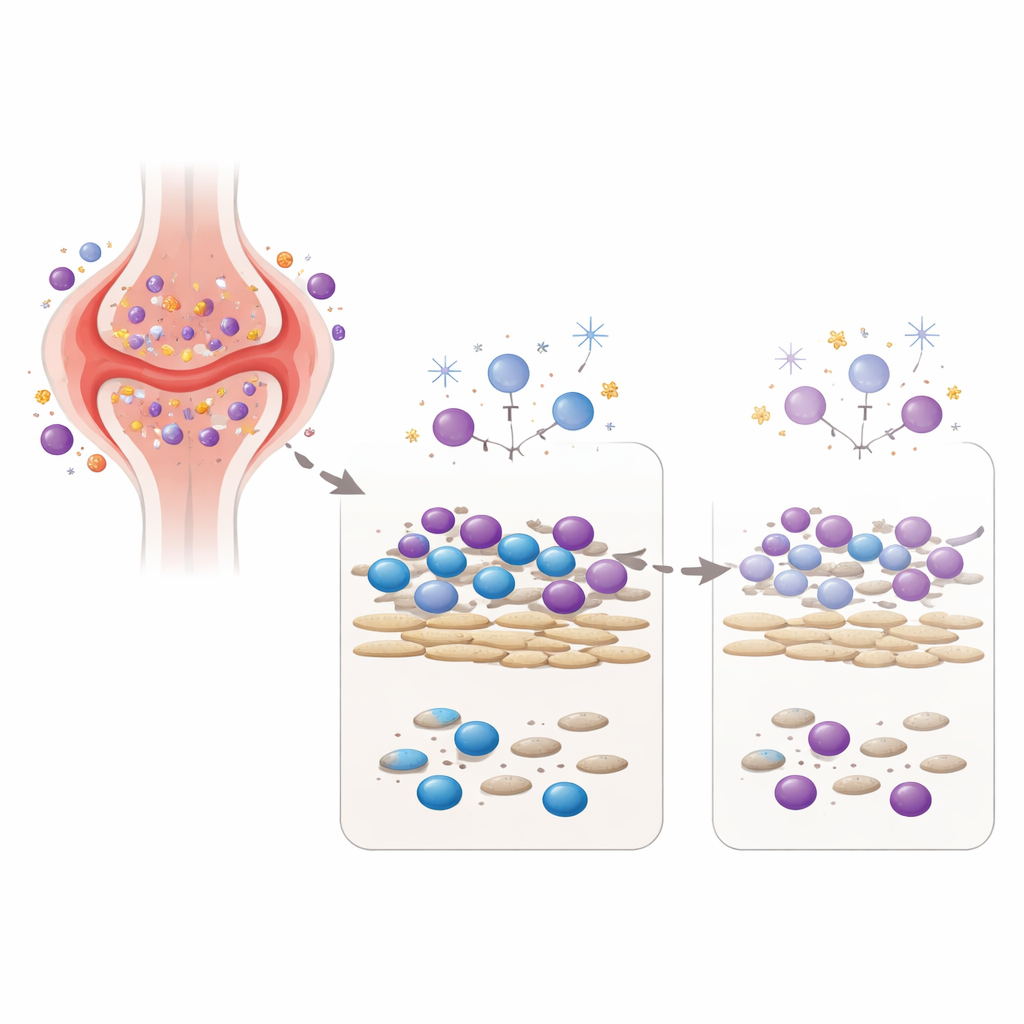
Recriando a articulação artrítica em um prato
Para testar esse conceito, a equipe montou um modelo laboratorial que reúne dois protagonistas chave da articulação: sinoviócitos fibroxantomatosos (fibroblast-like synoviocytes), que são células do tecido conectivo de pacientes com artrite reumatoide, e células imunes sanguíneas de voluntários saudáveis. Nessa co-cultura, os fibroblastos fornecem sinais que mantêm as células imunes vivas e ativas, de forma semelhante ao ambiente dentro de uma articulação inflamada. Os pesquisadores então expuseram essa comunidade celular mista a uma única dose cuidadosamente escolhida de três diferentes agentes danificadores de DNA: radiação gama em baixa dose, peróxido de hidrogênio (uma espécie reativa de oxigênio também encontrada em tecido inflamado) e um metabólito de droga relacionado à ciclofosfamida, uma quimioterapia usada em doenças autoimunes graves. Eles mediram não só quantas células sobreviveram, mas também quanto anticorpo e citocina — moléculas mensageiras do sistema imune — as células produziram dias depois.
Desligando a função sem perda celular massiva
Em todos os três agentes, surgiu um padrão claro: as funções das células B foram fortemente reduzidas em doses que ainda deixavam a maioria das células vivas. Por exemplo, após uma dose modesta de radiação gama, a sobrevivência celular geral permaneceu acima de 80 por cento, mas sinais-chave como a citocina anti-inflamatória IL-10 e vários tipos de anticorpos caíram aproximadamente pela metade ou mais. O peróxido de hidrogênio e o metabólito da quimioterapia mostraram atenuação similar ou até mais intensa da produção de anticorpos e citocinas, às vezes enquanto mais de dois terços das células ainda eram viáveis. Em outras palavras, o “impacto” genotóxico desacoplou a atividade imune da sobrevivência celular — as células estavam presentes, mas sua capacidade de alimentar a inflamação foi fortemente reduzida.
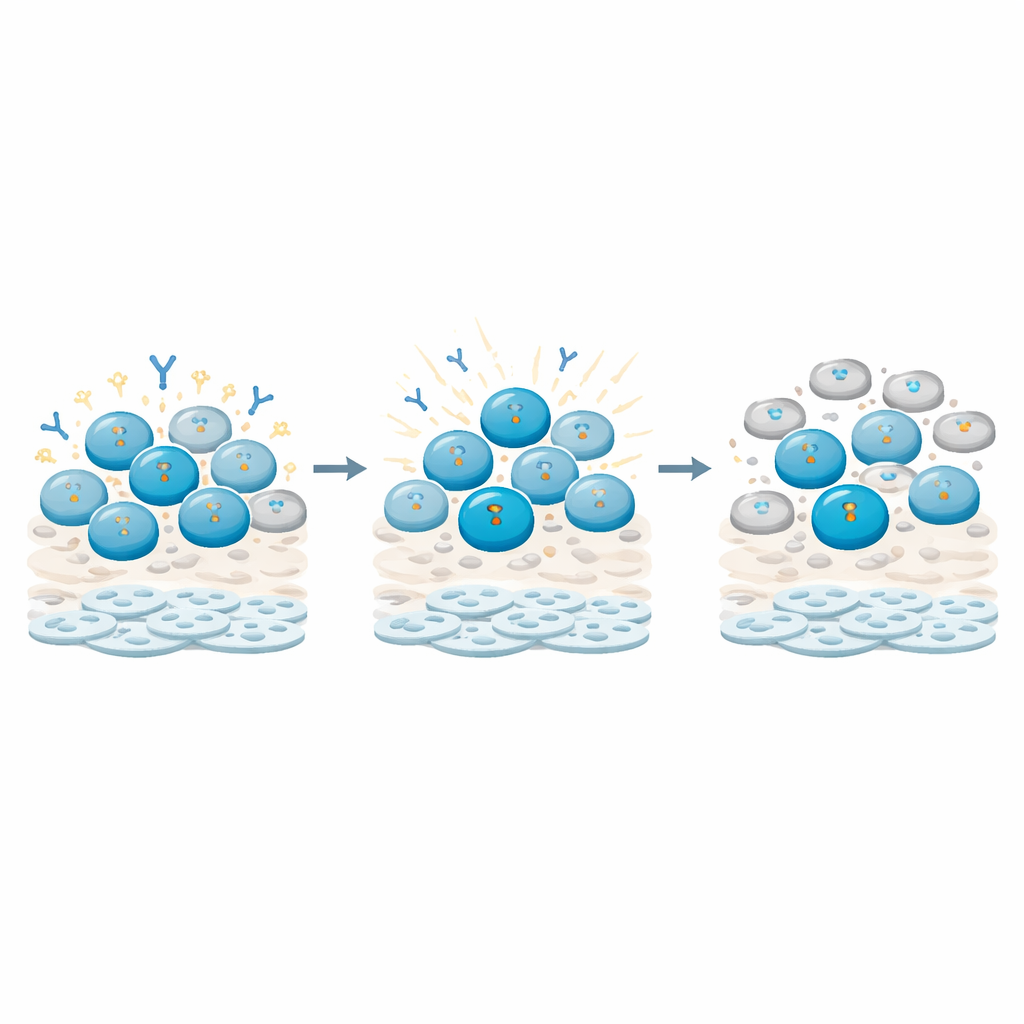
Como as células B detectam dano e apertam o freio
Ao aprofundar, os investigadores rastrearam sinais moleculares de dano ao DNA dentro de diferentes tipos de células imunes. Eles descobriram que as células B, especialmente as células B de memória (aquelas programadas por encontros passados), acumularam sinais particularmente fortes e duradouros de lesão no DNA em comparação com as células T. Esses sinais alimentaram pontos de verificação que pararam o ciclo celular das células B, mantendo-as presas em uma fase de repouso em vez de se dividirem e se diferenciarem ativamente. Ao mesmo tempo, a atividade gênica ligada à produção de anticorpos e à maturação das células B foi remodelada: alguns reguladores mestres e transcritos de cadeias de anticorpos aumentaram ou diminuíram em padrões que sugerem que as células foram mantidas em um estado de “reparar primeiro, funcionar depois”. As células T, por contraste, mostraram respostas mais transitórias e em grande parte recuperaram seu comportamento cíclico.
Uma nova perspectiva para terapias autoimunes mais suaves
No conjunto, o estudo mostra que um único pulso de baixo nível de dano ao DNA pode silenciar seletivamente programas das células B em um ambiente semelhante ao da artrite, preservando a maior parte das células T e das células do revestimento articular. Em vez de obliterar as células B, essa abordagem as empurra para um estado de ponto de verificação onde elas deixam de liberar moléculas e anticorpos inflamatórios. Para os pacientes, a ideia permanece teórica, mas sugere que exposições de curta duração e precisamente calibradas à radiação ou a drogas genotóxicas poderiam algum dia ser usadas não apenas para matar células, mas para silenciar temporariamente as mais problemáticas. Tais estratégias poderiam complementar as terapias existentes e, em princípio, oferecer uma forma de domar a inflamação autoimune crônica com menos danos colaterais ao sistema imunológico.
Citação: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Palavras-chave: artrite reumatoide, células B, dano ao DNA, modulação imune, doença autoimune