Clear Sky Science · es
Daño subletal del ADN apaga los programas efectores de células B en un co-cultivo RA-FLS-PBMC
Reducir una respuesta inmune sobreactivada
La artritis reumatoide está impulsada en parte por células inmunitarias que atacan las propias articulaciones del cuerpo, causando dolor, hinchazón y daño a largo plazo. Muchos fármacos actuales actúan eliminando conjuntos enteros de células inmunes, lo que puede dejar a los pacientes vulnerables a infecciones. Este estudio explora una idea más sutil: si una pequeña dosis cuidadosamente controlada de daño al ADN podría apagar temporalmente la actividad perjudicial de ciertas células inmunes —especialmente las células B— sin llegar a matar a la mayoría de ellas. Si tuviera éxito, este enfoque podría apuntar a tratamientos más suaves que calmen la enfermedad manteniendo gran parte del sistema inmune intacto.
Por qué las células B son un punto débil especial
Las células B son conocidas sobre todo por producir anticuerpos, pero en la artritis reumatoide también ayudan a sostener la inflamación y a organizar «puntos calientes» inmunitarios dentro de la articulación. Para afinar los anticuerpos que generan, las células B activadas cortan y vuelven a unir deliberadamente su propio ADN. Este comportamiento inusual las hace más sensibles a daños adicionales que muchas otras células. Los investigadores razonaron que un pequeño «empujón» extra de daño al ADN, por debajo del umbral que provoca muerte masiva celular, podría explotar esta vulnerabilidad y apaciguar selectivamente la actividad de las células B. Al mismo tiempo, querían evitar envenenar de forma general a las células inmunes o dañar las células estructurales que forman el revestimiento de la articulación.
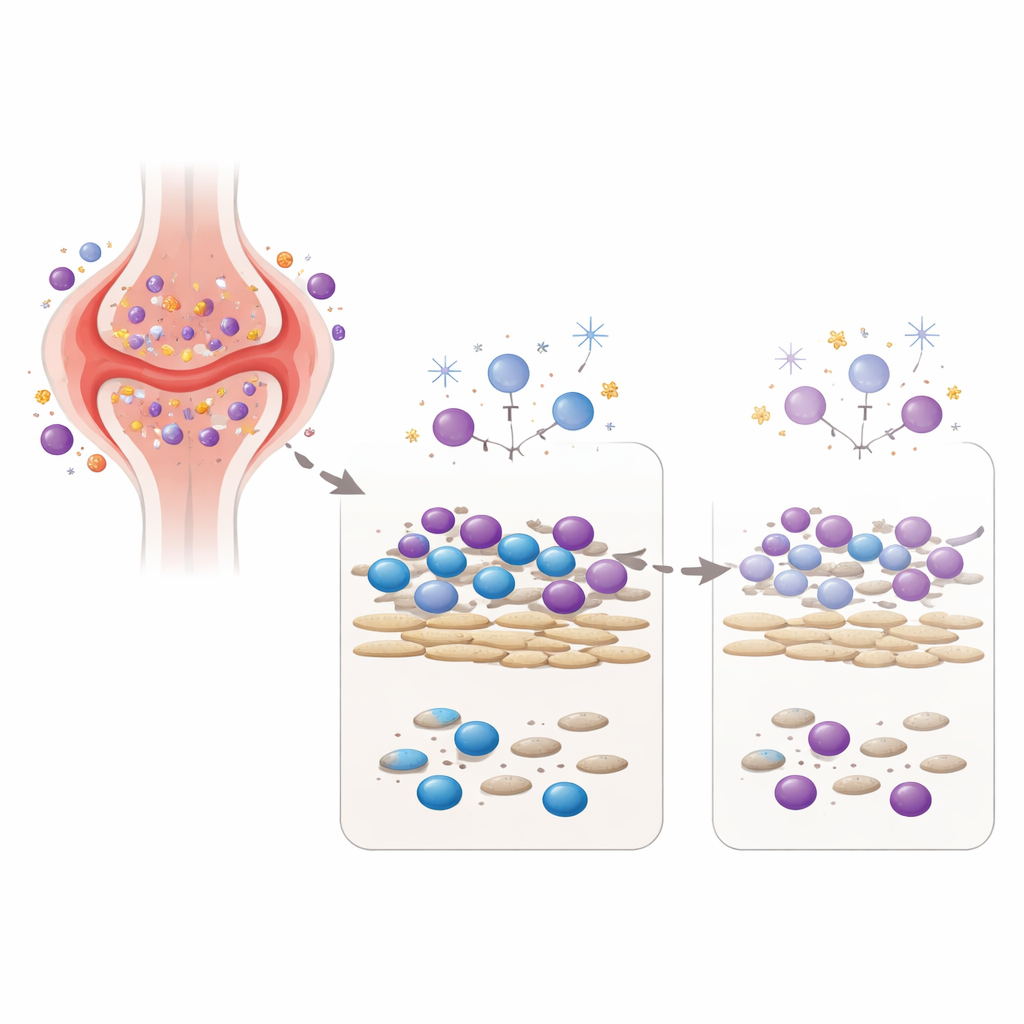
Recrear la articulación artrítica en un plato
Para probar este concepto, el equipo montó un modelo de laboratorio que reúne a dos actores clave de la articulación: sinoviocitos tipo fibroblasto, que son células del tejido conectivo de pacientes con artritis reumatoide, y células inmunitarias sanguíneas de voluntarios sanos. En este co-cultivo, los fibroblastos proporcionan señales que mantienen a las células inmunes vivas y activas, de forma parecida al entorno dentro de una articulación inflamada. Los investigadores expusieron esta comunidad celular mixta a una única dosis cuidadosamente elegida de tres agentes distintos que dañan el ADN: irradiación gamma a baja dosis, peróxido de hidrógeno (una especie reactiva de oxígeno también presente en tejido inflamado) y un metabolito farmacológico relacionado con ciclofosfamida, una quimioterapia usada en enfermedades autoinmunes graves. Midieron no solo cuántas células sobrevivían, sino también cuánto anticuerpo y citocinas —moléculas mensajeras inmunes— producían las células días después.
Apagar la función sin pérdida masiva de células
En los tres agentes se observó un patrón claro: las funciones de las células B se redujeron de forma marcada con dosis que aún dejaban a la mayoría de las células vivas. Por ejemplo, tras una dosis modesta de irradiación gamma, la supervivencia celular general se mantuvo por encima del 80 por ciento, pero señales clave como la citocina antiinflamatoria IL-10 y varios tipos de anticuerpos cayeron en torno a la mitad o más. El peróxido de hidrógeno y el metabolito quimioterápico mostraron efectos similares o incluso más fuertes en la disminución de la producción de anticuerpos y citocinas, a veces mientras más de dos tercios de las células seguían viables. En otras palabras, el «impacto» genotóxico desacopló la actividad inmunitaria de la supervivencia celular: las células estaban presentes, pero su capacidad para alimentar la inflamación quedó notablemente reducida.
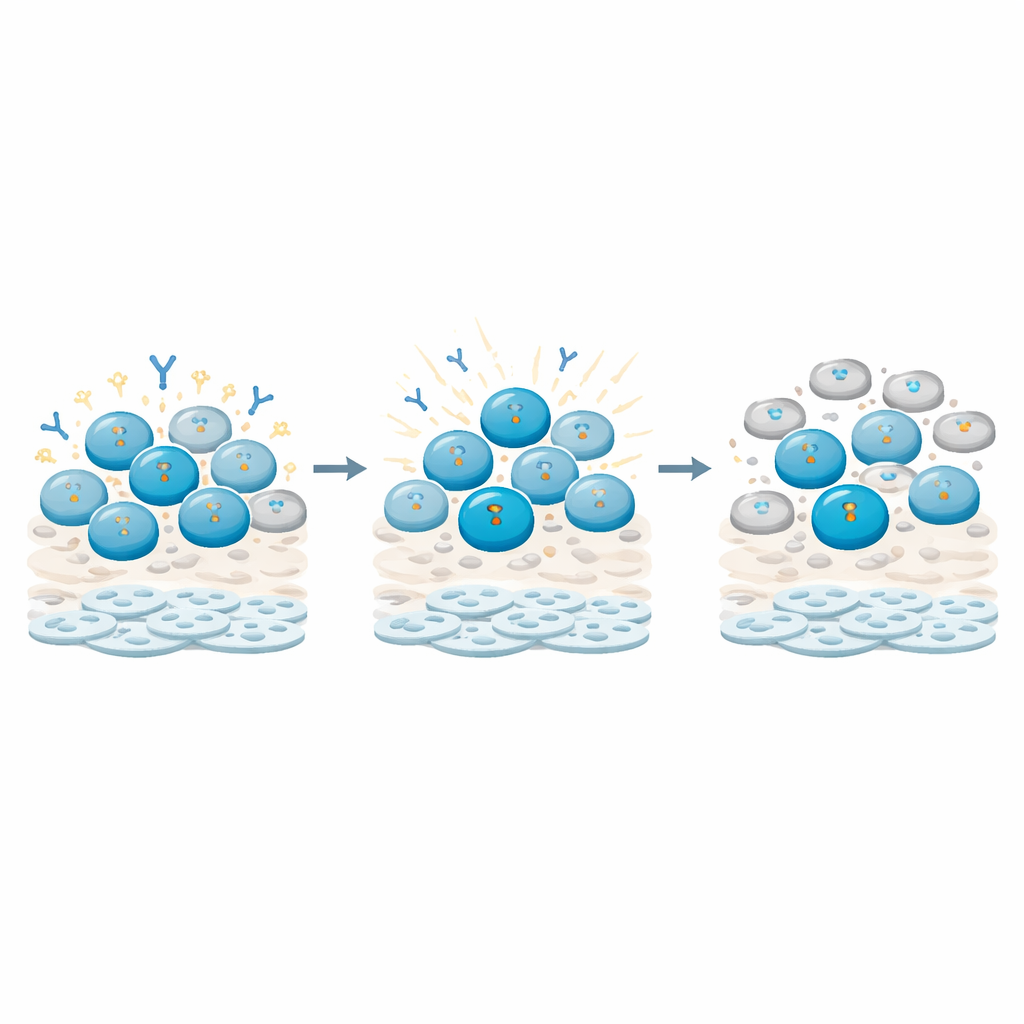
Cómo las células B perciben el daño y ponen el freno
Indagando más a fondo, los investigadores rastrearon señales moleculares de daño del ADN dentro de distintos tipos de células inmunes. Encontraron que las células B, especialmente las células B de memoria (las primadas por encuentros previos), acumulaban señales de lesión del ADN particularmente fuertes y duraderas en comparación con las células T. Estas señales alimentaban puntos de control que detenían el ciclo celular de las células B, manteniéndolas en una fase de reposo en lugar de dividirse y diferenciarse activamente. Al mismo tiempo, la actividad génica ligada a la producción de anticuerpos y la maduración de las células B se reconfiguró: algunos reguladores maestros y transcritos de las cadenas de anticuerpos subieron o bajaron en patrones que sugieren que las células eran retenidas en un estado de «reparar primero, funcionar después». Las células T, en cambio, mostraron respuestas más transitorias y en gran medida recuperaron su comportamiento proliferativo.
Una nueva perspectiva para terapias inmunes más suaves
En conjunto, el estudio demuestra que una única ráfaga de daño del ADN a bajo nivel puede silenciar selectivamente los programas de las células B en un entorno similar a la artritis, mientras deja intactas a la mayoría de las células T y a las células del revestimiento articular. En lugar de eliminar las células B, este enfoque las empuja hacia un estado de control donde dejan de secretar moléculas inflamatorias y anticuerpos. Para los pacientes, la idea sigue siendo teórica, pero sugiere que exposiciones breves y afinadas a radiación o fármacos genotóxicos podrían algún día usarse no solo para matar células, sino para silenciar temporalmente las más problemáticas. Tales estrategias podrían complementar las terapias existentes y, en principio, ofrecer una forma de domar la inflamación autoinmune crónica con menos daños colaterales al sistema inmune.
Cita: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Palabras clave: artritis reumatoide, células B, daño del ADN, modulación inmune, enfermedad autoinmune