Clear Sky Science · pl
Uszkodzenia DNA poniżej progu śmiertelności wyłączają programy efektorowe limfocytów B w ko-kulturze RA-FLS-PBMC
Tłumienie nadmiernej reakcji odpornościowej
Reumatoidalne zapalenie stawów jest częściowo napędzane przez komórki odpornościowe, które atakują własne stawy, powodując ból, obrzęk i długotrwałe uszkodzenia. Wiele obecnych leków działa przez eliminację całych grup komórek odpornościowych, co może pozostawiać pacjentów podatnych na infekcje. W badaniu tym zbadano subtelniejszą koncepcję: czy niewielka, precyzyjnie kontrolowana dawka uszkodzeń DNA może tymczasowo wyłączyć szkodliwą aktywność niektórych komórek odpornościowych — w szczególności limfocytów B — bez zabijania większości z nich. Jeśli okazałoby się skuteczne, podejście to mogłoby wskazać drogę ku łagodniejszym terapiom, które uciszają chorobę przy zachowaniu dużej części układu odpornościowego.
Dlaczego limfocyty B są szczególną słabością
Limfocyty B są najbardziej znane z wytwarzania przeciwciał, ale w reumatoidalnym zapaleniu stawów pomagają też podtrzymywać stan zapalny i organizować „ogniska” odpornościowe w obrębie stawu. Aby dopracować produkowane przeciwciała, aktywowane limfocyty B celowo dokonują cięć i ponownych przestawień własnego DNA. To nietypowe zachowanie czyni je bardziej wrażliwymi na dodatkowe uszkodzenia niż wiele innych komórek. Badacze założyli, że niewielki dodatkowy „pchnięcie” uszkodzeń DNA, poniżej progu wywołującego masowe obumieranie komórek, może wykorzystać tę podatność i selektywnie uciszyć funkcje limfocytów B. Jednocześnie chcieli uniknąć szerokiego zatrucia komórek odpornościowych lub uszkodzenia komórek strukturalnych tworzących wyściółkę stawu.
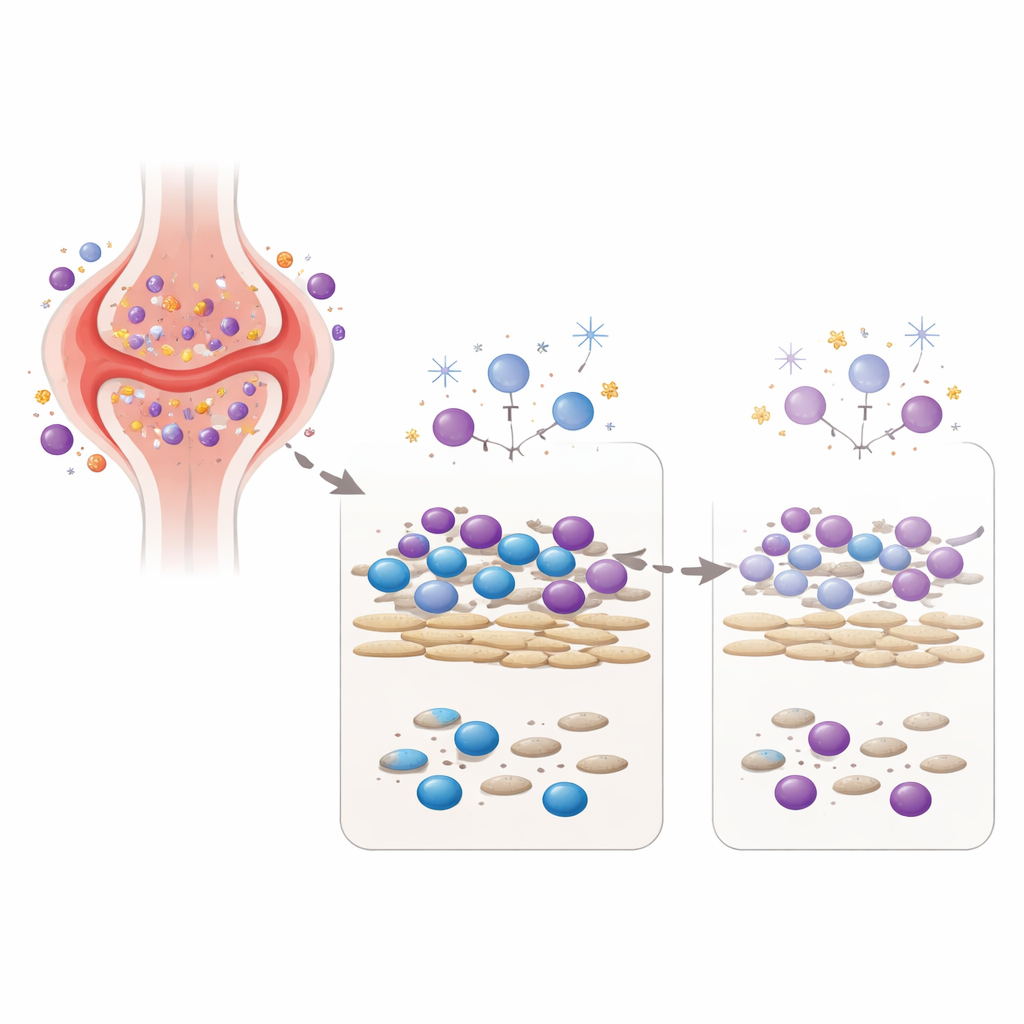
Odtworzenie stawu dotkniętego zapaleniem w naczyniu
Aby przetestować tę koncepcję, zespół stworzył model laboratoryjny łączący dwóch kluczowych graczy ze stawu: fibroblastopodobne synowiocyty pochodzące od pacjentów z reumatoidalnym zapaleniem stawów oraz komórki krwi obwodowej od zdrowych dawców. W tej ko-kulturze fibroblasty dostarczają sygnałów umożliwiających przeżycie i aktywację komórek odpornościowych, podobnie jak środowisko wewnątrz zapalonego stawu. Badacze następnie wystawili tę mieszaną społeczność komórkową na pojedynczą, starannie dobraną dawkę jednego z trzech różnorodnych czynników uszkadzających DNA: niskodawkową radiację gamma, nadtlenek wodoru (reaktywny rodzaj tlenu obecny także w zapalnej tkance) oraz metabolit leku związanego z cyklofosfamidem, chemioterapią stosowaną w ciężkich chorobach autoimmunologicznych. Mierzono nie tylko przeżywalność komórek, ale też, kilka dni później, ilość wytwarzanych przeciwciał i cytokin — przekaźników układu odpornościowego.
Wyłączenie funkcji bez masowej utraty komórek
We wszystkich trzech przypadkach wyłonił się wyraźny wzorzec: funkcje limfocytów B były silnie zmniejszone przy dawkach, które pozostawiały większość komórek przy życiu. Na przykład po umiarkowanej dawce promieniowania gamma ogólna przeżywalność komórek utrzymywała się powyżej 80 procent, a mimo to kluczowe sygnały, takie jak przeciwzapalna cytokina IL-10 i kilka rodzajów przeciwciał, spadły o około połowę lub więcej. Nadtlenek wodoru i metabolit chemioterapeutyczny wykazały podobne lub nawet silniejsze tłumienie produkcji przeciwciał i cytokin, czasami przy zachowaniu żywotności ponad dwóch trzecich komórek. Innymi słowy, uszkodzenie genotoksyczne rozłączało aktywność immunologiczną od przeżycia komórek — komórki były obecne, ale ich zdolność do napędzania stanu zapalnego została wyraźnie stłumiona.
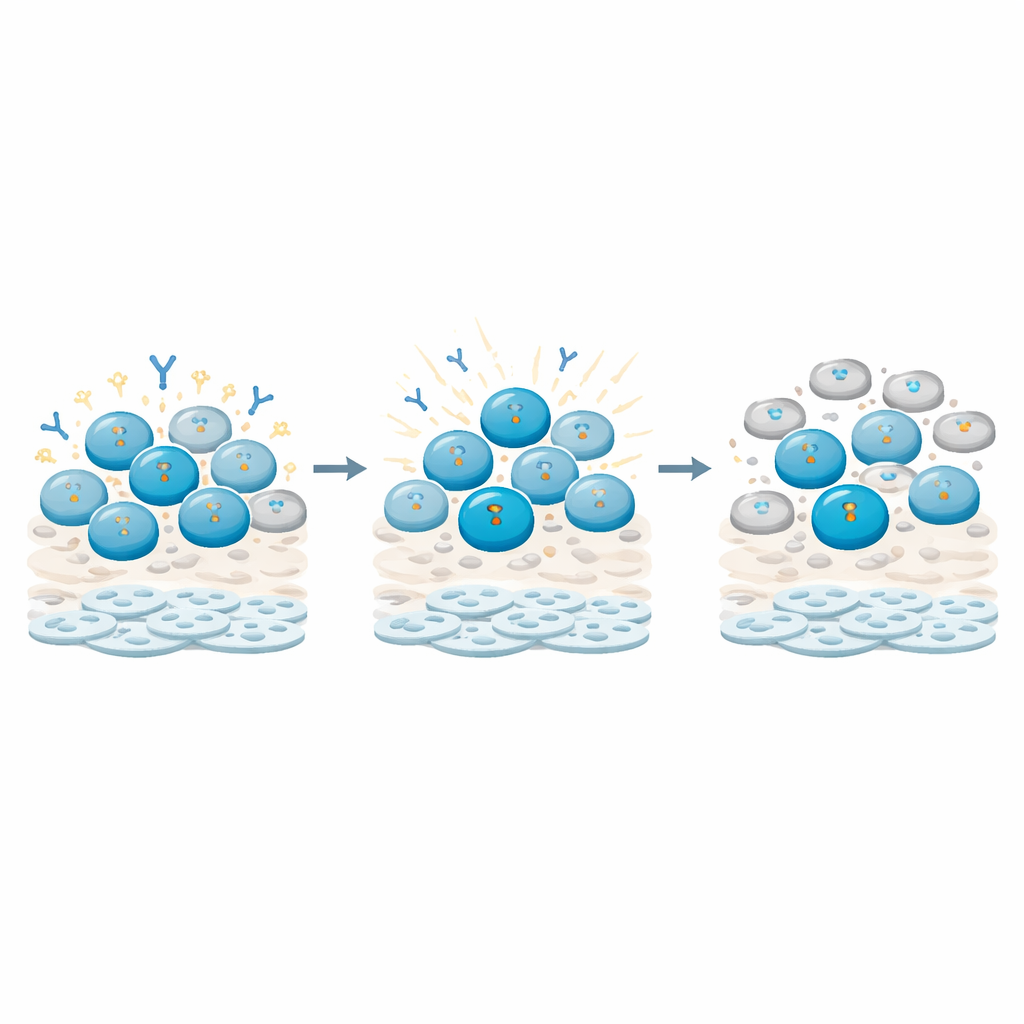
Jak limfocyty B wykrywają uszkodzenie i wprowadzają hamulec
Pogłębiając analizę, badacze śledzili molekularne oznaki uszkodzeń DNA w różnych typach komórek odpornościowych. Stwierdzili, że limfocyty B, zwłaszcza komórki pamięci B (uczestniczki uprzednich kontaktów z antygenem), gromadziły szczególnie silne i długotrwałe sygnały uszkodzeń DNA w porównaniu z limfocytami T. Sygnały te wchodziły w mechanizmy kontrolne zatrzymujące cykl komórkowy limfocytów B, utrzymując je w stanie spoczynku zamiast w aktywnej fazie podziału i różnicowania. Jednocześnie aktywność genów związanych z produkcją przeciwciał i dojrzewaniem limfocytów B została przekształcona: niektóre główne regulatory oraz transkrypty łańcuchów przeciwciał wzrastały lub malały w wzorcach sugerujących, że komórki zostały utrzymane w stanie „najpierw naprawa, potem funkcja”. Limfocyty T wykazywały natomiast bardziej przejściowe odpowiedzi i w dużej mierze odzyskiwały zdolność cykliczną.
Nowe spojrzenie na łagodniejsze terapie autoimmunologiczne
Podsumowując, badanie pokazuje, że pojedynczy, niskopoziomowy impuls uszkodzeń DNA może selektywnie uciszyć programy limfocytów B w środowisku przypominającym staw zapalny, pozostawiając przy tym większość limfocytów T i komórek wyściółki stawu nienaruszonych. Zamiast niszczyć limfocyty B, podejście to wprawia je w stan kontroli, w którym przestają wydzielać molekuły prozapalne i przeciwciała. Dla pacjentów pomysł ten pozostaje na razie teoretyczny, ale sugeruje, że precyzyjnie dawkowane, krótkotrwałe ekspozycje na promieniowanie lub leki genotoksyczne mogłyby pewnego dnia służyć nie tylko do zabijania komórek, lecz tymczasowego wyciszania tych najbardziej problematycznych. Takie strategie mogłyby uzupełniać istniejące terapie i — w zasadzie — dawać sposób na ujarzmienie przewlekłego zapalenia autoimmunologicznego przy mniejszych skutkach ubocznych dla układu odpornościowego.
Cytowanie: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Słowa kluczowe: reumatoidalne zapalenie stawów, limfocyty B, uszkodzenie DNA, modulacja odporności, choroba autoimmunologiczna