Clear Sky Science · ru
Сублетальная ДНК-повреждающая нагрузка выключает эффекторные программы В-клеток в со-культуре RA-FLS-PBMC
Уменьшение чрезмерно активного иммунного ответа
Ревматоидный артрит отчасти вызван иммунными клетками, которые атакуют собственные суставы, вызывая боль, отёк и длительное повреждение. Многие существующие препараты действуют, уничтожая целые группы иммунных клеток, что делает пациентов более уязвимыми к инфекциям. В этом исследовании рассматривается более тонкая идея: может ли крошечная, тщательно контролируемая доза повреждения ДНК временно выключить вредную активность определённых иммунных клеток — прежде всего В-клеток — не убивая при этом большинство из них. Если подход сработает, он может указать путь к более мягким методам лечения, которые успокаивают болезнь, сохраняя при этом большую часть иммунной системы.
Почему В-клетки — особая уязвимость
В-клетки известны прежде всего как производители антител, но при ревматоидном артрите они также поддерживают воспаление и организуют иммунные «очаги» внутри сустава. Чтобы отшлифовать антитела, которые они вырабатывают, активированные В-клетки намеренно разрезают и переписывают свою ДНК. Такое необычное поведение делает их более чувствительными к дополнительным повреждениям, чем многие другие клетки. Исследователи предположили, что небольшое дополнительное «подталкивание» в виде повреждения ДНК, ниже порога массовой гибели клеток, может использовать эту уязвимость и выборочно притушить активность В-клеток. При этом они стремились избежать широкого отравления иммунных клеток или повреждения структурных клеток, образующих выстилку сустава.
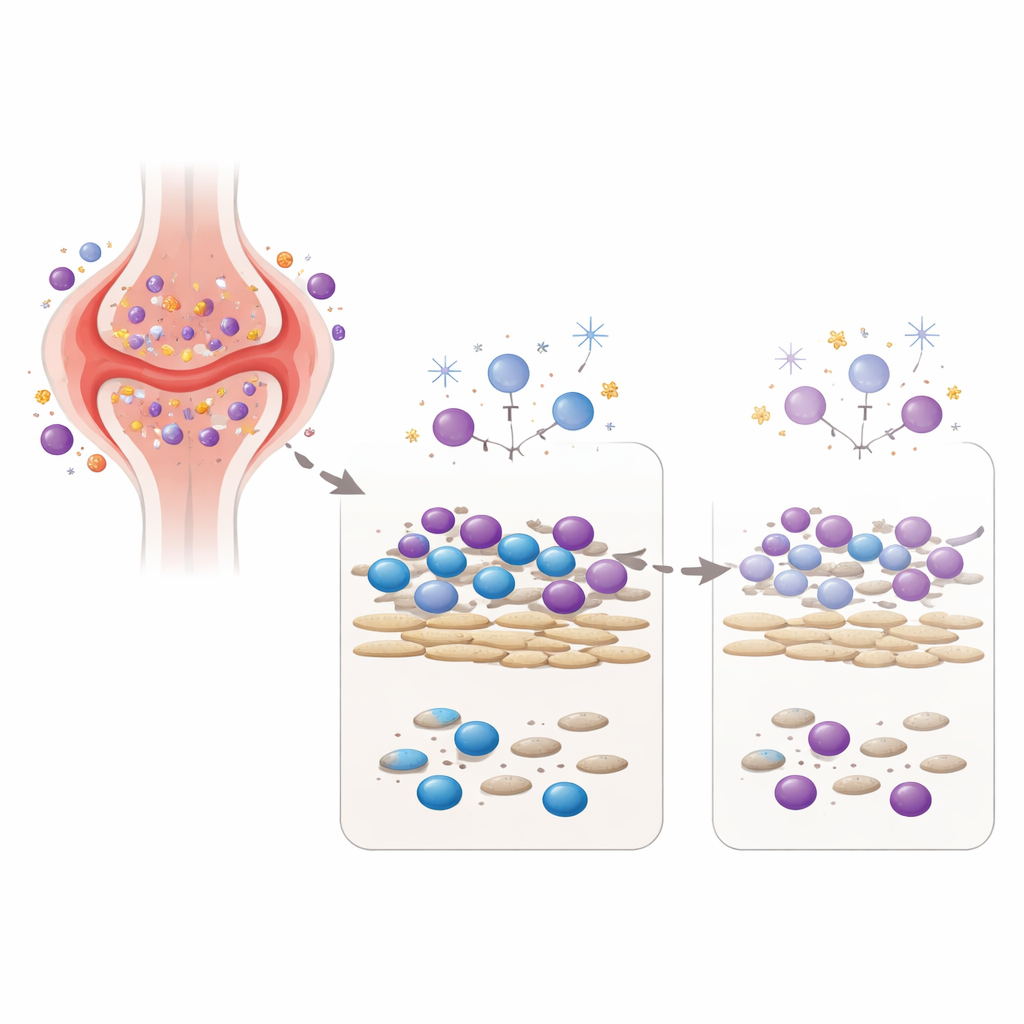
Воссоздание артритического сустава в чашке Петри
Чтобы проверить эту концепцию, команда создала лабораторную модель, объединяющую двух ключевых участников сустава: фибробластоподобные синовиоциты — клетки соединительной ткани от пациентов с ревматоидным артритом, и иммунные клетки крови от здоровых добровольцев. В этой со-культуре фибробласты обеспечивают сигналы, которые поддерживают иммунные клетки живыми и активными, напоминая среду внутри воспалённого сустава. Исследователи затем подвергали эту смешанную популяцию клеток одному заранее выбранному дозированию трёх различных генотоксичных агентов: низкодозовой гамма-облучению, перекиси водорода (реактивный кислородный вид, также встречающийся в воспалённой ткани) и метаболиту лекарства, связанного с циклофосфамидом — химиотерапевтическим средством, применяемым при тяжёлых аутоиммунных заболеваниях. Они измеряли не только выживаемость клеток, но и количество антител и цитокинов — иммунных мессенджеров — которые клетки продуцировали спустя несколько дней.
Выключение функции без массовой потери клеток
Во всех трёх случаях проявился явный паттерн: функции В-клеток сильно снижались при дозах, при которых большая часть клеток оставалась живой. Например, после умеренной дозы гамма-облучения общая выживаемость клеток оставалась выше 80 процентов, однако ключевые сигналы, такие как противовоспалительный цитокин IL-10 и несколько типов антител, падали примерно вдвое или больше. Перекись водорода и метаболит химиопрепарата показали схожее или даже более выраженное подавление продукции антител и цитокинов, иногда при том, что более двух третей клеток оставались жизнеспособными. Другими словами, генотоксическое «поражение» разъединило иммунную активность и выживание клеток — клетки были в наличии, но их способность подпитывать воспаление была резко снижена.
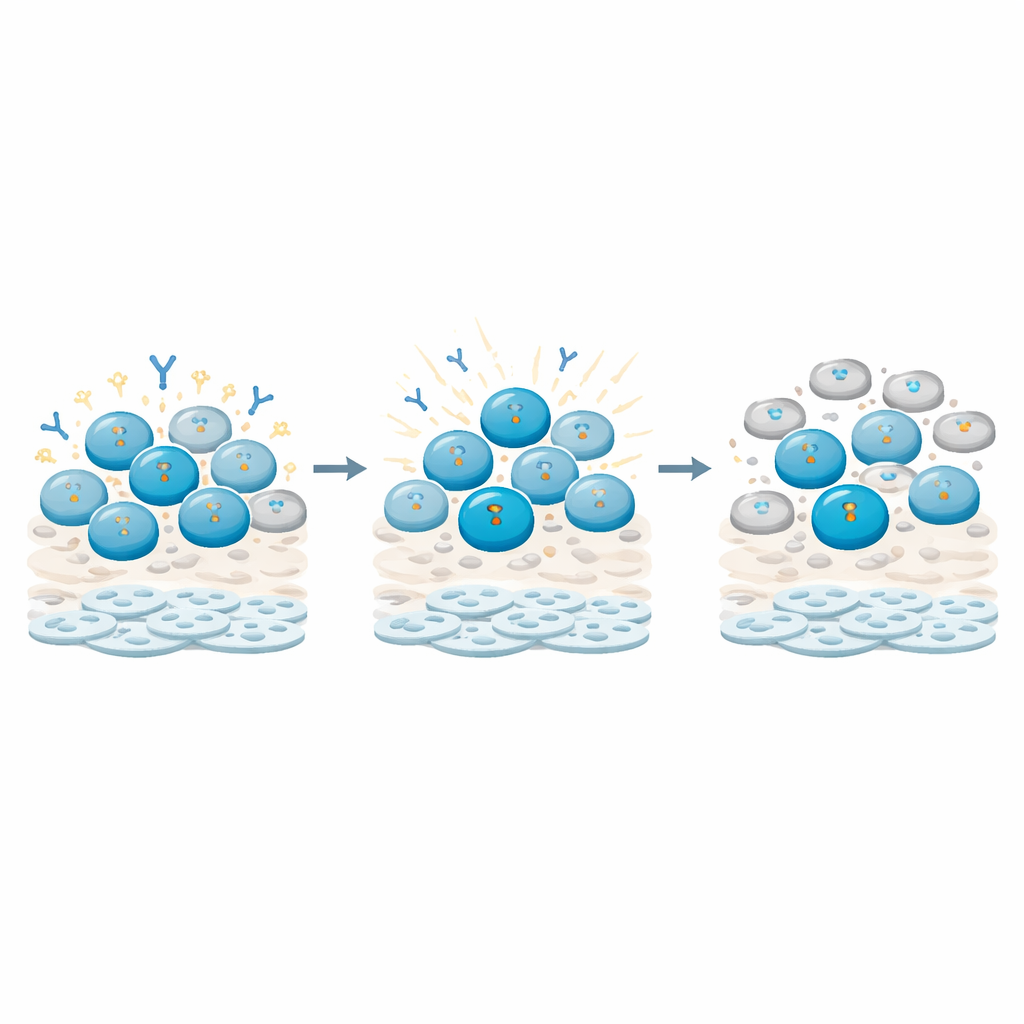
Как В-клетки улавливают повреждение и нажимают тормоза
Углубляясь в механизм, исследователи отслеживали молекулярные признаки повреждения ДНК в разных типах иммунных клеток. Они обнаружили, что В-клетки, особенно клетки памяти (те, что были подготовлены прежними встречами с антигеном), накапливали особенно сильные и стойкие признаки повреждения ДНК по сравнению с Т-клетками. Эти сигналы активировали контрольные точки, которые останавливали клеточный цикл В-клеток, удерживая их в фазе покоя вместо активного деления и дифференцировки. Одновременно активность генов, связанных с продукцией антител и созреванием В-клеток, менялась: некоторые ключевые регуляторы и транскрипты цепей антител повышались или понижались в паттернах, указывающих на то, что клетки переводились в состояние «сначала ремонт, потом функция». Т-клетки, напротив, демонстрировали более транзиторные ответы и в значительной степени восстанавливали свой цикл.
Новый подход к более мягким аутоиммунным терапии
В целом исследование показывает, что однократный низкоуровневый всплеск повреждения ДНК может выборочно притупить программы В-клеток в среде, имитирующей артрит, при этом оставляя большинство Т-клеток и клеток выстилки сустава невредимыми. Вместо уничтожения В-клеток этот подход подтолкнул их в состояние контрольной точки, где они перестают продуцировать воспалительные молекулы и антитела. Для пациентов идея остаётся теоретической, но она предполагает, что точно дозированные, кратковременные воздействия радиации или генотоксических препаратов однажды могут быть использованы не только для уничтожения клеток, но и для временного «отключения» наиболее проблемных из них. Такие стратегии могли бы дополнять существующие терапии и, по идее, предложить способ усмирить хроническое аутоиммунное воспаление с меньшим сопутствующим ущербом для иммунной системы.
Цитирование: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Ключевые слова: ревматоидный артрит, В-клетки, повреждение ДНК, модуляция иммунитета, аутоиммунное заболевание