Clear Sky Science · de
Subletale DNA-Schädigung schaltet B-Zell-Effektorprogramme in einer RA-FLS-PBMC-Kokultur aus
Eine überaktive Immunantwort herunterfahren
Rheumatoide Arthritis wird teilweise von Immunzellen angetrieben, die die eigenen Gelenke angreifen und so Schmerzen, Schwellungen und langfristige Schäden verursachen. Viele aktuelle Medikamente wirken, indem sie ganze Gruppen von Immunzellen ausschalten, wodurch Patienten anfälliger für Infektionen werden können. Diese Studie untersucht eine subtilere Idee: ob eine winzige, sorgfältig dosierte DNA-Schädigung die schädliche Aktivität bestimmter Immunzellen – insbesondere B-Zellen – vorübergehend abschalten kann, ohne die Mehrheit von ihnen tatsächlich abzutöten. Gelingt das, könnte dieser Ansatz auf schonendere Behandlungen hinweisen, die die Krankheit beruhigen, während ein Großteil des Immunsystems erhalten bleibt.
Warum B-Zellen eine besondere Verwundbarkeit haben
B-Zellen sind vor allem für die Produktion von Antikörpern bekannt, tragen aber bei rheumatoider Arthritis auch zur Aufrechterhaltung von Entzündungen und zur Organisation immunologischer „Hotspots“ im Gelenk bei. Um die von ihnen erzeugten Antikörper zu verfeinern, schneiden aktivierte B-Zellen absichtlich Teile ihrer eigenen DNA heraus und fügen sie wieder zusammen. Dieses ungewöhnliche Verhalten macht sie gegenüber zusätzlicher Schädigung empfindlicher als viele andere Zellen. Die Forschenden vermuteten, dass ein kleiner zusätzlicher „Anstoß“ von DNA-Schädigung, unterhalb der Schwelle für massenhaften Zelltod, diese Verwundbarkeit ausnutzen und die B-Zell-Aktivität selektiv dämpfen könnte. Gleichzeitig wollten sie eine breit angelegte Vergiftung von Immunzellen oder Schäden an den strukturellen Zellen der Gelenkschleimhaut vermeiden.
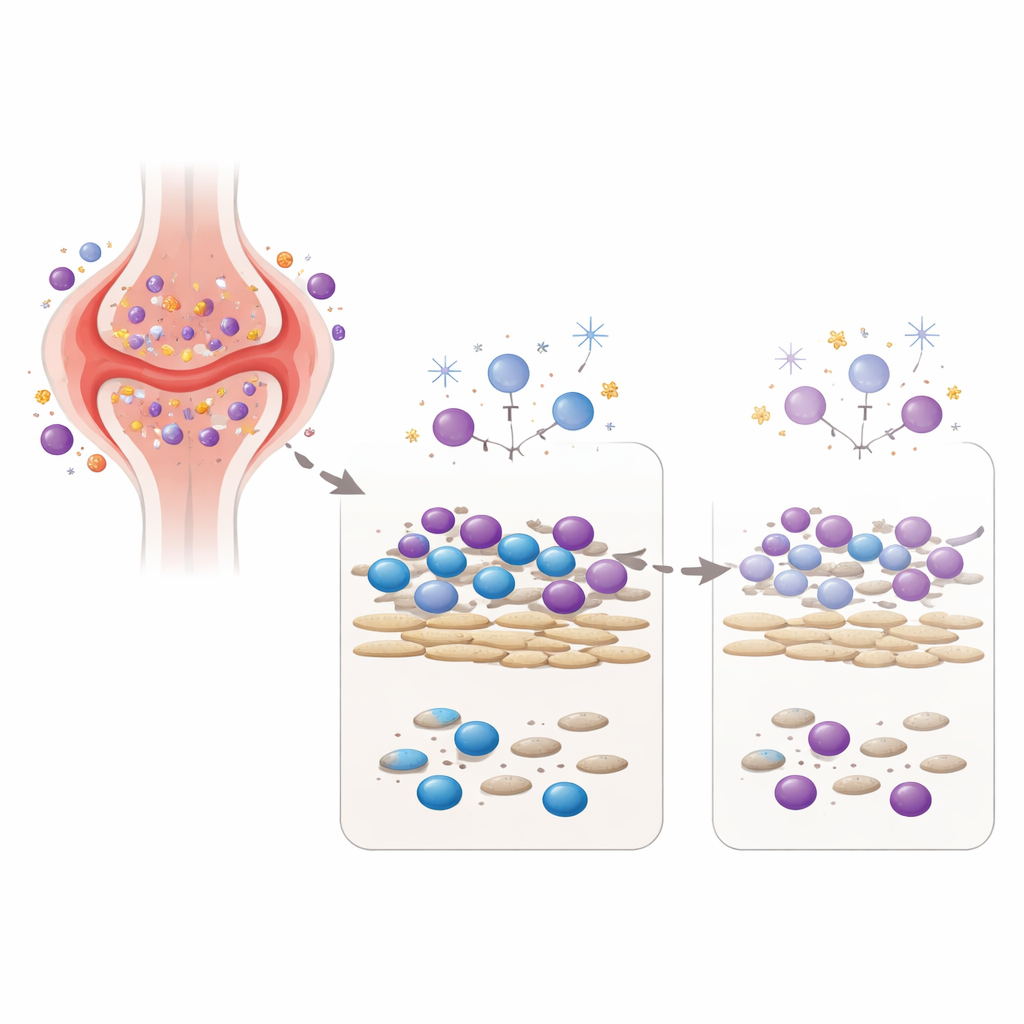
Das arthritische Gelenk in der Schale nachbilden
Um das Konzept zu testen, richtete das Team ein Labor-Modell ein, das zwei zentrale Akteure aus dem Gelenk zusammenbringt: fibroblastenähnliche Synoviozyten, also Bindegewebszellen von Patient:innen mit rheumatoider Arthritis, und Blut-Immunzellen gesunder Freiwilliger. In dieser Kokultur liefern die Fibroblasten Signale, die Immunzellen am Leben und aktiv halten – ähnlich der Umgebung in einem entzündeten Gelenk. Die Forschenden setzten diese gemischte Zellgemeinschaft dann einer einmaligen, sorgfältig gewählten Dosis von drei verschiedenen DNA-schädigenden Agenzien aus: niedrig dosierter Gamma-Bestrahlung, Wasserstoffperoxid (eine reaktive Sauerstoffspezies, die auch in entzündetem Gewebe vorkommt) und einem Arzneistoffmetaboliten, der mit Cyclophosphamid verwandt ist, einem Chemotherapeutikum, das in schweren Autoimmunerkrankungen eingesetzt wird. Sie maßen nicht nur, wie viele Zellen überlebten, sondern auch, wie viel Antikörper und Zytokine – immunologische Botenstoffe – die Zellen Tage später produzierten.
Funktionen ausschalten ohne massiven Zelltod
Bei allen drei Agenzien zeigte sich ein klares Muster: Die Funktionen der B-Zellen wurden stark reduziert bei Dosen, die die Mehrheit der Zellen am Leben ließen. Nach einer moderaten Dosis Gamma-Bestrahlung blieb beispielsweise das Gesamtaberleben über 80 Prozent, gleichzeitig sanken jedoch zentrale Signale wie das antiinflammatorische Zytokin IL-10 und mehrere Antikörpertypen um grob die Hälfte oder mehr. Wasserstoffperoxid und der Chemotherapie-Metabolit zeigten ähnliche oder sogar stärkere Dämpfungen der Antikörper- und Zytokinproduktion, teils während noch mehr als zwei Drittel der Zellen lebensfähig waren. Anders gesagt entkoppelte der genotoxische „Schlag“ die immunologische Aktivität vom Zellüberleben – Zellen waren vorhanden, aber ihre Fähigkeit, die Entzündung anzutreiben, war deutlich herabgesetzt.
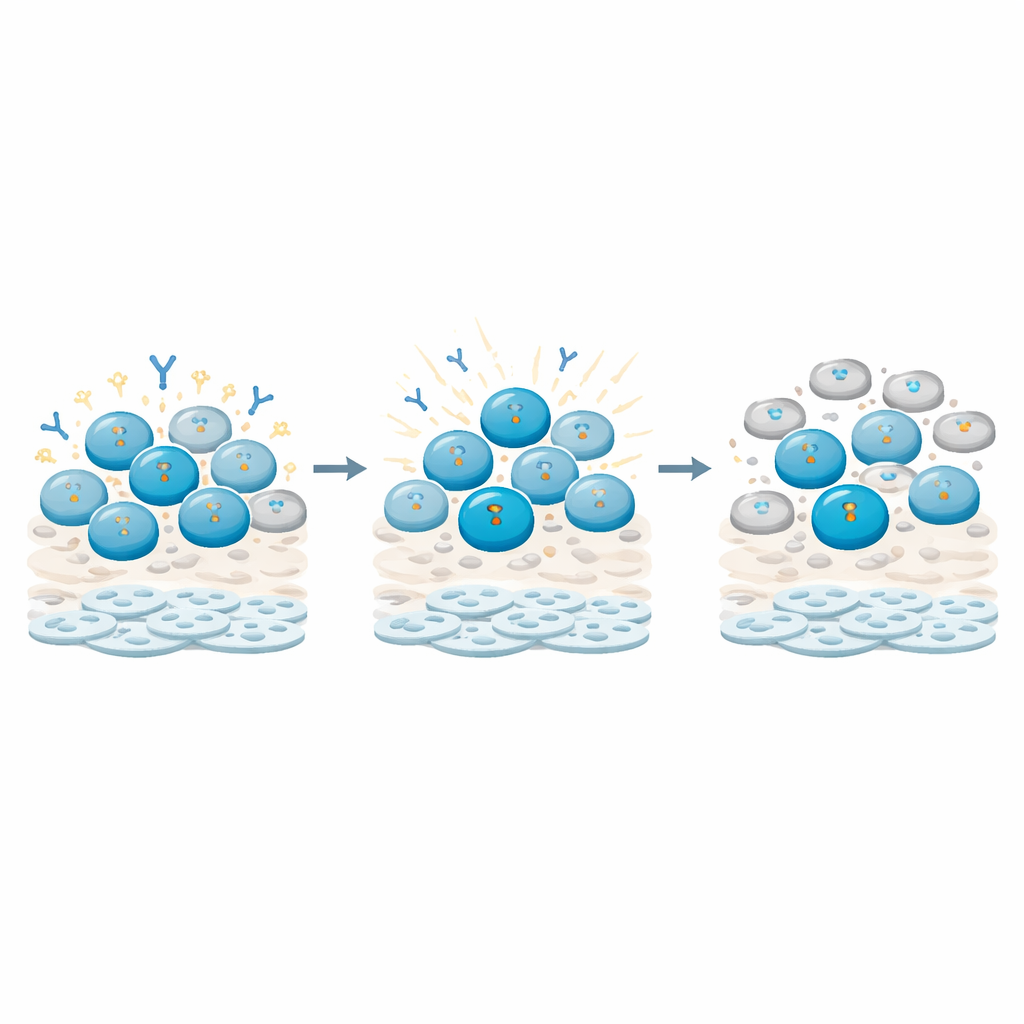
Wie B-Zellen Schäden wahrnehmen und die Bremse ziehen
Bei genaueren Untersuchungen verfolgten die Forschenden molekulare Zeichen von DNA-Schädigung in verschiedenen Immunzelltypen. Sie fanden, dass B-Zellen, insbesondere Gedächtnis-B-Zellen (also solche, die durch frühere Begegnungen vorgeprimt wurden), besonders starke und anhaltende Signale für DNA-Schäden im Vergleich zu T-Zellen akkumulierten. Diese Signale flossen in Kontrollpunkte ein, die den Zellzyklus der B-Zellen anhielten und sie in einer Ruhephase festhielten, statt sie aktiv teilen und differenzieren zu lassen. Gleichzeitig wurde die Genaktivität, die mit Antikörperproduktion und B-Zell-Reifung verknüpft ist, umgestaltet: Einige Masterregulatoren und Antikörperketten-Transkripte stiegen oder fielen in Mustern, die nahelegen, dass die Zellen in einem „zuerst reparieren, später funktionieren“-Zustand gehalten wurden. T-Zellen zeigten dagegen eher vorübergehende Reaktionen und erholten weitgehend ihr Teilungsverhalten.
Ein neuer Ansatz für sanftere Autoimmuntherapien
Insgesamt zeigt die Studie, dass eine einmalige, niedrig dosierte DNA-Schädigung selektiv B-Zell-Programme in einer arthritisähnlichen Umgebung stilllegen kann, während die meisten T-Zellen und die gelenkbeschichtenden Zellen intakt bleiben. Anstatt B-Zellen zu vernichten, bringt dieser Ansatz sie in einen Kontrollpunktzustand, in dem sie aufhören, entzündungsfördernde Moleküle und Antikörper auszustoßen. Für Patient:innen bleibt die Idee theoretisch, aber sie deutet darauf hin, dass präzise abgestimmte, kurzzeitige Expositionen gegenüber Strahlung oder genotoxischen Medikamenten eines Tages nicht nur zum Abtöten von Zellen genutzt werden könnten, sondern auch, um die störendsten Zellen vorübergehend zu stummschalten. Solche Strategien könnten bestehende Therapien ergänzen und prinzipiell einen Weg bieten, chronische autoimmune Entzündungen mit weniger Kollateralschäden am Immunsystem zu zähmen.
Zitation: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Schlüsselwörter: rheumatoide arthritis, B-Zellen, DNA-Schädigung, Immunmodulation, Autoimmunerkrankung