Clear Sky Science · tr
Subletal DNA hasarı RA-FLS-PBMC ko-kültüründe B hücresi efektör programlarını kapatıyor
Aşırı Aktif Bir İmmün Yanıtı Sakinleştirmek
Romatoid artrit, kısmen vücudun kendi eklemlerine saldıran bağışıklık hücrelerinin neden olduğu; ağrı, şişlik ve uzun vadeli hasara yol açan bir hastalıktır. Mevcut birçok ilaç, bağışıklık hücrelerinin geniş gruplarını yok ederek çalışır; bu da hastaları enfeksiyonlara karşı savunmasız bırakabilir. Bu çalışma, daha ince bir fikri araştırıyor: çok küçük, dikkatle kontrollü bir DNA hasarı dozunun, çoğu hücreyi öldürmeden belirli bağışıklık hücrelerinin —özellikle B hücrelerinin— zararlı aktivitelerini geçici olarak kapatıp kapatamayacağını. Başarılı olursa, bu yaklaşım hastalığı yatıştırırken bağışıklık sisteminin büyük bir bölümünü koruyan daha nazik tedavilere işaret edebilir.
Neden B Hücreleri Özel Bir Zayıf Nokta?
B hücreleri en çok antikor ürettikleriyle bilinir; ancak romatoid artritte inflamasyonu sürdürmeye ve eklem içinde bağışıklık “sıcak noktaları” oluşturmaya da yardımcı olurlar. Ürettikleri antikorları ince ayarlamak için aktive olmuş B hücreleri kasıtlı olarak DNA’larını kesip yeniden birleştirirler. Bu alışılmadık davranış, onları birçok diğer hücreye göre ek hasara daha duyarlı kılar. Araştırmacılar, kitlesel hücre ölümüne yol açmayacak düzeyde küçük bir ek “dürtünün” bu kırılganlıktan yararlanarak B hücresi aktivitesini seçici olarak susturabileceği sonucuna vardı. Aynı zamanda, bağışıklık hücrelerini yaygın biçimde zehirlemekten veya eklem yüzeyini oluşturan yapısal hücrelere zarar vermekten kaçınmak istediler.
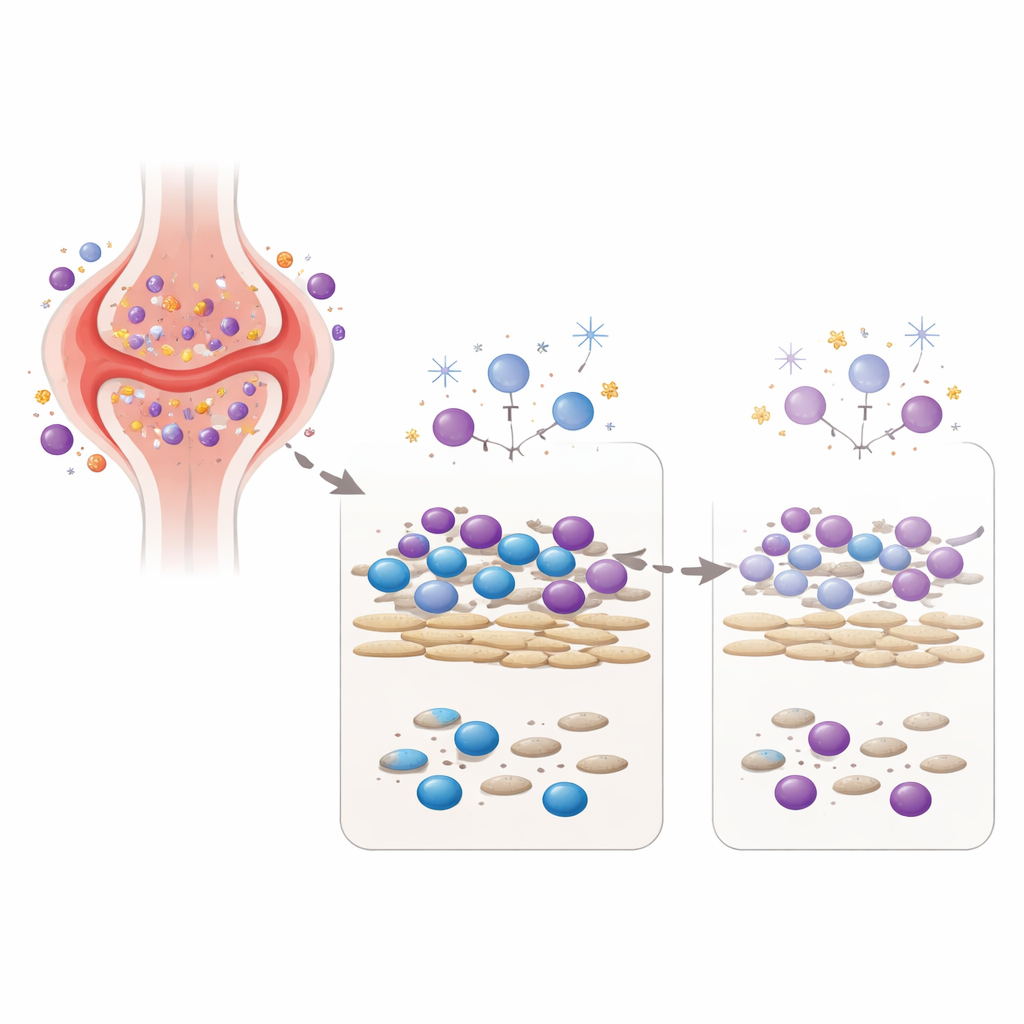
Artritik Eklem Ortamını Bir Plağa Yeniden Yaratmak
Bu kavramı test etmek için ekip, eklemden iki kilit oyuncuyu bir araya getiren bir laboratuvar modeli kurdu: romatoid artritli hastalardan alınan fibroblast benzeri sinoviositler (bağ dokusu hücreleri) ve sağlıklı gönüllülerden alınan kan immün hücreleri. Bu ko-kültürde, fibroblastlar iltihaplı bir eklem içindeki ortama benzer şekilde bağışıklık hücrelerini hayatta ve aktif tutan sinyaller sağlar. Araştırmacılar daha sonra bu karışık hücre topluluğunu üç farklı DNA hasar verici ajanın tek, dikkatle seçilmiş bir dozuna maruz bıraktı: düşük doz gama ışınlaması, hidrojen peroksit (iltihaplı dokuda bulunan reaktif oksijen türlerinden biri) ve siklofosfamide ilişkili bir ilaç metaboliti (şiddetli otoimmün hastalıklarda kullanılan bir kemoterapi). Sadece kaç hücrenin hayatta kaldığını değil, aynı zamanda günler sonra hücrelerin ne kadar antikor ve sitokin —bağışıklık haberci molekülleri— ürettiğini de ölçtüler.
Kitlesel Hücre Kaybı Olmadan Fonksiyonu Kapatmak
Üç ajanın tümünde belirgin bir desen ortaya çıktı: B hücresi fonksiyonları, çoğu hücre hayatta kalmış dozlarda güçlü biçimde azaldı. Örneğin, mütevazı bir gama ışınlaması dozundan sonra genel hücre sağkalımı %80’in üzerinde kaldı, ancak IL-10 gibi anti-inflamatuar sitokinler ve birkaç antikor türü yaklaşık yarı veya daha fazla azaldı. Hidrojen peroksit ve kemoterapi metaboliti, antikor ve sitokin üretiminde benzer veya daha güçlü bir sönümlenme gösterdi; bazen hücrelerin üçte ikisinden fazlası hâlâ canlıyken bile. Başka bir deyişle, genotoksik “vuruş” bağışıklık aktivitesini hücre hayatta kalımından ayırdı — hücreler vardı, ancak inflamasyonu besleme yetenekleri keskin biçimde azaltıldı.
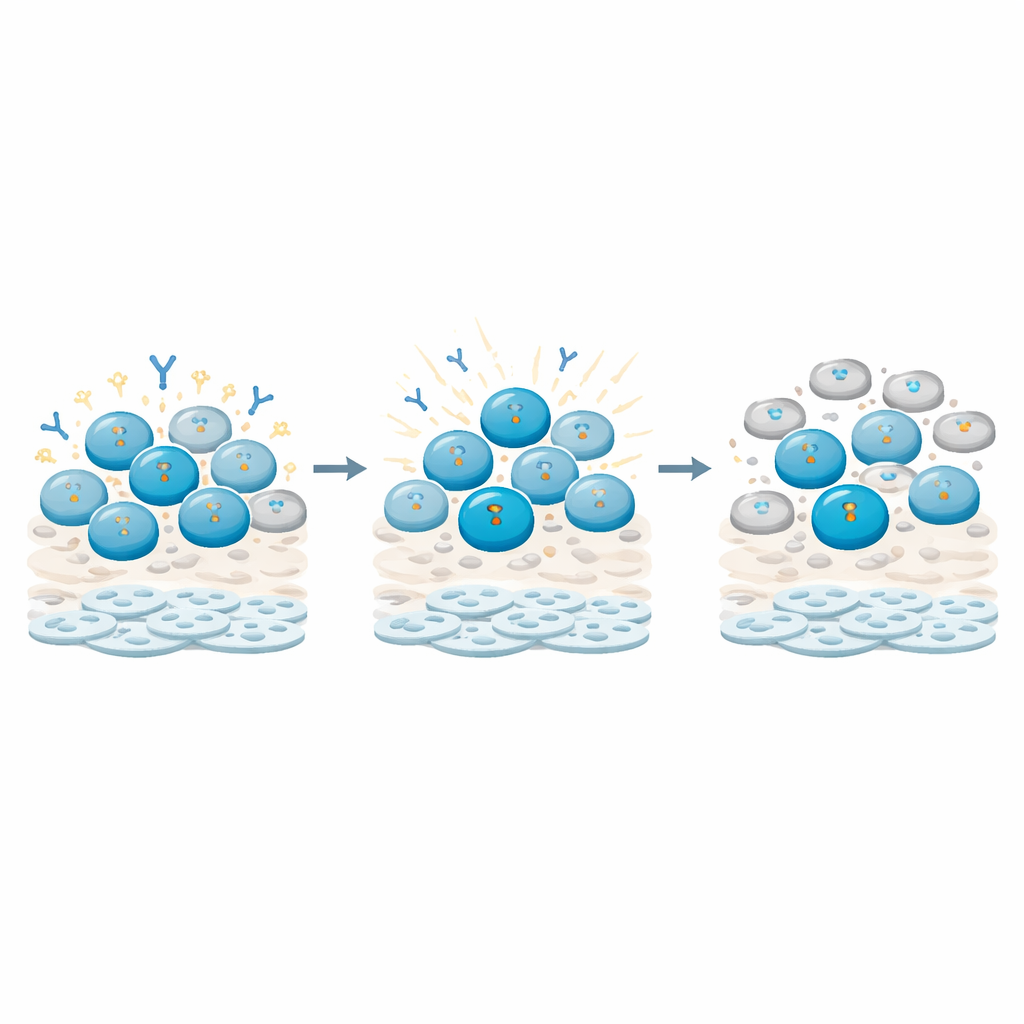
B Hücreleri Hasarı Nasıl Algılıyor ve Frenleri Nasıl Çekileiyor?
Daha derine inerek, araştırmacılar farklı immün hücre tipleri içinde DNA hasarının moleküler işaretlerini izlediler. B hücrelerinin, özellikle bellek B hücrelerinin (geçmiş karşılaşmalarla primlenmiş olanlar), T hücrelerine kıyasla özellikle güçlü ve kalıcı DNA hasarı işaretleri biriktirdiğini buldular. Bu işaretler, B hücrelerinin hücre döngüsünü durduran kontrol noktalarına bilgi verdi; böylece hücreler aktif bölünüp farklılaşmak yerine dinlenme fazında takılı kaldı. Aynı zamanda antikor üretimi ve B hücresi olgunlaşmasıyla ilgili gen etkinliği yeniden şekillendi: bazı ana düzenleyiciler ve antikor zinciri transkriptleri, hücrelerin “önce onar, sonra işlev” durumunda tutulduğunu işaret eden şekillerde yükseldi ya da düştü. Karşıt olarak T hücreleri daha geçici tepkiler gösterdi ve büyük ölçüde döngüsel davranışlarını geri kazandı.
Daha Yumuşak Otoimmün Terapilere Yeni Bir Bakış Açısı
Genel olarak çalışma, tek seferlik, düşük seviyeli bir DNA hasarı patlamasının artrit benzeri bir ortamda B hücresi programlarını seçici olarak susturabileceğini, aynı zamanda çoğu T hücresi ve eklem döşeyici hücreleri sağlam bırakabileceğini gösteriyor. B hücrelerini yok etmek yerine, bu yaklaşım onları iltihaplayıcı moleküller ve antikor üretimini durduracak bir kontrol noktası durumuna itiyor. Hastalar için bu fikir şimdilik teorik kalıyor, ancak hassas ayarlanmış, kısa süreli radyasyon veya genotoksik ilaç maruziyetlerinin bir gün sadece hücreleri öldürmek için değil, en sorunlu hücreleri geçici olarak sessize almak için de kullanılabileceğini öne sürüyor. Bu tür stratejiler mevcut terapileri tamamlayabilir ve prensipte bağışıklık sistemine daha az zarar vererek kronik otoimmün inflamasyonu yatıştırmanın bir yolunu sunabilir.
Atıf: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
Anahtar kelimeler: romatoid artrit, B hücreleri, DNA hasarı, bağışıklık modülasyonu, otoimmün hastalık