Clear Sky Science · he
נזקי DNA תת-קטלניים מכבים תוכניות אפקטור של תאי B בקו-תרבית RA-FLS-PBMC
הורדת תגובה חיסונית פעילה מדי
דלקת מפרקים שגרונית מונעת בחלקה על ידי תאים חיסוניים התוקפים את המפרקים של הגוף, וגורמים לכאב, נפיחות ונזק ארוך טווח. רבים מהתרופות הקיימות פועלות על ידי השמדת קבוצות שלמות של תאים חיסוניים, מה שעלול לחשוף את המטופלים לזיהומים. המחקר הזה בוחן רעיון עדין יותר: האם מנת נזקי DNA זעירה ומבוקרת יכולה לכבות זמנית את פעילותם המזיקה של תאים חיסוניים מסוימים — ובעיקר תאי B — ללא השמדה רחבה של רובם. אם כן, גישה זו עשויה להצביע על טיפולים עדינים יותר המרגיעים את המחלה תוך שמירה על רוב מערכת החיסון.
מדוע תאי B הם נקודה רגישה מיוחדת
תאי B ידועים בעיקר בייצור נוגדנים, אך בדלקת מפרקים שגרונית הם גם מסייעים לשמר דלקת ומארגנים “מוקדי חיסון” בתוך המפרק. כדי לכוונן את הנוגדנים שהם מייצרים, תאי B מופעלים מבצעים בכוונה שבירות ויתקונים של ה-DNA שלהם. התנהגות יוצאת דופן זו הופכת אותם לרגישים יותר לנזקים נוספים לעומת תאים רבים אחרים. החוקרים הסיקו שמנה קטנה נוספת של נזקי DNA, מתחת לסף שגורם למות תאים המוני, עלולה לנצל פגיעות זו ולשכך באופן סלקטיבי את פעילות תאי B. במקביל רצו להימנע מהרעלה כללית של תאים חיסוניים או מפגיעה בתאים המבניים שמרכיבים את רירית המפרק.
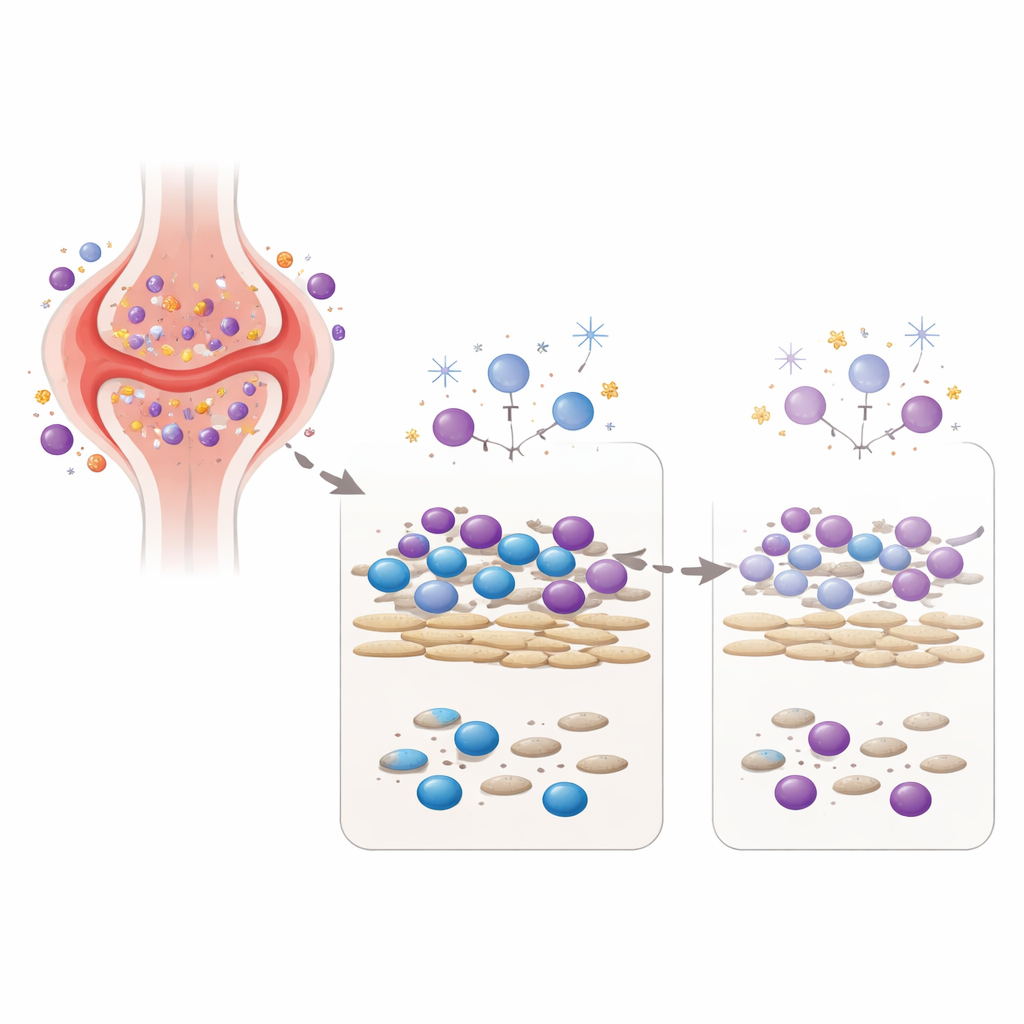
שחזור המפרק הארטריטי בצלוחית
כדי לבחון את הרעיון, הצוות הקים מודל מעבדה שמפגיש שחקנים מרכזיים מהמפרק: תאי פיברובלסט-דמויי סינוביווציטים, שהם תאי חיבור ממטופלים עם דלקת מפרקים שגרונית, ותאי דם חיסוניים ממתנדבים בריאים. בקו-תרבית זו, הפיברובלסטים מספקים אותות המשמרים את התאים החיסוניים בחיים ובמצב פעיל, בדמיון לסביבה בתוך מפרק מודלק. החוקרים חשפו את הקהילה התאית המעורבת למנה אחת ומותאמת היטב של שלושה גורמי נזקי DNA שונים: קרינת גאמא במינון נמוך, מי חמצן (מודל של סוגי חמצון הנמצאים ברקמה דלקתית), ומטבוליט של תרופת כימותרפיה הקשורה לציקלופוספאמיד, הנמצאת בשימוש במחלות אוטואימוניות חמורות. הם מדדו לא רק כמה תאים שרדו, אלא גם כמה נוגדנים וציטוקינים — מוליכי אות חיסוניים — התאים ייצרו ימים לאחר החשיפה.
כיבוי פונקציה ללא אובדן תאים המוני
בכל שלושת הסוכנים נראתה דפוס ברור: פונקציות תאי B הופחתו בקרבה רבה במינונים שעדיין השאירו את רוב התאים בחיים. למשל, לאחר מנת קרינת גאמא מתונה שרידות התאים הכוללת נותרה מעל 80 אחוז, אך אותות מרכזיים כמו הציטוקין נוגד הדלקת IL-10 וכמה סוגי נוגדנים ירדו בכ-50% או יותר. מי חמצן ומטבוליט הכימותרפיה הראו דיכוי דומה ואפילו חזק יותר בייצור נוגדנים וציטוקינים, לפעמים בעוד יותר משני שלישים מהתאים עדיין היו כשירים. במילים אחרות, ה״מכה״ הגנטוטוקסית ניתקה את הפעילות החיסונית ממצב שרידות התאים — התאים נוכחים, אך יכולתם להניע דלקת הועמעה באופן חד.
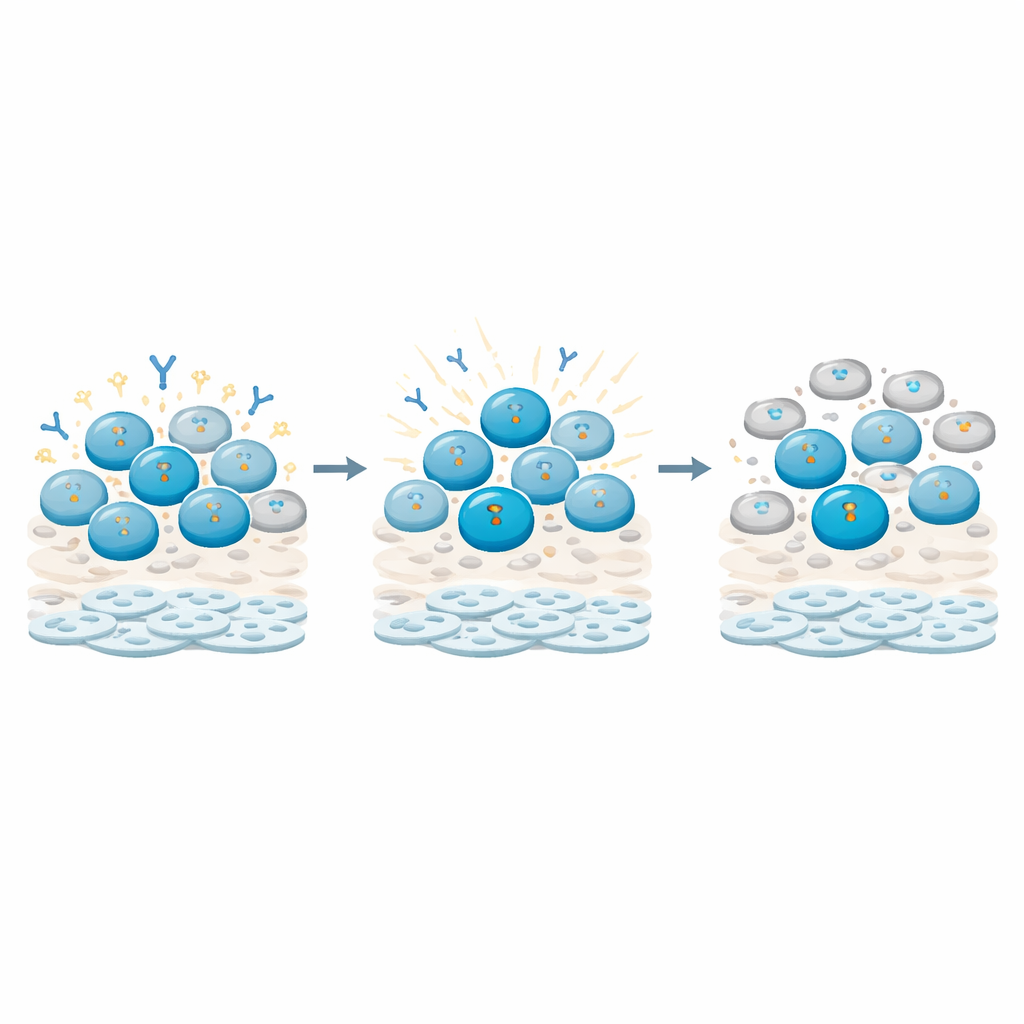
כיצד תאי B חשים את הנזק ולוחצים על הבלמים
בחינת המנגנונים הראתה שהחוקרים עקבו אחרי סימנים מולקולריים של נזקי DNA בתאי חיסון שונים. הם מצאו שתאי B, ובמיוחד תאי B זכרוניים (אלה המוכנים ממפגשים קודמים), הצטברו עם אותות נזק חזקים ומתמשכים יותר בהשוואה לתאי T. אותות אלה הובילו לתחנות בדיקה שעצרו את מחזור התא של תאי B, והשאירו אותם תקועים בשלב מנוחה במקום להתחלק ולהתמיין. במקביל, פעילות גנים הקשורה לייצור נוגדנים ולהבשלה של תאי B השתנתה: כמה רגולטורים מרכזיים וטרנסקריפטים של שרשראות נוגדן עלו או ירדו בדפוסים שמרמזים שהתאים מוחזקים במצב של "תיקון קודם, פונקציה מאוחר יותר". תאי T, לעומת זאת, הראו תגובות יותר חולפות ושיקמו ברובם את יכולת המחזור שלהם.
זווית חדשה על טיפולים רכים יותר באוטואימוניות
בסך הכל, המחקר מראה שמנה בודדת ברמת נמוכה של נזקי DNA יכולה לשתק באופן סלקטיבי תוכניות של תאי B בסביבה דמוית דלקת מפרקים תוך השארת רוב תאי T ותאי רירית המפרק שלמים. במקום לשמד תאי B, הגישה דוחפת אותם למצב בדיקה שבו הם מפסיקים לשחרר מולקולות דלקת ונוגדנים. עבור מטופלים, הרעיון נשאר תיאורטי, אבל הוא מציע שאקספוזיציות קצרות ומדויקות לקרינה או לתרופות גנטוטוקסיות עשויות בעתיד לשמש לא רק להריגה של תאים, אלא כדי להחריש זמנית את אלו הבעייתיים ביותר. אסטרטגיות כאלה יכולות להשלים טיפולים קיימים ובהחלט להציע דרך לרסן דלקת אוטואימונית כרונית עם פחות נזק צדדי למערכת החיסון.
ציטוט: Bruci, D., Lowin, T., Fritz, G. et al. Sublethal DNA damage switches off B cell effector programs in an RA-FLS-PBMC co-culture. Cell Death Discov. 12, 161 (2026). https://doi.org/10.1038/s41420-026-03021-1
מילות מפתח: דלקת מפרקים שגרונית, תאי B, נזקי DNA, מודולציה חיסונית, מחלה אוטואימונית