Clear Sky Science · zh
将免疫原性细胞死亡纳入非小细胞肺癌治疗格局:利用免疫系统的力量
为什么让肿瘤学会向免疫系统报警很重要
肺癌仍然是全球最致命的癌症之一,主要原因在于肿瘤常常复发或对标准治疗产生耐药。本文探讨了一个有前景的思路:与其悄无声息地杀死癌细胞,不如让其以能明显提醒机体防御的方式死亡。通过将肿瘤破坏转变为一种内部疫苗的形式,被称为免疫原性细胞死亡的治疗可以帮助免疫系统识别、记忆并更有效地对抗非小细胞肺癌。
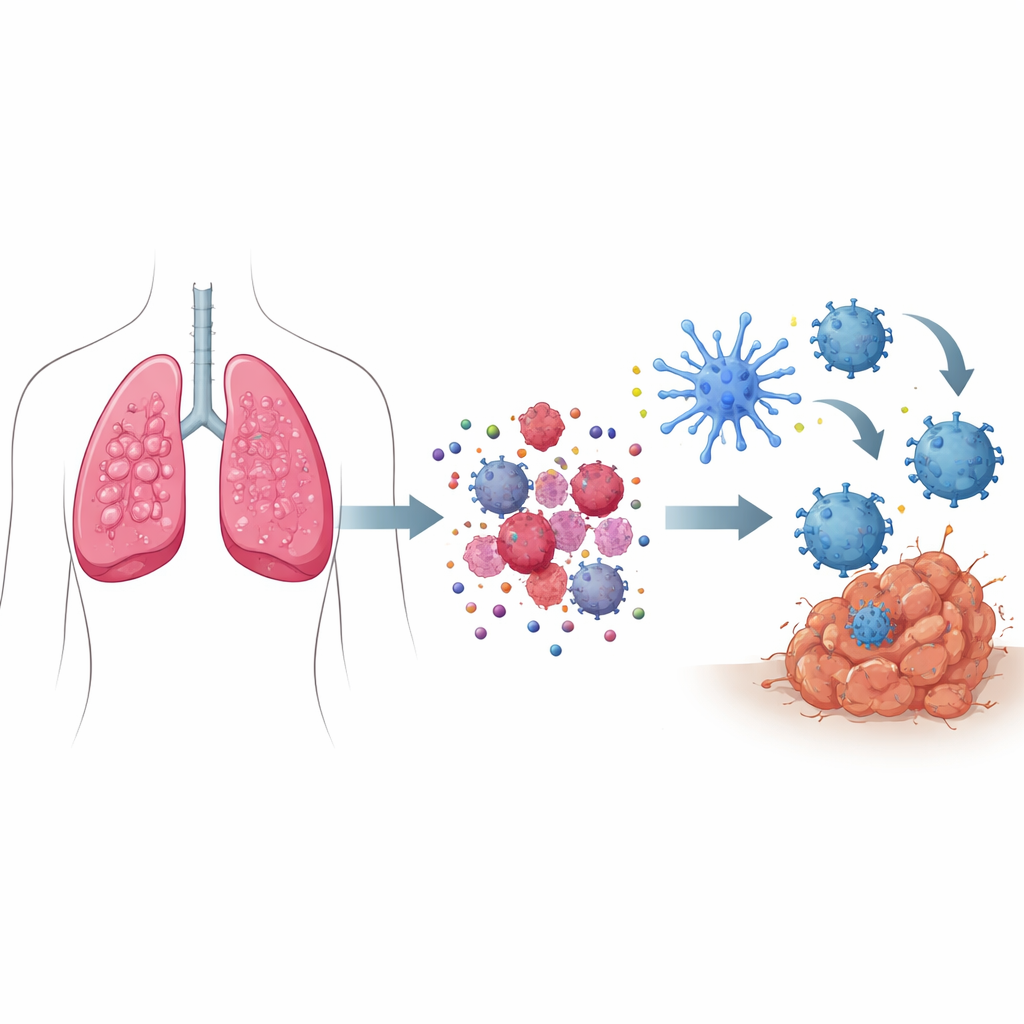
“危险信号”如何将细胞死亡变成求救呼号
当大多数细胞死亡时,通常是无声的,不会激起免疫反应。然而在免疫原性细胞死亡中,垂死的癌细胞会发出一套协调的危险信号。细胞内受压的成分将某些蛋白质推到细胞表面,将其标记为应被免疫哨兵“吞噬”的对象。与此同时,小分子如 ATP 漏出,像照明弹一样吸引免疫细胞聚集,其他蛋白则被释放出来充当警报。这些信号共同吸引并激活名为树突状细胞的专门侦察者,它们吞噬肿瘤碎片、加工处理后将肿瘤片段呈递给 T 细胞——训练它们在全身范围内寻找并摧毁癌细胞。
将常见治疗转变为免疫训练剂
许多常见的肺癌疗法在以合适方式使用时可诱导这种充满警报的细胞死亡。某些化疗药物,包括常用的紫杉类和铂类化合物,能使肿瘤细胞进入一种应激状态,进而释放危险信号。这些治疗不仅能直接缩小肿瘤,还能激发 T 细胞和有益的巨噬细胞发挥作用。更新的、更具针对性的化疗形式——抗体–药物偶联物,可以将毒性载荷精确输送至癌细胞。在早期研究中,这类靶向药物不仅更干净地杀死肿瘤,而且似乎能以更少的全身副作用激发更强的免疫反应。
放疗、靶向药物与光疗作为免疫协同者
放射治疗不仅仅是烧灼肿瘤;通过损伤 DNA 并在癌细胞内产生活性分子,它可以促使细胞走向免疫原性死亡。然而,其作用在很大程度上依赖剂量和时间安排:适度且时机良好的放疗能强烈刺激免疫,而过高剂量反而可能抑制关键的感知通路。研究者还在设计纳米颗粒以放大有利信号并抵消抑制性信号。与此同时,阻断 EGFR、ALK、AXL 或血管相关信号等生长驱动因子的精准药物如今被认识到具有双重作用:它们减缓肿瘤生长,并在许多模型中有助于揭露肿瘤物质和危险提示,从而唤醒 T 细胞。光激活疗法利用光敏化合物在肿瘤内产生一阵阵有毒氧化物种,可被调节以针对最能触发免疫可见性细胞死亡的细胞结构。
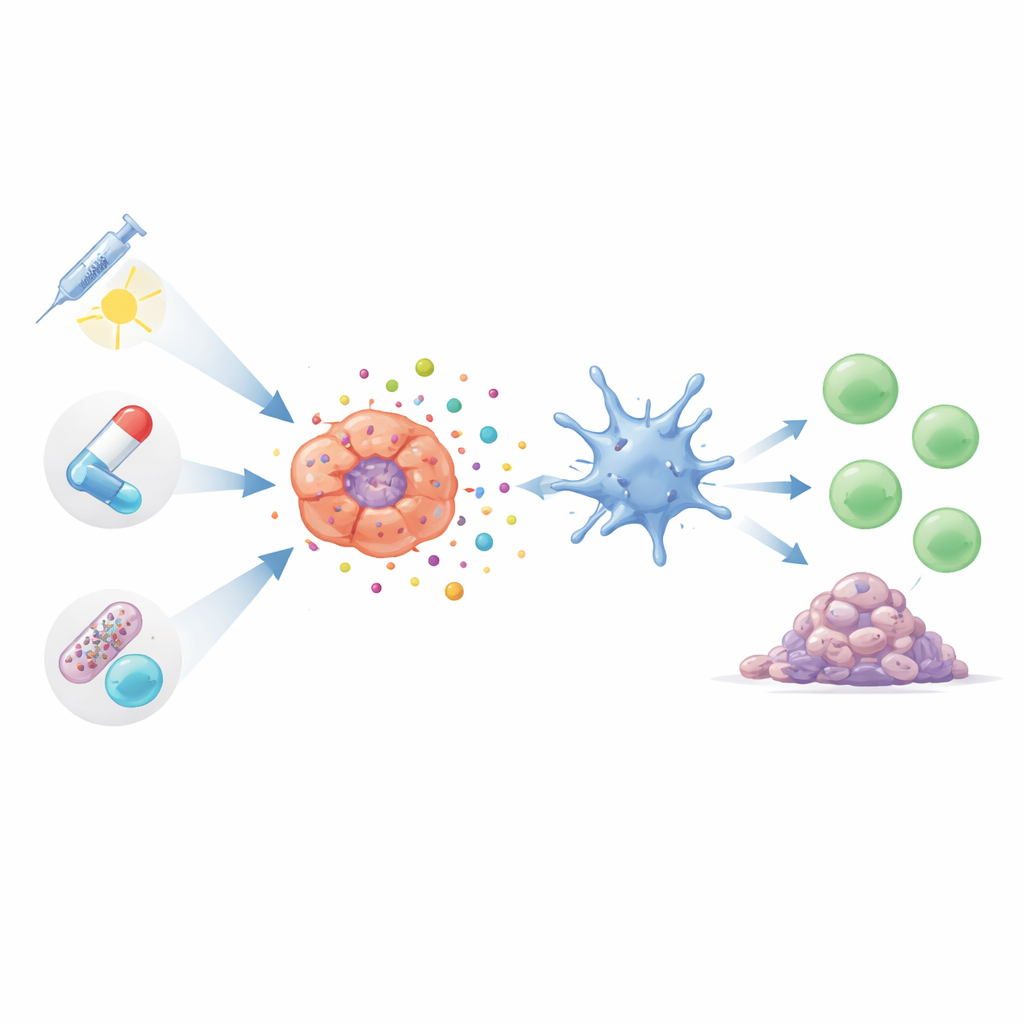
新兴手段:病毒、电场与肠道微生物组
除了传统的治疗支柱之外,若干新兴工具也依赖免疫原性细胞死亡。工程化病毒能选择性感染肺癌细胞并使其裂解,同时吸引免疫细胞,在实验模型中有时可导致远处未治疗肿瘤的退缩。低强度交变电场已在其他癌症中应用,能以释放危险信号并鼓励 T 细胞浸润的方式给肺癌细胞施加应激。甚至我们肠道内的细菌也可能影响这些由 ICD 驱动反应的强弱。某些肠道微生物似乎促进更活跃的抗肿瘤环境,而另一些则助长免疫抑制状态,可能削弱基于 ICD 的治疗收益。
这对未来肺癌护理意味着什么
本文的总体信息是:肿瘤细胞如何死亡与是否死亡同等重要。如果死亡具有免疫原性,每个被销毁的癌细胞都可以成为免疫系统的课程,帮助其识别并攻击残余癌细胞,并可能预防复发。要将这一点变为非小细胞肺癌患者的可行现实,研究者仍需找到明确的标志来判断患者体内是否发生了 ICD,优化剂量与疗法组合的匹配方式,以及制定对抗肿瘤多重逃逸机制的策略。如果这些挑战能够被克服,未来的治疗方案可能常规将诱导 ICD 的疗法与增强免疫的药物配对,把短暂的反应转化为对疾病更持久的控制。
引用: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
关键词: 免疫原性细胞死亡, 非小细胞肺癌, 癌症免疫疗法, 化放疗, 肿瘤微环境