Clear Sky Science · he
שילוב מוות תאי אימונוגני בנוף הטיפולי של סרטן הריאה שאינו תאי קטן: ניצול כוח המערכת החיסונית
מדוע חשוב ללמד גידולים להתריע בפני המערכת החיסונית
סרטן הריאה נותר אחד מהסרטן הקטלניים ביותר בעולם, וזאת במידה רבה מפני שלעיתים קרובות הגידולים חוזרים או עמידים לטיפולים המקובלים. מאמר זה בוחן רעיון מבטיח: במקום להרוג תאים סרטניים בשקט, ייתכן שאפשר לגרום להם למות באופן שמתריע בחוזקה בפני מנגנוני ההגנה של הגוף. על ידי הפיכת השמדת הגידול לסוג של חיסון פנימי, טיפול המכונה מוות תאי אימונוגני עשוי לסייע למערכת החיסון לזהות, לזכור וללחום ביתר יעילות בסרטן הריאה שאינו תאי קטן.
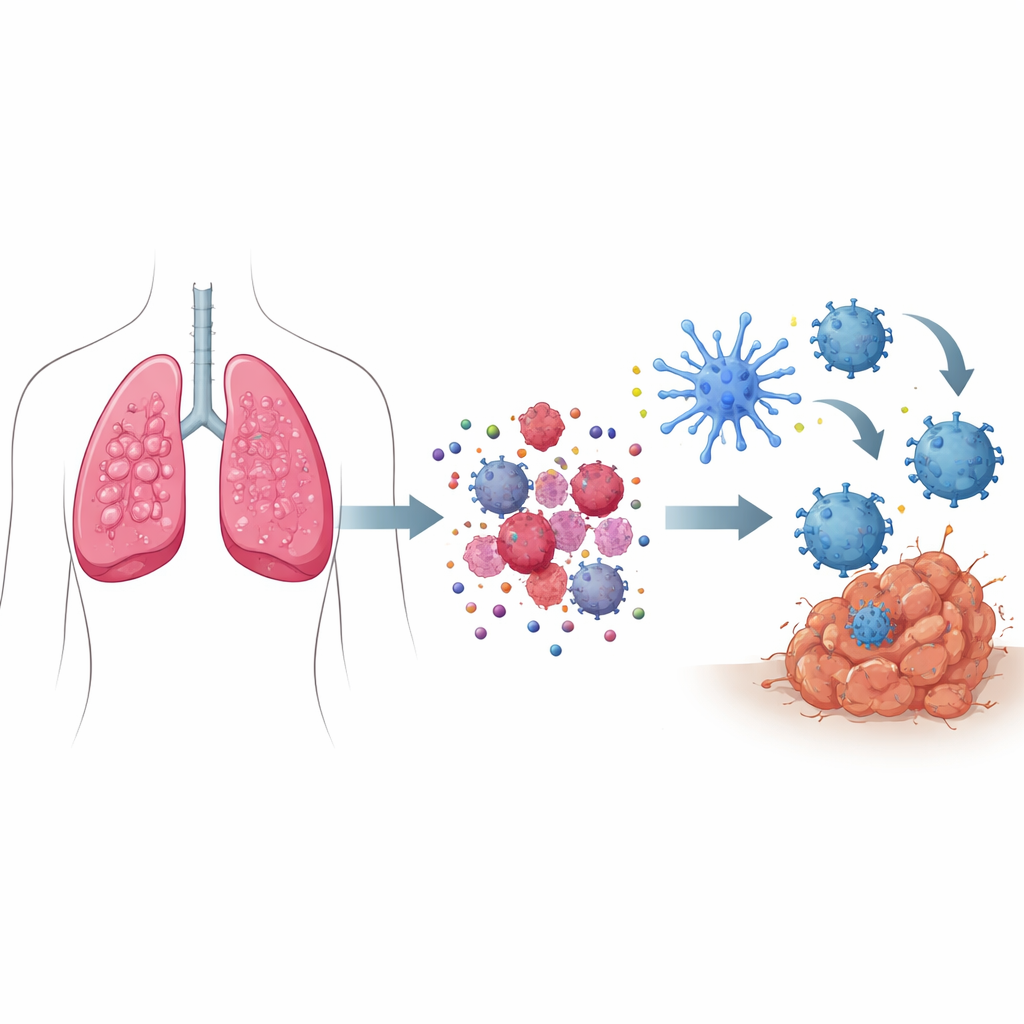
כיצד “אותות סכנה” הופכים מוות תאי לקריאת עזרה
כאשר רוב התאים מתים, הם עושים זאת בשקט, מבלי לעורר את המערכת החיסונית. במוות תאי אימונוגני, לעומת זאת, התאים המתים שולחים מערך מתואם של אותות סכנה. מרכיבים מותשים בתוך התא דוחפים חלבונים מסוימים אל פני השטח שלו, כיחסון המיועד להיאכל על‑ידי סוכנים חיסוניים. במקביל, מולקולות קטנות כמו ATP נדיפות החוצה, פועלות כמארבים שמושכים תאים חיסוניים לאזור, בעוד שחלבונים אחרים משוחררים ומתנהגים כתרעות. אותות אלה ביחד מושכים ומפעילים סיירים מיוחדים הנקראים תאים דנדריטיים, שסופגים חלקיקים של הגידול, מעבדים אותם ואז מציגים קטעי גידול לתאי T — ואימונים אלה גורמים להם לחפש ולהשמיד תאים סרטניים בכל הגוף.
הפיכת טיפולים מקובלים למאמני מערכת החיסון
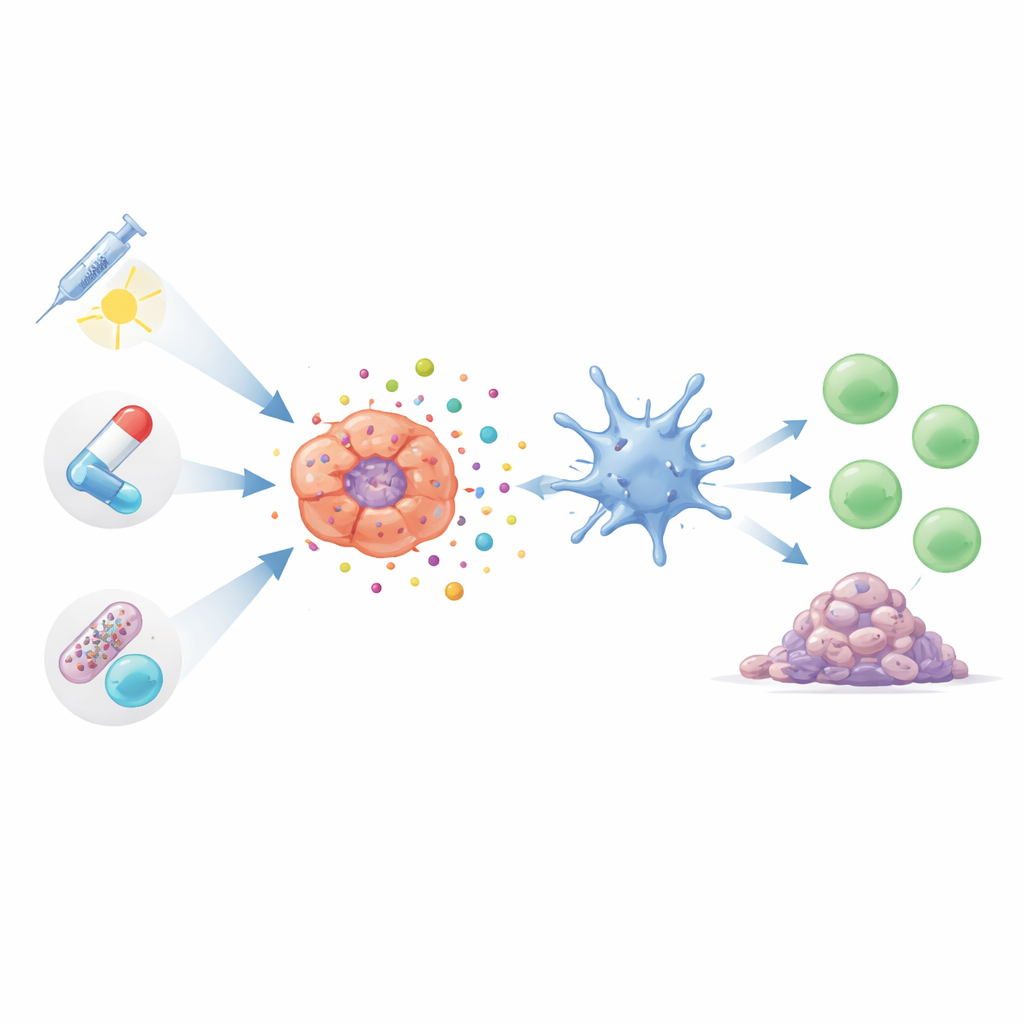
רבות מהתרופות המוכרות לטיפול בסרטן הריאה יכולות לעורר סוג של מוות תאי מלא בתרעות אם משתמשים בהן בדרך הנכונה. סוגים מסוימים של כימותרפיה, כולל טקסאנים ונוגדי מתכת לפלטינה בשימוש נרחב, יכולים לדחוף תאי גידול למצב של סטרס שמוביל לשחרור אותות סכנה. טיפולים אלה לא רק מצמצמים את הגידולים ישירות, אלא גם יכולים לעורר את תאי ה‑T והמקרופאגים התורמים לפעילות חיסונית. צורות חדשות וממוקדות יותר של כימותרפיה, המכונות קונזוגטים של נוגדן‑תרופה, מספקות מטענים רעילים בדיוק לתאים סרטניים. במחקרים ראשוניים, תרופות ממוקדות אלה לא רק הורגות גידולים בצורה נקייה יותר, אלא גם נראות כמציפות תגובות חיסוניות חזקות יותר עם תופעות לוואי סיסטמיות מופחתות.
קרינה, תרופות ממוקדות וטיפולים מבוססי אור כשותפים חיסוניים
הקרינה עושה יותר מאשר פשוט לקלות את הגידולים; בנזק שהיא גורמת ל‑DNA ובהיווצרות מולקולות פעילויות בתוך התאים הסרטניים, היא יכולה לדחוף אותם לעבר מוות אימונוגני. עם זאת, ההשפעה תלויה במידה רבה במנה ובלוח הזמנים: קרינה מתונה ומתוזמנת היטב יכולה לעורר תגובה חיסונית חזקה, בעוד שמנות גבוהות מדי עלולות לדכא מסלולים חושיים מרכזיים. חוקרים גם מעצבים ננו־חלקיקים שמגבירים את האותות המועילים ומנטרלים את האותות המדכאים. במקביל, תרופות מדויקות החוסמות מנועי גדילה כגון EGFR, ALK, AXL או אותות כלי הדם נתפסות כיום כבעלות תפקיד כפול: הן מאטות את התפשטות הגידול ובמקרים רבים מסייעות לחשוף חומרי גידול ואותות סכנה שמעירים את תאי ה‑T. טיפולים מונחי אור, המשתמשים בחומרים פוטו‑רגישים כדי ליצור פרצי סוגי חמצן רעילים בתוך הגידולים, ניתנים לכוונון כך שיפגעו במבנים תאיים שמעוררים בצורה היעילה ביותר מוות תאי גלוי למערכת החיסון.
שחקנים חדשים: וירוסים, שדות חשמליים והמיקרוביוטה של המעיים
מעבר לעמודי התווך הסטנדרטיים בטיפול בסרטן, כמה כלים מתפתחים גם הם נשענים על מוות תאי אימונוגני. וירוסים מהונדסים שזיהום סלקטיבי בתאי סרטן ריאה גורם להם להתפוצץ יכולים למשוך לתוכם תאים חיסוניים ולעתים להביא להצטמצמות של גידולים מרוחקים שלא טופלו במודלים ניסיוניים. שדות חשמליים מתחלפים בעוצמה נמוכה, שכבר נמצאו בשימוש בסוגי סרטן אחרים, הוצגו כגורמים לסטרס בתאי סרטן ריאה בצורה שמשחררת אותות סכנה ומעודדת חדירת תאי T. אפילו החיידקים החיים במעיים שלנו עשויים להשפיע על עוצמת התגובות המונעות‑על ידי ICD. מיקרובים מסוימים במעיים נראים כמעודדים סביבה אנטי‑גידולית פעילה יותר, בעוד אחרים מעודדים מצב מדכא חיסונית שיכול להחליש את היתרונות של טיפולים מבוססי ICD.
מה משמעות הדבר לטיפול העתידי בסרטן הריאה
המסר הכולל של המאמר הוא שלצורת מות התא חשיבות לא פחותה מהעובדה שהוא מת. אם המוות הוא אימונוגני, כל תא סרטני שנהרס יכול להפוך לשיעור עבור המערכת החיסונית, ולעזור לה לזהות ולהתקיף תאים סרטניים שנותרו ואולי למנוע הישנות. כדי שהרעיון יהפוך למציאות מעשית אצל אנשים עם סרטן ריאה שאינו תאי קטן, חוקרים עדיין זקוקים לסמנים ברורים שיגידו מתי ICD מתרחש אצל מטופלים, לשיטות טובות יותר להתאמת מינונים ושילובי טיפולים, ולאסטרטגיות נגד נתיבי הבריחה הרבים של הגידול. אם ניתן לענות על אתגרים אלה, תוכניות טיפול עתידיות עשויות לשלב באופן שגרתי טיפולים שמעוררים ICD עם תרופות המחזקות את המערכת החיסונית, ולהפוך תגובות קצרות טווח לשליטה מתמשכת במחלה.
ציטוט: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
מילות מפתח: מוות תאי אימונוגני, סרטן ריאה שאינו תאי קטן, אימונותרפיה לסרטן, כימורדיותרפיה, מיקרוסביבה של הגידול