Clear Sky Science · de
Integration des immunogenen Zelltods in die Behandlungslandschaft des nicht‑kleinzelligen Lungenkarzinoms: die Kraft des Immunsystems nutzen
Warum es wichtig ist, Tumoren beizubringen, das Immunsystem zu alarmieren
Lungenkrebs ist nach wie vor eine der tödlichsten Krebsarten weltweit, vor allem weil Tumoren häufig zurückkehren oder Standardtherapien widerstehen. Dieser Artikel untersucht eine vielversprechende Idee: Anstatt Krebszellen nur still zu töten, könnten Ärzte sie so zum Absterben bringen, dass sie die Abwehrkräfte lautstark alarmieren. Indem man die Tumorzerstörung in eine Art interne Impfung verwandelt, könnte eine Behandlung namens immunogener Zelltod dem Immunsystem helfen, das nicht‑kleinzellige Lungenkarzinom besser zu erkennen, sich daran zu erinnern und wirksamer zu bekämpfen.
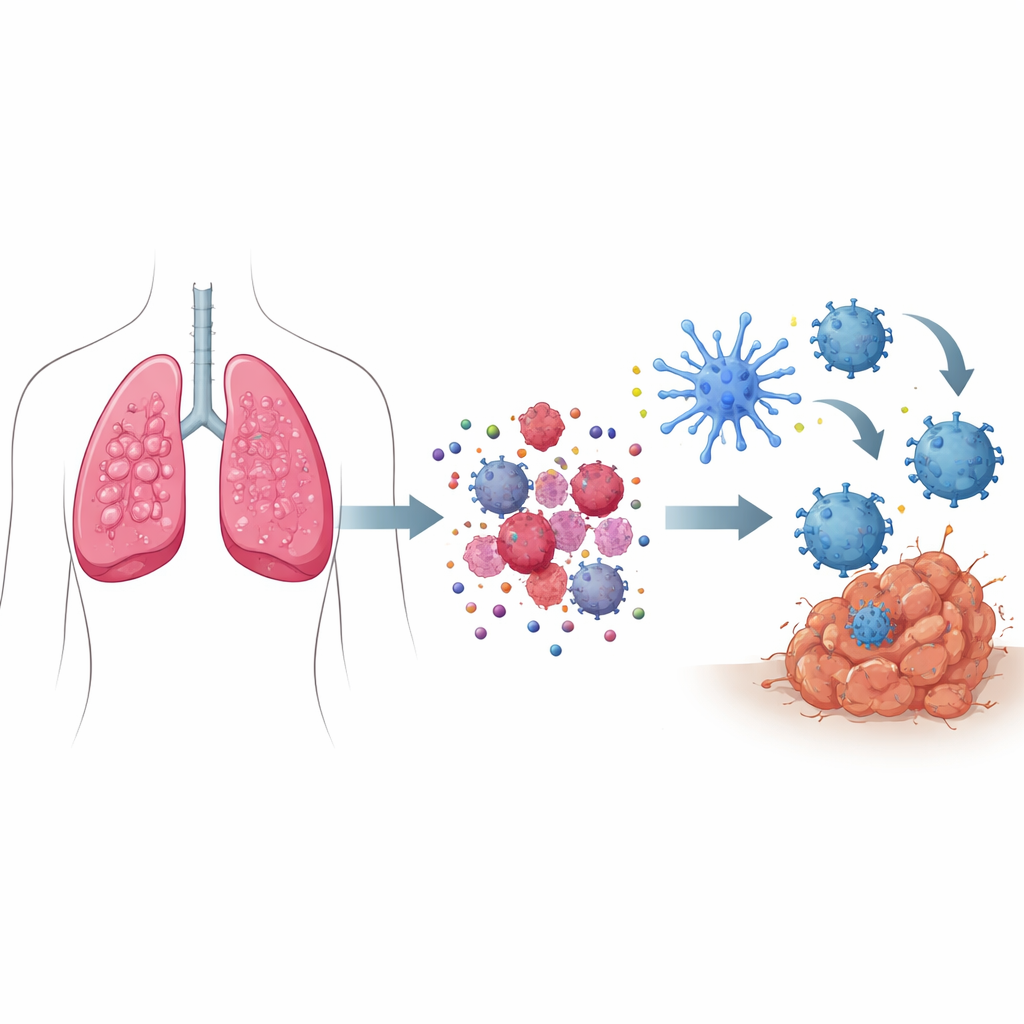
Wie „Gefahrensignale“ den Zelltod zum Hilferuf machen
Wenn die meisten Zellen sterben, geschieht dies still und ohne das Immunsystem zu rühren. Beim immunogenen Zelltod senden sterbende Krebszellen dagegen ein koordiniertes Set an Gefahrensignalen aus. Gestresste Zellbestandteile treiben bestimmte Proteine an die Zelloberfläche und markieren sie so als etwas, das von Immunaufklärern „gefressen“ werden soll. Gleichzeitig treten kleine Moleküle wie ATP aus und wirken wie Leuchtsignale, die Immunzellen anziehen, während andere Proteine freigesetzt werden, die wie Alarmsignale fungieren. Zusammen ziehen diese Signale spezialisierte Aufklärer an und aktivieren sie — die dendritischen Zellen —, die Tumorstücke aufnehmen, verarbeiten und dann Fragmente dem T‑Zell‑System präsentieren, wodurch T‑Zellen trainiert werden, Krebszellen im ganzen Körper zu suchen und zu zerstören.
Gewöhnliche Therapien als Immuntrainer nutzen
Viele vertraute Lungenkrebsbehandlungen können diese Art von alarmreichem Zelltod auslösen, wenn sie richtig angewendet werden. Bestimmte Chemotherapeutika, darunter weit verbreitete Taxane und Platinverbindungen, können Tumorzellen in einen gestressten Zustand treiben, der zur Freisetzung von Gefahrensignalen führt. Diese Therapien verkleinern Tumoren nicht nur direkt, sondern können auch T‑Zellen und hilfreiche Makrophagen in Aktion versetzen. Neuerere, gezieltere Formen der Chemotherapie, so genannte Antikörper‑Wirkstoff‑Konjugate, liefern toxische Wirkstoffe präzise an Krebszellen. In frühen Studien töten diese zielgerichteten Mittel Tumoren nicht nur sauberer ab, sondern scheinen auch stärkere Immunantworten mit geringeren systemischen Nebenwirkungen zu entfachen.
Strahlentherapie, zielgerichtete Medikamente und lichtbasierte Therapie als Immunpartner
Strahlentherapie tut mehr, als Tumoren zu verkohlen; durch DNA‑Schäden und die Erzeugung reaktiver Moleküle in Krebszellen kann sie diese in Richtung immunogenen Zelltods treiben. Der Effekt hängt jedoch stark von Dosis und Zeitplan ab: Moderat dosierte, gut terminierte Strahlung kann stark immunstimulierend wirken, während übermäßig hohe Dosen wichtige Erkennungswege dämpfen können. Forscher entwickeln zudem Nanopartikel, die hilfreiche Signale verstärken und unterdrückende Signale ausgleichen. Parallel dazu zeigen präzise Wirkstoffe, die Wachstumsfaktoren wie EGFR, ALK, AXL oder angiogene Signale blockieren, eine doppelte Wirkung: Sie verlangsamen das Tumorwachstum und helfen in vielen Modellen, Tumormaterial und Gefahrensignale freizulegen, die T‑Zellen wecken. Lichtaktivierte Therapien, die photosensitive Verbindungen nutzen, um kurzzeitig toxische Sauerstoffspezies in Tumoren zu erzeugen, lassen sich so abstimmen, dass sie zelluläre Strukturen gezielt treffen, die am effektivsten einen immunologisch sichtbaren Zelltod auslösen.
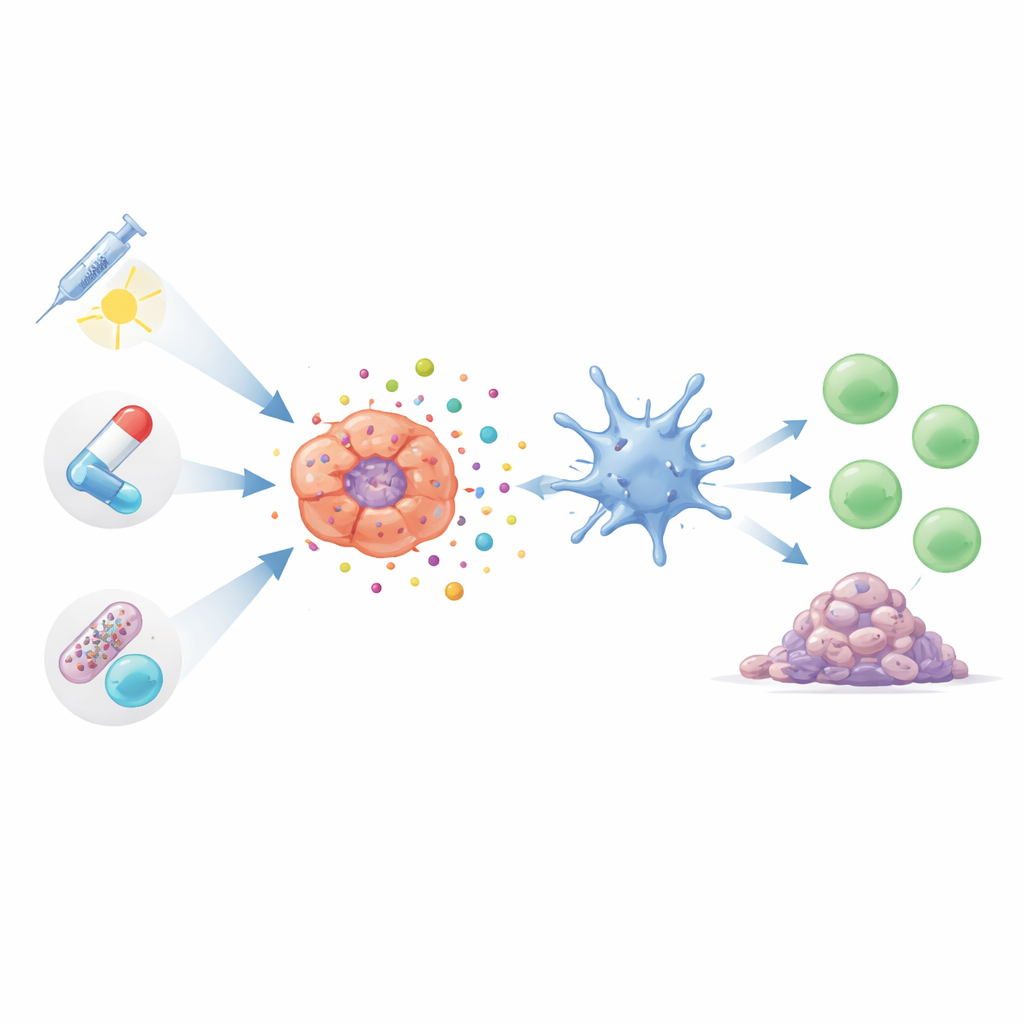
Neue Akteure: Viren, elektrische Felder und das Darmmikrobiom
Über die Standardpfeiler der Krebsbehandlung hinaus stützen sich mehrere neue Werkzeuge ebenfalls auf immunogenen Zelltod. Gezielt entwickelte Viren, die selektiv Lungenkrebszellen infizieren, bringen diese zum Aufplatzen und ziehen zugleich Immunzellen an, was in experimentellen Modellen manchmal zur Regression entfernter, unbehandelter Tumoren führt. Niedrigintensive Wechselstromfelder, die bereits bei anderen Krebsarten eingesetzt werden, haben gezeigt, dass sie Lungenkrebszellen so stressen, dass Gefahrensignale freigesetzt werden und T‑Zellen einwandern. Selbst die Bakterien in unserem Darm können beeinflussen, wie stark diese ICD‑vermittelten Reaktionen ausfallen. Bestimmte Darmmikroben scheinen ein aktiveres anti‑tumorales Umfeld zu fördern, während andere einen immundämpfenden Zustand begünstigen, der den Nutzen ICD‑basierter Therapien abschwächen könnte.
Was das für die zukünftige Behandlung von Lungenkrebs bedeutet
Die Kernaussage des Artikels lautet, dass die Art und Weise, wie eine Tumorzelle stirbt, genauso wichtig ist wie die Tatsache, dass sie stirbt. Wenn der Tod immunogen ist, kann jede zerstörte Krebszelle zur Lektion für das Immunsystem werden und ihm helfen, verbleibende Tumorzellen zu erkennen und anzugreifen und möglicherweise ein Wiederauftreten zu verhindern. Damit dies für Menschen mit nicht‑kleinzelligem Lungenkarzinom praktisch wird, brauchen Forscher noch verlässliche Marker, um ICD bei Patientinnen und Patienten nachzuweisen, bessere Wege, Dosen und Therapiekombinationen abzustimmen, sowie Strategien, um die zahlreichen Fluchtwege des Tumors zu kontern. Wenn diese Herausforderungen gemeistert werden, könnten zukünftige Behandlungspläne routinemäßig ICD‑induzierende Therapien mit immunstärkenden Medikamenten kombinieren und so kurzlebige Ansprechraten in eine länger anhaltende Kontrolle der Erkrankung verwandeln.
Zitation: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Schlüsselwörter: immunogener Zelltod, nicht‑kleinzelliges Lungenkarzinom, Krebsimmuntherapie, Chemo‑Radiotherapie, Tumormikroumgebung