Clear Sky Science · ru
Интеграция иммуногенного клеточного гибели в ландшафт лечения немелкоклеточного рака легкого: использование силы иммунной системы
Почему важно научить опухоли предупреждать иммунную систему
Рак легкого по‑прежнему остается одним из самых смертоносных онкологических заболеваний в мире, во многом потому, что опухоли часто рецидивируют или оказываются резистентными к стандартным методам лечения. В этой статье рассматривается многообещающая идея: вместо того чтобы просто тихо уничтожать раковые клетки, врачи могут заставить их умирать так, чтобы это громко сигнализировало защитным силам организма. Превратив гибель опухоли в нечто вроде внутренней вакцинации, подход под названием иммуногенная клеточная гибель (ИКГ) может помочь иммунной системе распознавать, запоминать и эффективнее бороться с немелкоклеточным раком легкого.
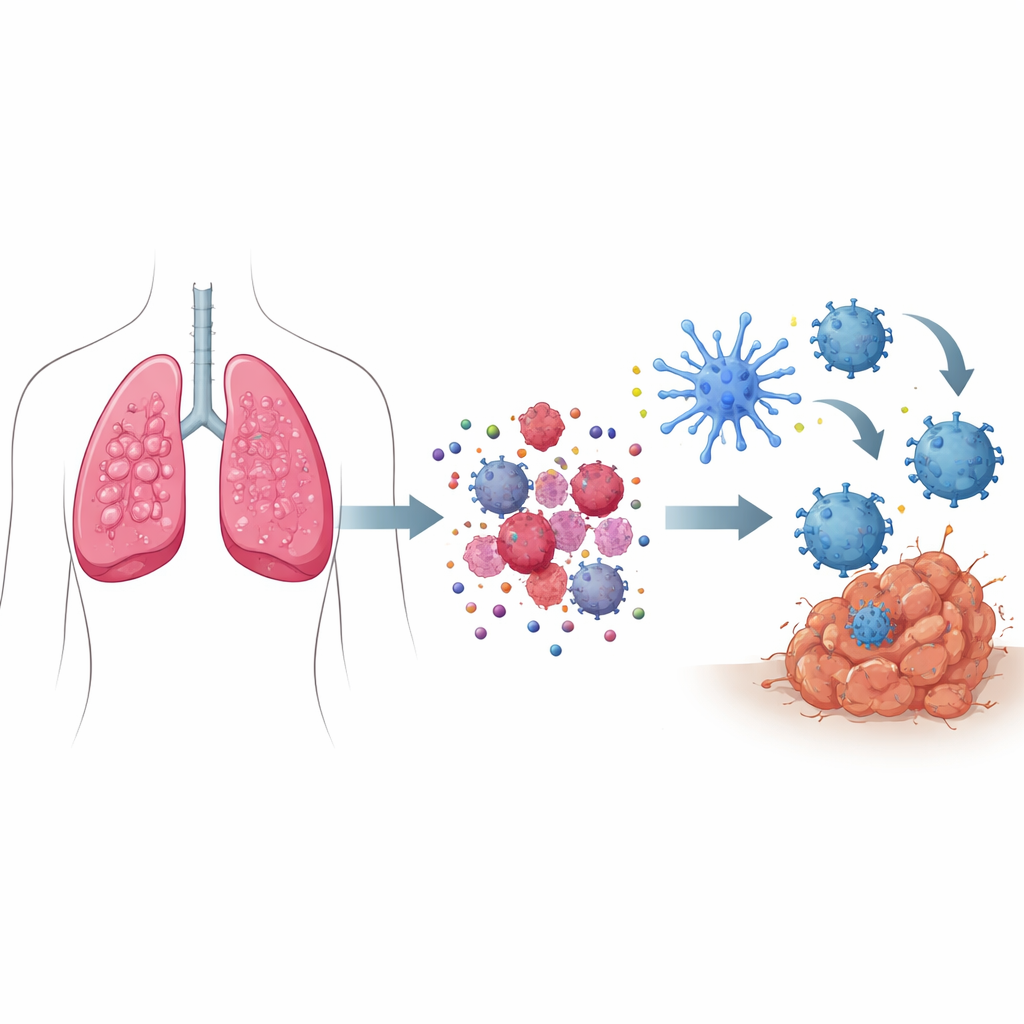
Как «сигналы опасности» превращают гибель клетки в призыв о помощи
Когда большинство клеток умирают, это происходит тихо, не привлекая внимания иммунитета. При иммуногенной клеточной гибели умирающие раковые клетки, напротив, посылают скоординированный набор сигналов опасности. Компоненты клетки в состоянии стресса выталкивают определенные белки на поверхность, отмечая клетку как пригодную для «поглощения» иммунными стражами. Одновременно небольшие молекулы, такие как АТФ, просачиваются наружу, действуя как сигнальные факелы, привлекающие иммунные клетки, а другие белки высвобождаются и ведут себя как тревожные сигналы. Вместе эти послания привлекают и активируют специализированных разведчиков — дендритные клетки, которые захватывают фрагменты опухоли, перерабатывают их и затем представляют фрагменты опухолевых антигенов Т‑клеткам, обучая их искать и уничтожать раковые клетки по всему организму.
Преобразование обычных методов лечения в «тренажеры» для иммунитета
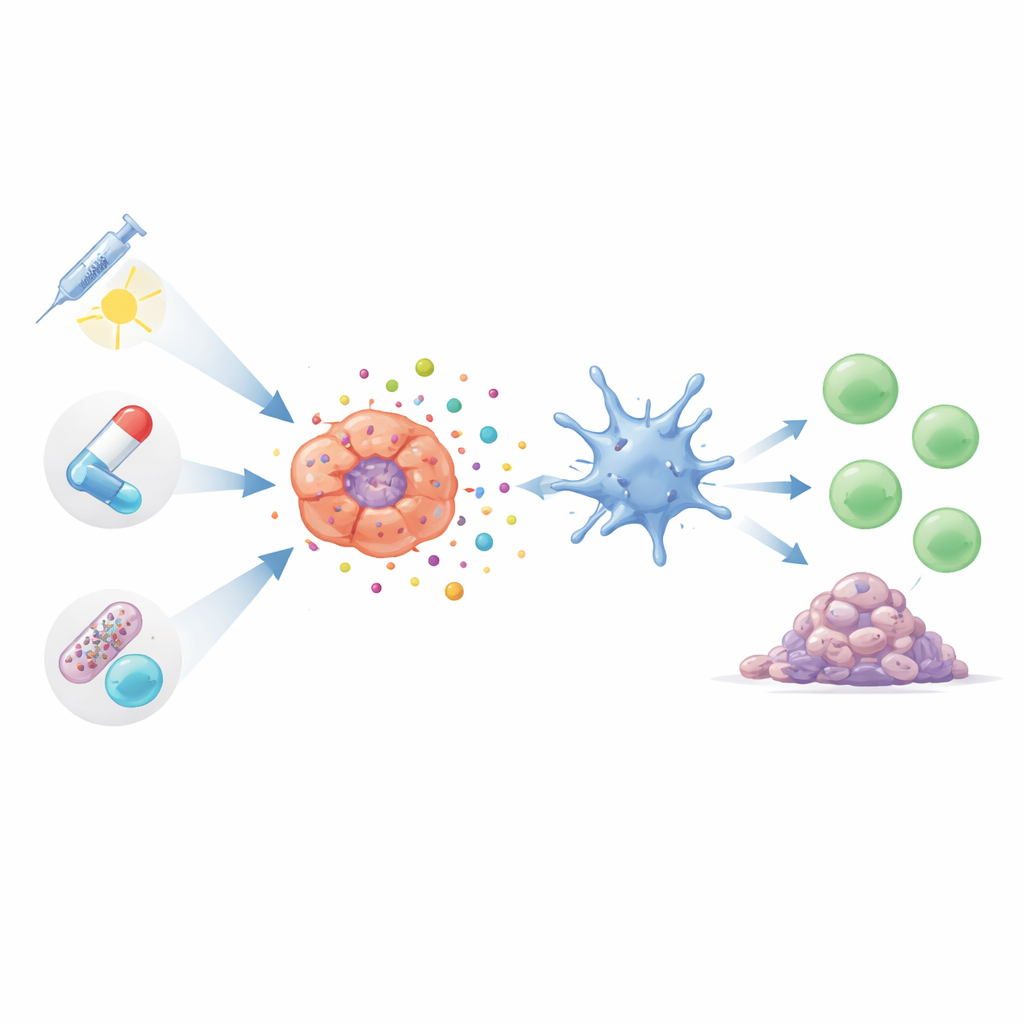
Многие знакомые методы терапии рака легкого могут вызвать такой сигнализирующий гибельный процесс при правильном применении. Некоторые химиопрепараты, включая широко используемые таксаны и платиновые соединения, способны переводить опухолевые клетки в состояние стресса, приводящее к высвобождению сигналов опасности. Эти лечения не только непосредственно сокращают опухоли, но и могут стимулировать Т‑клетки и полезные макрофаги к действию. Новые, более таргетные формы химиотерапии — антитело‑лекарственные конъюгаты — доставляют токсическую нагрузку прямо в раковые клетки. В ранних исследованиях эти таргетные препараты не только чище уничтожают опухоли, но и, по видимому, вызывают более сильные иммунные ответы с меньшими системными побочными эффектами.
Лучевая терапия, таргетные препараты и фототерапия как партнёры иммунитета
Лучевая терапия делает больше, чем просто «поджаривает» опухоли; повреждая ДНК и генерируя реактивные молекулы внутри раковых клеток, она может направлять их к иммуногенной гибели. Однако эффект сильно зависит от дозы и графика: умеренная, правильно спланированная радиация может сильно стимулировать иммунитет, тогда как чрезмерно высокие дозы могут подавлять ключевые пути распознавания. Исследователи также разрабатывают наночастицы, которые усиливают полезные сигналы и противодействуют подавляющим. Тем временем точечные препараты, блокирующие драйверы роста, такие как EGFR, ALK, AXL, или сигналы, связанные с кровоснабжением, сейчас рассматриваются как двойного назначения: они замедляют рост опухоли и, во многих моделях, способствуют обнажению опухолевого материала и сигналов опасности, пробуждающих Т‑клетки. Лечения, активируемые светом, которые используют фоточувствительные соединения для генерации всплесков токсичных форм кислорода внутри опухолей, можно настроить так, чтобы поражать клеточные структуры, наиболее эффективно вызывающие иммунно‑видимую гибель клеток.
Новые участники: вирусы, электрические поля и микробиом кишечника
Помимо стандартных столпов онкологической помощи, несколько новых инструментов также опираются на иммуногенную клеточную гибель. Инженерные вирусы, селективно инфицирующие клетки рака легкого, разрывают их и одновременно привлекают иммунные клетки, иногда приводя в экспериментальных моделях к регрессии отдаленных, нелеченных опухолей. Низкоинтенсивные переменные электрические поля, уже применяемые при других формах рака, показали способность вызывать стресс в клетках рака легкого таким образом, что высвобождаются сигналы опасности и поощряется инфильтрация Т‑клеток. Даже бактерии, обитающие в нашем кишечнике, могут влиять на силу этих ответов, опосредованных ИКГ. Определенные микробы кишечника, по‑видимому, способствуют более активному антиопухолевому окружению, в то время как другие создают иммуно‑подавляющее состояние, которое может ослаблять преимущества методов, основанных на ИКГ.
Что это значит для будущего лечения рака легкого
Главная мысль статьи в том, что то, как умирает опухолевая клетка, так же важно, как и то, умирает ли она вообще. Если гибель иммуногенна, каждая уничтоженная раковая клетка может стать уроком для иммунной системы, помогая ей распознавать и атаковать оставшиеся клетки опухоли и возможно предотвращать рецидив. Чтобы сделать это практической реальностью для людей с немелкоклеточным раком легкого, исследователям по‑прежнему нужны четкие маркеры, позволяющие определить, происходит ли ИКГ у пациентов, лучшие способы согласования доз и комбинаций терапий и стратегии противодействия многочисленным путям уклонения опухоли. Если эти задачи будут решены, будущие схемы лечения могут регулярно сочетать препараты, индуцирующие ИКГ, с иммуноусиливающими препаратами, превращая кратковременные ответы в более долговременный контроль заболевания.
Цитирование: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Ключевые слова: иммуногенная клеточная гибель, немелкоклеточный рак легкого, иммунотерапия рака, химиолучевая терапия, опухолевый микроокружение