Clear Sky Science · sv
Integrering av immunogen celldöd i behandlingslandskapet för icke-småcellig lungcancer: utnyttja immunsystemets kraft
Varför det spelar roll att lära tumörer att larma immunsystemet
Lungcancer är fortfarande en av de dödligaste cancerformerna i världen, till stor del därför att tumörer ofta återkommer eller är motståndskraftiga mot standardbehandlingar. Denna artikel undersöker en lovande idé: i stället för att bara döda cancerceller tyst kan läkare få dem att dö på ett sätt som högljutt varnar kroppens försvar. Genom att omvandla tumörförstörelse till en slags intern vaccinering kan en behandling som immunogen celldöd hjälpa immunsystemet att känna igen, minnas och mer effektivt bekämpa icke‑småcellig lungcancer.
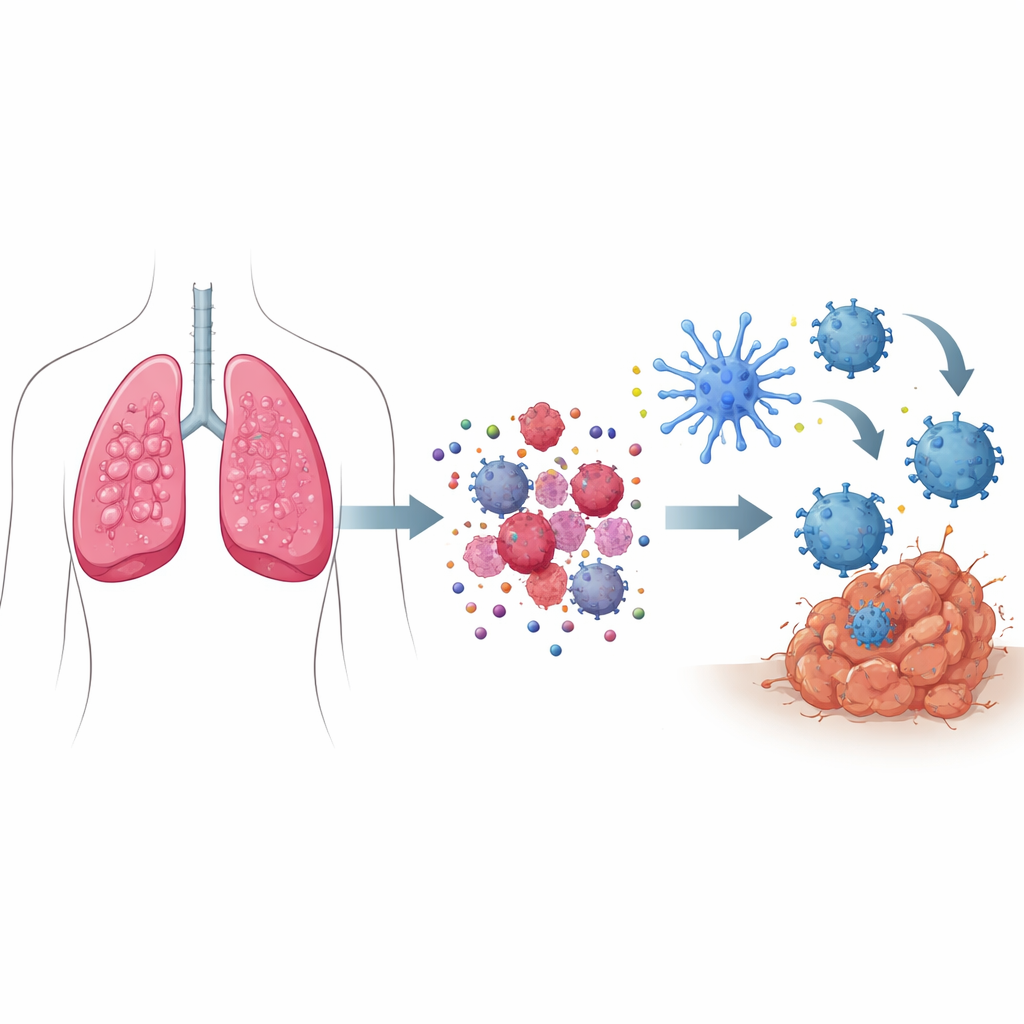
Hur ”farsignaler” förvandlar celldöd till ett nödrop
När de flesta celler dör sker det tyst, utan att immunsystemet reagerar. Vid immunogen celldöd skickar de döende cancercellerna däremot ut ett koordinerat set av farsignaler. Stresståliga komponenter inuti cellen trycker vissa proteiner till cellytan, vilket markerar den som något som ska ”ätas” av immunsystemets vakter. Samtidigt sipprar små molekyler som ATP ut och fungerar som nödraketer som drar immunceller till området, medan andra proteiner släpps fria och beter sig som larm. Tillsammans attraherar och aktiverar dessa signaler specialiserade spejare kallade dendritiska celler, som tar upp fragment av tumören, bearbetar dem och sedan presenterar tumörbitar för T‑celler—genom detta tränas de att söka upp och förstöra cancerceller i hela kroppen.
Göra vanliga behandlingar till immun‑tränare
Många välkända lungcancerterapier kan utlösa denna typ av alarmfylld celldöd om de används på rätt sätt. Vissa cytostatika, inklusive de ofta använda taxanerna och platinakomplexen, kan driva tumörceller till ett stressat tillstånd som leder till frisättning av farsignaler. Dessa behandlingar krymper inte bara tumörer direkt utan kan också stimulera T‑celler och fördelaktiga makrofager att slå till. Nyare, mer riktade former av cytostatika, kallade antikropps-läkemedelskonjugat, levererar toxiska laster precist till cancerceller. I tidiga studier tycks dessa riktade läkemedel inte bara döda tumörer mer selektivt utan också framkalla starkare immunrespons med färre systemiska biverkningar.
Strålning, riktade läkemedel och ljusbaserad terapi som immunsamarbetspartners
Strålbehandling gör mer än att bränna tumörer; genom att skada DNA och generera reaktiva molekyler i cancerceller kan den driva dem mot immunogen död. Effekten beror dock starkt på dos och schema: måttlig, välavvägd strålning kan vara starkt immunstimulerande, medan alltför höga doser faktiskt kan dämpa viktiga sensorsystem. Forskare utvecklar också nanopartiklar som förstärker de hjälpsamma signalerna och motverkar de undertryckande. Samtidigt förstår man nu att precisionsläkemedel som blockerar tillväxtdrivare som EGFR, ALK, AXL eller kärlbildningssignaler kan ha dubbel verkan: de bromsar tumörtillväxt och hjälper i många modeller till att exponera tumörmaterial och farsignaler som väcker T‑celler. Ljusaktiverade behandlingar, som använder fotosensitiva föreningar för att generera spridda mängder toxiska syreradikaler i tumörer, kan ställas in för att träffa de cellulära strukturer som mest effektivt utlöser immun‑synlig celldöd.
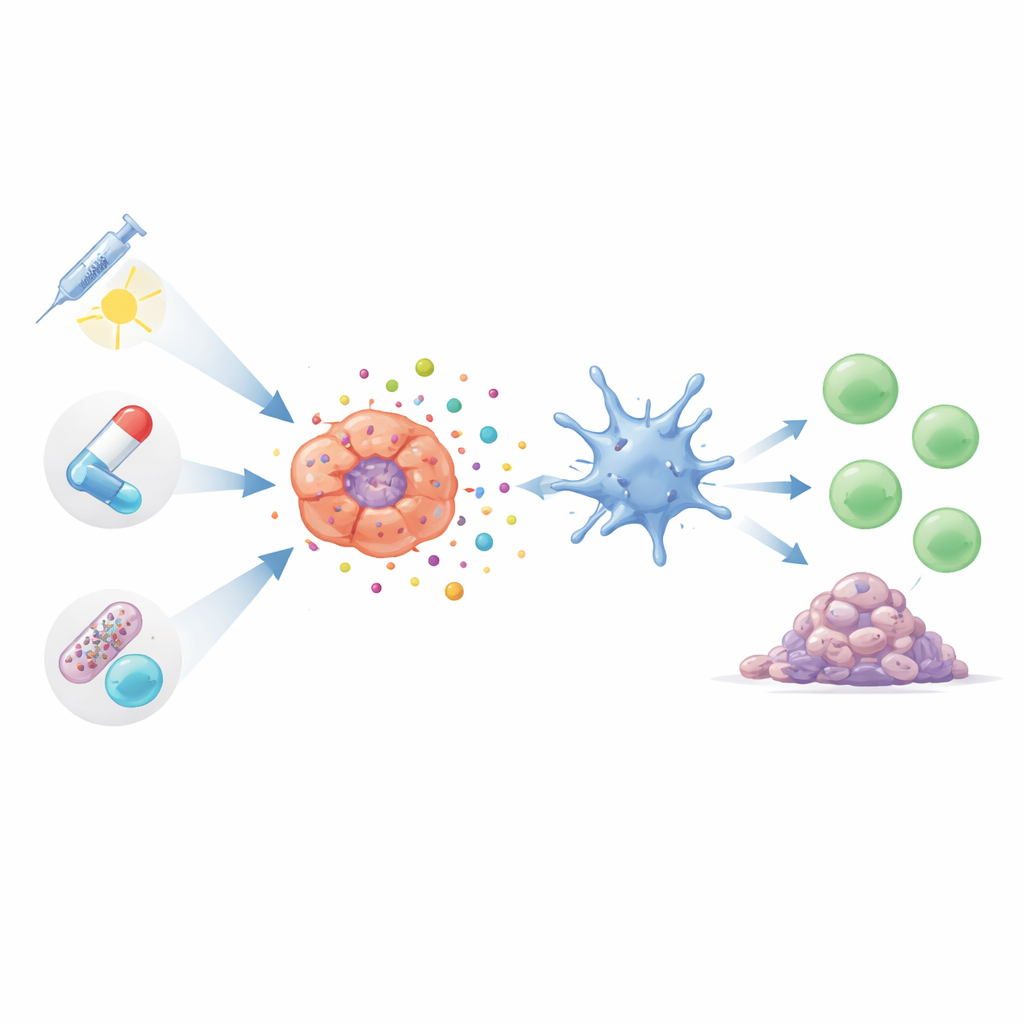
Nya aktörer: virus, elektriska fält och tarmmikrobiomet
Bortom de klassiska vårdpelarna för cancer bygger flera framväxande verktyg också på immunogen celldöd. Modifierade virus som selektivt infekterar lungcancerceller får dem att brista och samtidigt dra till sig immunceller, vilket i försöksmodeller ibland leder till regression av fjärrbelägna, obehandlade tumörer. Växelström med låg intensitet, redan använd i andra cancerformer, har visat sig stressa lungcancerceller på sätt som får dem att släppa farsignaler och uppmuntra T‑cellsinfiltration. Till och med bakterierna i våra tarmar kan påverka hur kraftfulla dessa ICD‑drivna responser blir. Vissa tarmmikrober verkar främja en mer aktiv anti‑tumörmiljö, medan andra skapar ett immundämpande tillstånd som kan försvaga nyttan av ICD‑baserade behandlingar.
Vad detta betyder för framtidens lungcancervård
Artikelns övergripande budskap är att hur en tumörcell dör är minst lika viktigt som att den dör. Om döden är immunogen kan varje förstörd cancercell bli en läxa för immunsystemet, hjälpa det att känna igen och angripa kvarvarande cancer och möjligen förhindra återfall. För att göra detta till verklighet för personer med icke‑småcellig lungcancer behöver forskare fortfarande tydliga markörer för att avgöra när ICD sker hos patienter, bättre metoder för att matcha doser och kombinationer av behandlingar samt strategier för att motverka tumörens många flyktvägar. Om dessa utmaningar kan mötas kan framtida behandlingsplaner rutinmässigt para ihop ICD‑inducerande terapier med immunstimulerande läkemedel och förvandla kortvariga svar till mer hållbar kontroll av sjukdomen.
Citering: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Nyckelord: immunogen celldöd, icke-småcellig lungcancer, cancerimmunterapi, kemoradioterapi, tumörmikromiljö