Clear Sky Science · nl
Integratie van immunogeen celdood in het behandelbeeld van niet‑kleincellige longkanker: het benutten van de kracht van het immuunsysteem
Waarom het belangrijk is tumoren te leren het immuunsysteem te alarmeren
Longkanker blijft een van de dodelijkste kankersoorten wereldwijd, grotendeels omdat tumoren vaak terugkeren of bestand zijn tegen standaardbehandelingen. Dit artikel onderzoekt een veelbelovend idee: in plaats van kankercellen stilletjes te doden, zouden artsen ze zodanig kunnen laten sterven dat ze luid het afweersysteem alarmeren. Door tumordestructie te veranderen in een soort interne vaccinatie, zou een behandeling genaamd immunogeen celdood het immuunsysteem kunnen helpen de niet‑kleincellige longkanker te herkennen, te onthouden en effectiever te bestrijden.
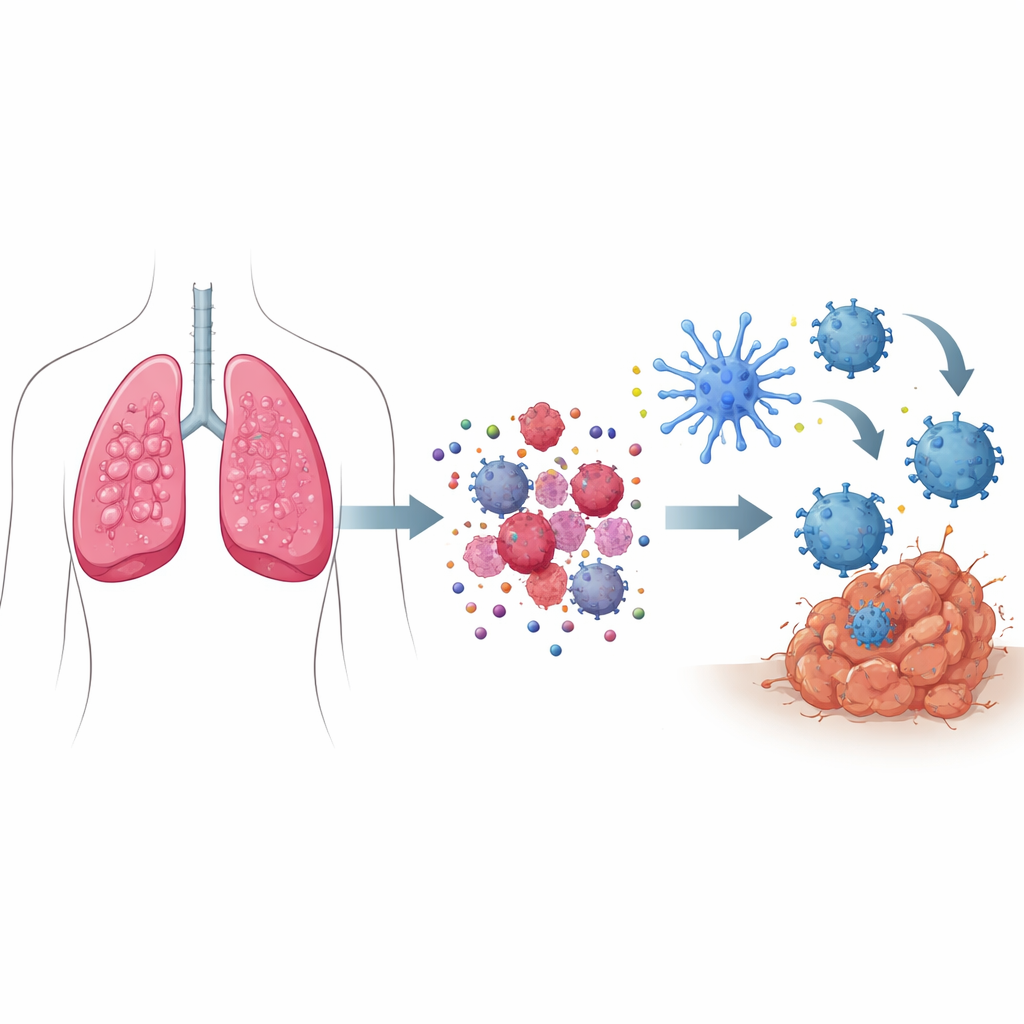
Hoe “gevaarssignalen” celdood veranderen in een noodoproep
Wanneer de meeste cellen sterven, gebeurt dat stil en zonder het immuunsysteem op te schrikken. Bij immunogeen celdood sturen stervende kankercellen echter een gecoördineerde set gevaarssignalen uit. Gestreste componenten binnen de cel verplaatsen bepaalde eiwitten naar het celoppervlak en markeren de cel als iets dat door immuunsentinels moet worden “opgeruimd”. Tegelijkertijd sijpelen kleine moleculen zoals ATP naar buiten en fungeren als fakkels die immuuncellen aantrekken, terwijl andere eiwitten vrijkomen die als alarmen werken. Samen trekken en activeren deze signalen gespecialiseerde verkenners, de dendritische cellen, die stukjes tumor opnemen, verwerken en vervolgens tumorfragmenten presenteren aan T‑cellen — waardoor die worden getraind om kankercellen in het hele lichaam op te zoeken en te vernietigen.
Veelgebruikte behandelingen omvormen tot immuuntrainers
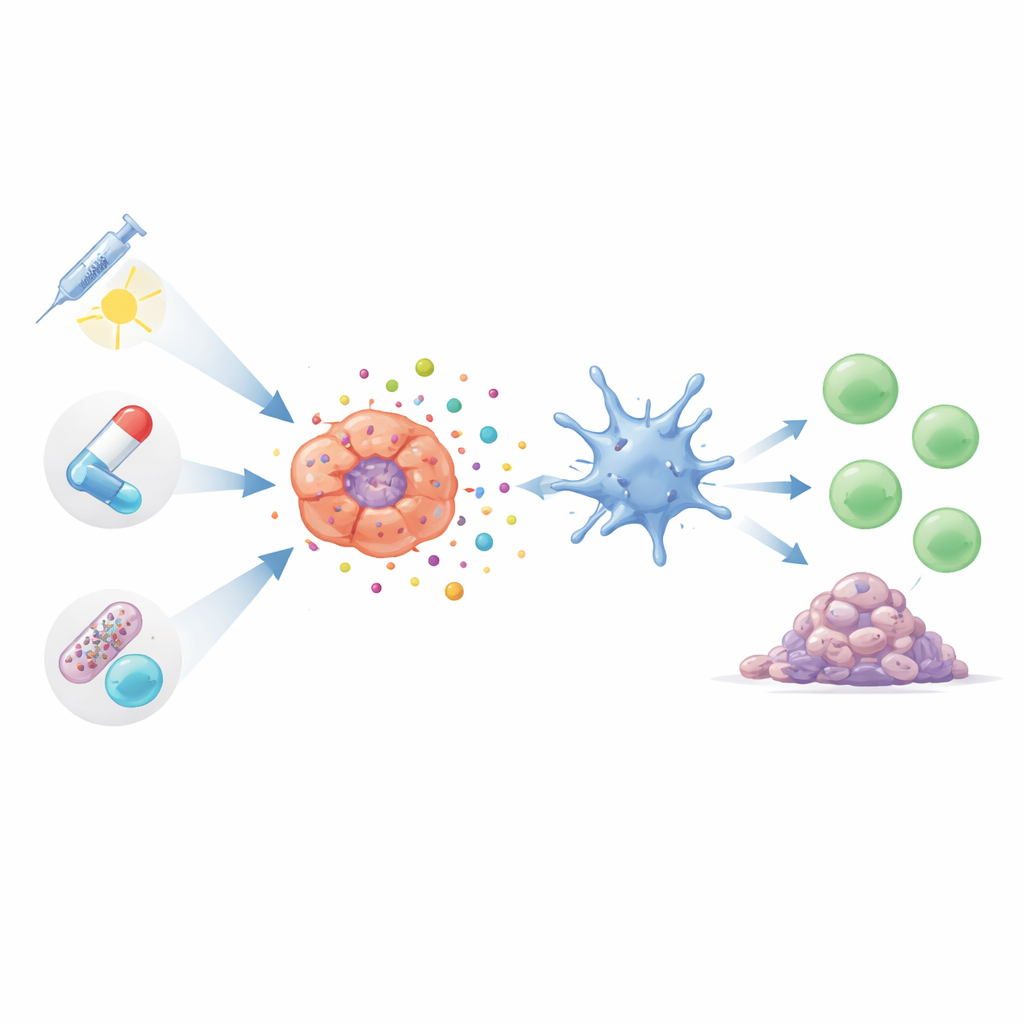
Verschillende bekende therapieën voor longkanker kunnen dit type alarmrijke celdood opwekken als ze op de juiste manier worden ingezet. Bepaalde chemotherapiemiddelen, waaronder veelgebruikte taxanen en platinumverbindingen, kunnen tumorcellen in een gestreste toestand brengen die leidt tot de afgifte van gevaarssignalen. Deze behandelingen verkleinen niet alleen tumoren direct, maar kunnen ook T‑cellen en gunstige macrofagen activeren. Nieuwere, gerichtere vormen van chemotherapie, zogenaamde antilichaam‑chemische conjugaten, leveren toxische ladingen nauwkeurig af bij kankercellen. In vroege studies doden deze gerichte middelen tumoren niet alleen schoner, maar lijken ze ook sterkere immuunreacties op te roepen met minder systemische bijwerkingen.
Radiatie, gerichte medicijnen en lichtgebaseerde therapie als immuunpartners
Radiotherapie doet meer dan alleen tumoren verschroeien; door DNA te beschadigen en reactieve moleculen binnen kankercellen te genereren, kan het hen naar immunogeen celdood duwen. Het effect hangt echter sterk af van dosis en schema: matige, goed getimedede stralingsbehandelingen kunnen sterk immuunstimulerend zijn, terwijl te hoge doses juist sleuteldetectieroutes kunnen onderdrukken. Onderzoekers ontwerpen ook nanodeeltjes die de nuttige signalen versterken en de onderdrukkende tegengaan. Tegelijkertijd blijken precisiegeneesmiddelen die groeidrivers zoals EGFR, ALK, AXL of vaatvormingssignalen blokkeren, een dubbele rol te vervullen: ze remmen tumorgroei en helpen in veel modellen tumormateriaal en gevaarssignalen bloot te leggen die T‑cellen wakker schudden. Lichtgeactiveerde behandelingen, die fotosensitieve verbindingen gebruiken om uitbarstingen van toxische zuurstofsoorten in tumoren te genereren, kunnen zodanig worden afgestemd dat ze die celstructuren raken die het meest effectief immuunzichtbare celdoodreacties oproepen.
Nieuwe spelers: virussen, elektrische velden en het darmmicrobioom
Naast de standaardpijlers van kankerzorg vertrouwen meerdere opkomende instrumenten ook op immunogeen celdood. Gecultiveerde virussen die selectief longkankercellen infecteren laten deze openbarsten en trekken tegelijkertijd immuuncellen aan, wat in experimentele modellen soms leidt tot regressie van verre, onbehandelde tumoren. Lage‑intensiteits afwisselende elektrische velden, al gebruikt bij andere kankers, blijken longkankercellen op een manier te belasten die gevaarssignalen vrijmaakt en T‑celinfiltratie bevordert. Zelfs de bacteriën in onze darmen kunnen beïnvloeden hoe sterk deze ICD‑gedreven reacties zijn. Bepaalde darmmicroben lijken een aktiever antitumormilieu te bevorderen, terwijl andere een immuundempende toestand ondersteunen die de voordelen van ICD‑gebaseerde behandelingen zou kunnen verminderen.
Wat dit betekent voor de toekomstige zorg bij longkanker
De algemene boodschap van het artikel is dat de manier waarop een tumorcel sterft net zo belangrijk is als het feit dat hij sterft. Als de celdood immunogeen is, kan elke vernietigde kankercel een les worden voor het immuunsysteem, waardoor het resterende kankercellen herkent en aanvalt en mogelijk recidief voorkomt. Om dit praktisch haalbaar te maken voor mensen met niet‑kleincellige longkanker hebben onderzoekers nog duidelijke markers nodig om te bepalen wanneer ICD bij patiënten plaatsvindt, betere manieren om doseringen en combinaties van therapieën af te stemmen, en strategieën om de vele ontsnappingsroutes van de tumor te ondermijnen. Als deze uitdagingen kunnen worden opgelost, kunnen toekomstige behandelplannen routinematig ICD‑inducerende therapieën combineren met immuunversterkende geneesmiddelen en zo kortdurende responsen omzetten in duurzamere ziektecontrole.
Bronvermelding: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Trefwoorden: immunogeen celdood, niet‑kleincellige longkanker, kankerimmunotherapie, chemo‑radiotherapie, tumormicro‑omgeving