Clear Sky Science · tr
İmmünojenez yaratan hücre ölümünün ileri evre olmayan akciğer kanseri tedavi yelpazesine entegrasyonu: bağışıklık sisteminin gücünden yararlanmak
Tümörlere Bağışıklık Sistemini Uyarmayı Öğretmenin Önemi
Akciğer kanseri, büyük ölçüde tümörlerin sıkça nüks etmesi veya standart tedavilere direnç göstermesi nedeniyle dünya çapında en ölümcül kanserlerden biridir. Bu makale umut verici bir fikri inceliyor: kanser hücrelerini sessizce öldürmek yerine, onların ölümüyle vücudun savunmasını yüksek sesle uyandırmak mümkün olabilir. Tümör yok edilişini içsel bir aşılamaya dönüştürerek, immünojenik hücre ölümü olarak adlandırılan bir yaklaşım, bağışıklık sisteminin küçük hücre dışı akciğer kanserini tanımasını, hatırlamasını ve daha etkili şekilde savaşmasını sağlayabilir.
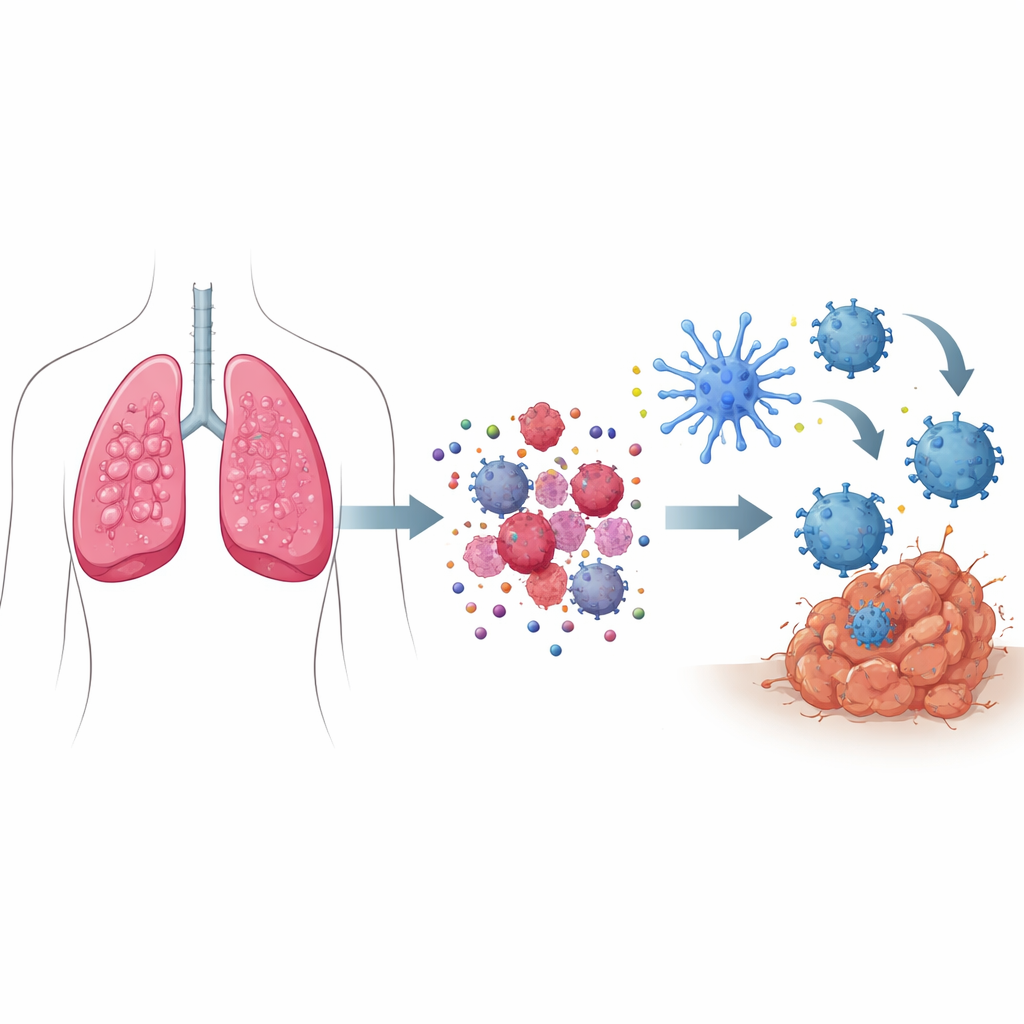
“Tehlike Sinyalleri” Hücre Ölümünü Yardım Çağrısına Nasıl Dönüştürür
Çoğu hücre öldüğünde bunu sessizce yapar ve bağışıklık sistemini uyandırmaz. Ancak immünojenik hücre ölümünde, ölen kanser hücreleri koordineli bir tehlike sinyali seti gönderir. Hücre içindeki stresli bileşenler belirli proteinleri hücre yüzeyine taşır ve böylece hücreyi bağışıklık gözcülerince “yenecek” bir şey olarak işaretler. Aynı zamanda ATP gibi küçük moleküller dışarı sızar, işaret fenerleri gibi bağışıklık hücrelerini bölgeye çeker ve diğer proteinler alarm görevini üstlenir. Bu sinyaller birlikte dendritik hücreler adı verilen özelleşmiş keşif hücrelerini çekip aktive eder; bunlar tümörden parçacıklar alır, işler ve ardından tümör parçalarını T hücrelerine sunar—T hücrelerini vücut genelinde kanser hücrelerini arayıp yok etmeye çalışacak şekilde eğitir.
Yaygın Tedavileri Bağışıklık Eğiticilerine Dönüştürmek
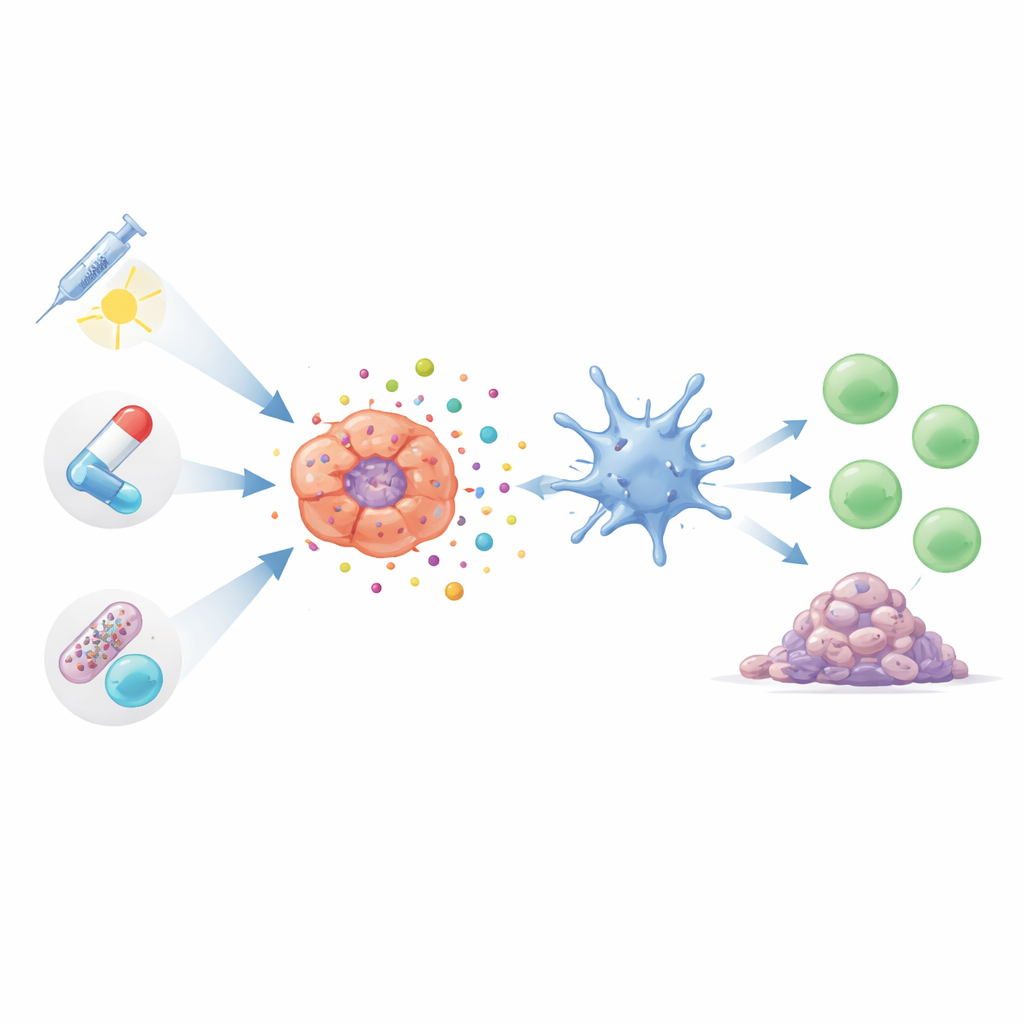
Birçok bilinen akciğer kanseri tedavisi, doğru şekilde kullanıldığında bu tür alarm dolu hücre ölümünü tetikleyebilir. Yaygın olarak kullanılan taksanlar ve platin bileşikleri gibi bazı kemoterapi ilaçları, tümör hücrelerini stresli bir duruma sokarak tehlike sinyallerinin salınmasına yol açabilir. Bu tedaviler sadece tümörleri doğrudan küçültmekle kalmaz, aynı zamanda T hücreleri ve yararlı makrofajları da harekete geçirebilir. Antikor‑ilaç konjugatları olarak adlandırılan daha yeni, hedefe yönelik kemoterapi biçimleri ise toksik yükleri hassas şekilde kanser hücrelerine taşır. Erken çalışmalarda, bu hedefe yönelik ilaçların tümörleri daha temiz şekilde öldürmekle kalmayıp, tüm vücut yan etkileri daha az olurken daha güçlü bağışıklık yanıtları tetiklediği görünmektedir.
Radyasyon, Hedefe Yönelik İlaçlar ve Işık Temelli Tedaviler: Bağışıklığın Ortakları
Radyoterapi, tümörleri yakmanın ötesinde etki gösterir; DNA’ya zarar vererek ve kanser hücreleri içinde reaktif moleküller üreterek onları immünojenik ölüme itebilir. Ancak bu etkinin doz ve programa çok bağlı olduğu unutulmamalıdır: ölçülü, iyi zamanlanmış radyasyon güçlü şekilde bağışıklığı uyaran olabilirken, aşırı yüksek dozlar temel algılama yollarını baskılayabilir. Araştırmacılar, yararlı sinyalleri güçlendiren ve baskılayıcı olanları etkisizleştiren nanopartiküller tasarlamaktadır. Bu arada EGFR, ALK, AXL gibi büyüme sürücülerini veya damar sinyallerini engelleyen hassas ilaçların artık çifte görev yaptığı anlaşılmaktadır: tümör büyümesini yavaşlatmak ve birçok modelde tümör materyalini ve T hücrelerini uyandıran tehlike ipuçlarını açığa çıkarmaya yardım etmek. Fotosensitif bileşikler kullanarak tümör içinde toksik oksijen türleri patlaması oluşturan ışıkla aktive edilen tedaviler ise, en etkili şekilde bağışıklık‑görünür hücre ölümünü tetikleyen hücresel yapıların hedeflenmesi için ayarlanabilir.
Yeni Oyuncular: Virüsler, Elektrik Alanları ve Bağırsak Mikrobiyomu
Standart kanser bakımının ötesinde, birkaç ortaya çıkan araç da immünojenik hücre ölümüne dayanıyor. Seçilerek akciğer kanseri hücrelerini enfekte eden genetik olarak tasarlanmış virüsler hücreleri parçalayarak açık hale getirirken aynı zamanda bağışıklık hücrelerini çeker; deneysel modellerde bazen uzak, tedavi edilmemiş tümörlerin gerilemesine yol açar. Diğer kanserlerde zaten kullanılan düşük‑şiddetli alternatif elektrik alanlarının akciğer kanseri hücrelerini strese soktuğu, tehlike sinyallerinin salınmasına ve T hücresi infiltrasyonunun teşvik edilmesine yol açtığı gösterilmiştir. Hatta bağırsaklarımızda yaşayan bakteriler bile bu ICD kaynaklı yanıtların gücünü etkileyebilir. Bazı bağırsak mikropları daha aktif bir antitümör ortamı teşvik ederken, bazıları immünü baskılayıcı bir durum oluşturarak ICD tabanlı tedavilerin faydalarını azaltabilir.
Bu, Gelecekteki Akciğer Kanseri Bakımı İçin Ne Anlama Geliyor
Makalenin genel mesajı şudur: bir tümör hücresinin nasıl öldüğü, sadece ölüp ölmediği kadar önemlidir. Eğer ölüm immünojenikse, her yok edilen kanser hücresi bağışıklık sistemi için bir ders haline gelebilir; bu, kalan kanseri tanımasına, saldırmasına ve nüksü önlemeye yardımcı olabilir. Bunu küçük hücre dışı akciğer kanserli hastalar için pratik bir gerçeğe dönüştürebilmek adına araştırmacıların hâlâ hastalarda ICD’nin ne zaman olduğunu gösteren net belirteçlere, dozları ve tedavi kombinasyonlarını eşleştirmek için daha iyi yaklaşımlara ve tümörün birçok kaçış yoluna karşı stratejilere ihtiyacı vardır. Bu zorluklar aşılabilirse, gelecekteki tedavi planları rutin olarak ICD indükleyici tedavileri bağışıklığı güçlendirici ilaçlarla eşleştirerek kısa süreli yanıtları hastalığın daha kalıcı kontrolüne dönüştürebilir.
Atıf: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Anahtar kelimeler: immünojenik hücre ölümü, küçük hücre dışı akciğer kanseri, kanser immünoterapisi, kemoradyoterapi, tümör mikroçevresi