Clear Sky Science · pl
Integracja immunogennej śmierci komórkowej w leczeniu niedrobnokomórkowego raka płuca: wykorzystanie siły układu odpornościowego
Dlaczego warto nauczyć guzy alarmować układ odpornościowy
Rak płuca pozostaje jednym z najbardziej śmiertelnych nowotworów na świecie, w dużej mierze dlatego, że guzy często nawracają lub wykazują oporność na standardowe terapie. W tym artykule analizujemy obiecującą koncepcję: zamiast tylko cicho zabijać komórki nowotworowe, lekarze mogą je skłonić do takiej śmierci, która głośno alarmuje mechanizmy obronne organizmu. Przekształcając niszczenie guza w rodzaj wewnętrznego szczepienia, terapia zwana immunogenną śmiercią komórkową może pomóc układowi odpornościowemu rozpoznać, zapamiętać i skuteczniej zwalczać niedrobnokomórkowego raka płuca.
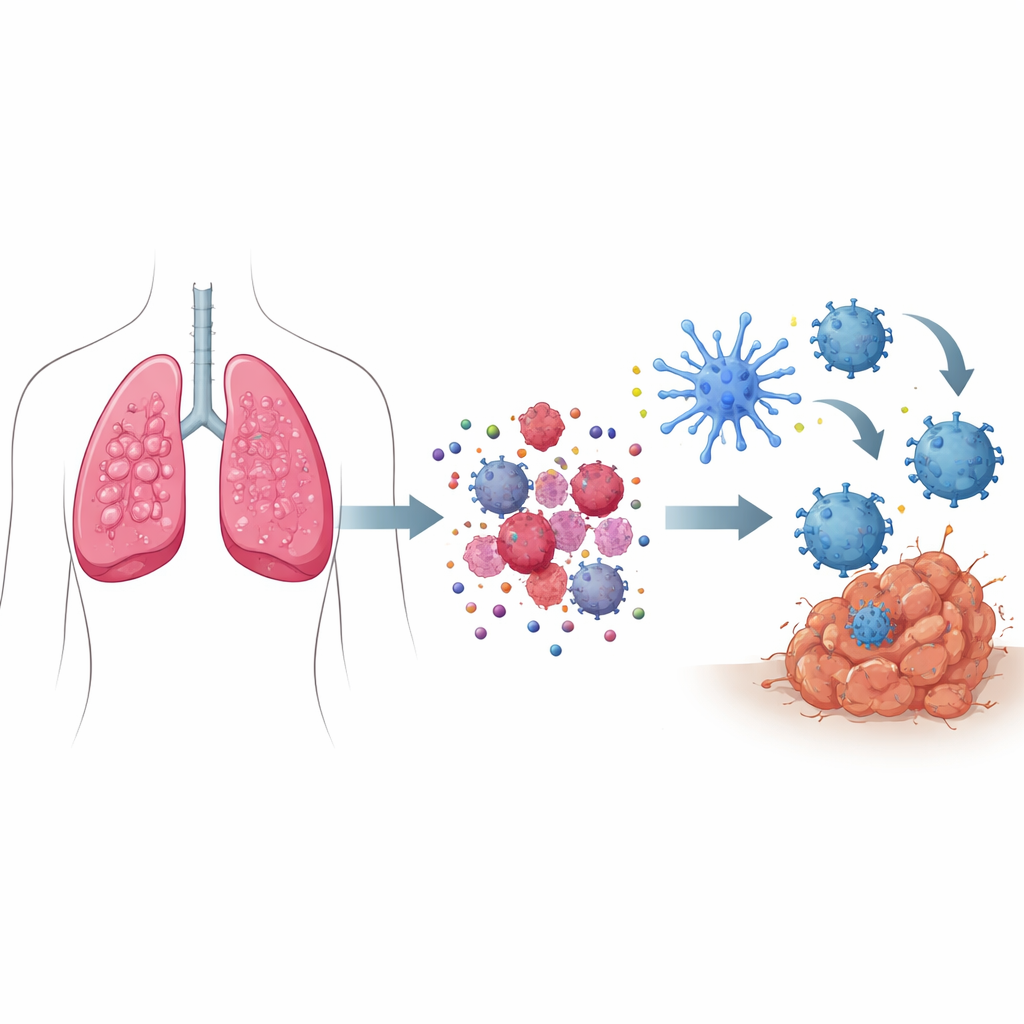
Jak „sygnały niebezpieczeństwa” zamieniają śmierć komórki w wezwanie o pomoc
Kiedy większość komórek umiera, dzieje się to cicho, bez pobudzenia układu odpornościowego. W immunogennej śmierci komórkowej jednak umierające komórki nowotworowe wysyłają skoordynowany zestaw sygnałów niebezpieczeństwa. Zestresowane elementy wewnątrz komórki przemieszczają określone białka na powierzchnię komórki, oznaczając ją jako do „pożarcia” przez strażników immunologicznych. Równocześnie małe cząsteczki, takie jak ATP, wydostają się na zewnątrz, działając niczym race przyciągające komórki odpornościowe, podczas gdy inne białka są uwalniane i zachowują się jak alarmy. Te sygnały razem przyciągają i aktywują wyspecjalizowane zwiadowcze komórki — komórki dendrytyczne, które pochłaniają fragmenty guza, przetwarzają je, a następnie prezentują fragmenty nowotworu limfocytom T — ucząc je rozpoznawać i niszczyć komórki nowotworowe w całym organizmie.
Przekształcanie powszechnych terapii w trenerów odporności
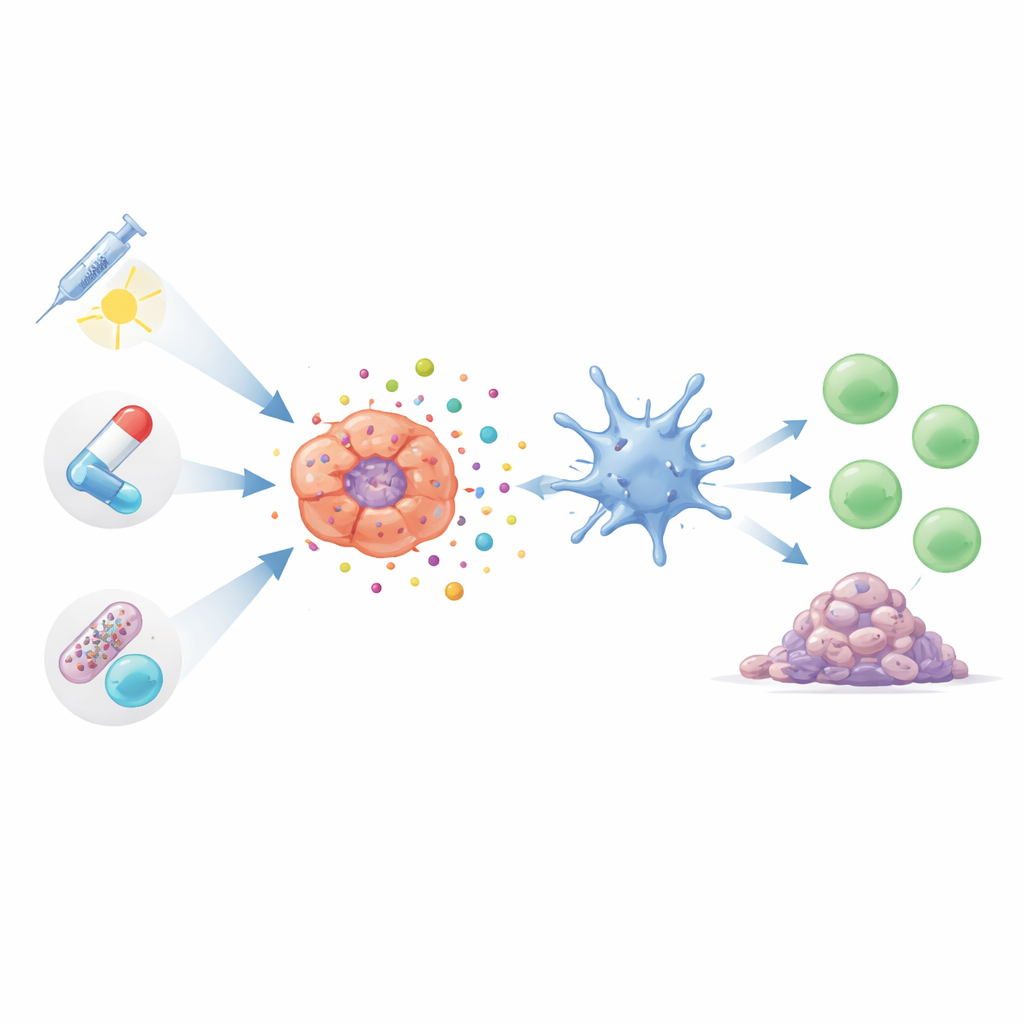
Wiele znanych terapii raka płuca może wywołać tego rodzaju alarmującą śmierć komórkową, jeśli zostaną użyte w odpowiedni sposób. Niektóre leki chemioterapeutyczne, w tym szeroko stosowane taksany i związki platyny, mogą wprowadzać komórki nowotworowe w stan stresu prowadzący do uwolnienia sygnałów niebezpieczeństwa. Terapie te nie tylko bezpośrednio zmniejszają guzy, lecz także mogą pobudzać limfocyty T i korzystne makrofagi do działania. Nowocześniejsze, bardziej ukierunkowane formy chemioterapii, zwane koniugatami przeciwciało–lek, dostarczają toksyczne ładunki precyzyjnie do komórek nowotworowych. W wczesnych badaniach te leki celowane nie tylko zabijają guzy w bardziej selektywny sposób, lecz także wydają się wzmacniać odpowiedzi immunologiczne przy mniejszych ogólnoustrojowych skutkach ubocznych.
Radioterapia, leki celowane i terapie światłem jako partnerzy immunologiczni
Radioterapia robi więcej niż tylko przypala guzy; uszkadzając DNA i generując reaktywne cząsteczki wewnątrz komórek nowotworowych, może popychać je w kierunku immunogennej śmierci. Efekt zależy jednak w dużym stopniu od dawki i harmonogramu: umiarkowana, dobrze zaplanowana radioterapia może silnie stymulować układ odpornościowy, podczas gdy nadmiernie wysokie dawki mogą osłabić kluczowe szlaki detekcji. Badacze projektują też nanocząstki, które wzmacniają korzystne sygnały i przeciwdziałają tym hamującym. Tymczasem precyzyjne leki blokujące czynniki wzrostu, takie jak EGFR, ALK, AXL czy sygnały naczyniowe, wykazują podwójną rolę: spowalniają wzrost guza i w wielu modelach pomagają odsłonić materiał guza oraz sygnały niebezpieczeństwa, które budzą limfocyty T. Terapie aktywowane światłem, wykorzystujące fotosensybilne związki do generowania impulsów toksycznych form tlenu w obrębie guza, można dostroić tak, by trafiały w struktury komórkowe najsilniej wywołujące immunologicznie widoczną śmierć komórkową.
Nowi gracze: wirusy, pola elektryczne i mikrobiom jelitowy
Później poza standardowymi filarami opieki onkologicznej pojawia się kilka nowych narzędzi opierających się również na immunogennej śmierci komórkowej. Inżynieryjne wirusy, które selektywnie infekują komórki raka płuca, powodują ich pęknięcie, przyciągając jednocześnie komórki odpornościowe, co w modelach eksperymentalnych czasem prowadzi do regresji odległych, nieleczonych guzów. Niskonapięciowe zmienne pola elektryczne, już stosowane w innych nowotworach, wykazano, że stresują komórki raka płuca w sposób sprzyjający uwalnianiu sygnałów niebezpieczeństwa i napływowi limfocytów T. Nawet bakterie zamieszkujące nasze jelita mogą wpływać na siłę tych odpowiedzi wywoływanych przez ICD. Niektóre mikroby jelitowe wydają się sprzyjać bardziej aktywnemu środowisku przeciwguza, podczas gdy inne promują stan tłumiący odporność, który może osłabić korzyści terapii opartych na ICD.
Co to oznacza dla przyszłej opieki nad rakiem płuca
Główne przesłanie artykułu jest takie, że to, w jaki sposób komórka nowotworowa umiera, ma taką samą wagę jak to, czy w ogóle umiera. Jeśli śmierć jest immunogenna, każda zniszczona komórka nowotworowa może stać się lekcją dla układu odpornościowego, pomagając mu rozpoznać i zaatakować pozostałe komórki nowotworowe oraz potencjalnie zapobiegać nawrotom. Aby uczynić to praktyczną rzeczywistością dla osób z niedrobnokomórkowym rakiem płuca, badacze potrzebują wciąż jasnych markerów wskazujących, kiedy ICD zachodzi u pacjentów, lepszych sposobów dopasowania dawek i kombinacji terapii oraz strategii przeciwdziałania licznym drogim ucieczki guza. Jeśli tym wyzwaniom uda się sprostać, przyszłe plany leczenia mogą rutynowo łączyć terapie indukujące ICD z lekami wzmacniającymi odporność, przekształcając krótkotrwałe odpowiedzi w bardziej trwałą kontrolę choroby.
Cytowanie: Liu, Z., Xu, X., Wang, M. et al. Integration of immunogenic cell death in the treatment landscape of non-small cell lung cancer: harnessing the power of the immune system. Cell Death Discov. 12, 155 (2026). https://doi.org/10.1038/s41420-026-03012-2
Słowa kluczowe: immunogenna śmierć komórkowa, niedrobnokomórkowy rak płuca, immunoterapia nowotworów, chemioterapia i radioterapia, mikrośrodowisko guza