Clear Sky Science · zh
克雷伯氏肺炎杆菌LPS通过基质介导抑制p53并导致结直肠癌化疗耐药
为什么肠道细菌会影响癌症治疗
结直肠癌通常采用强效化疗药物治疗,但许多肿瘤会学会在这些攻击下生存。本研究探讨了一个出人意料的“同伙”:某些肠道细菌。研究者展示了这些微生物产生的分子如何在肿瘤内悄然削弱人体主要的抗癌防线之一,使标准治疗效果下降——即便癌细胞本身并未被细菌直接接触。
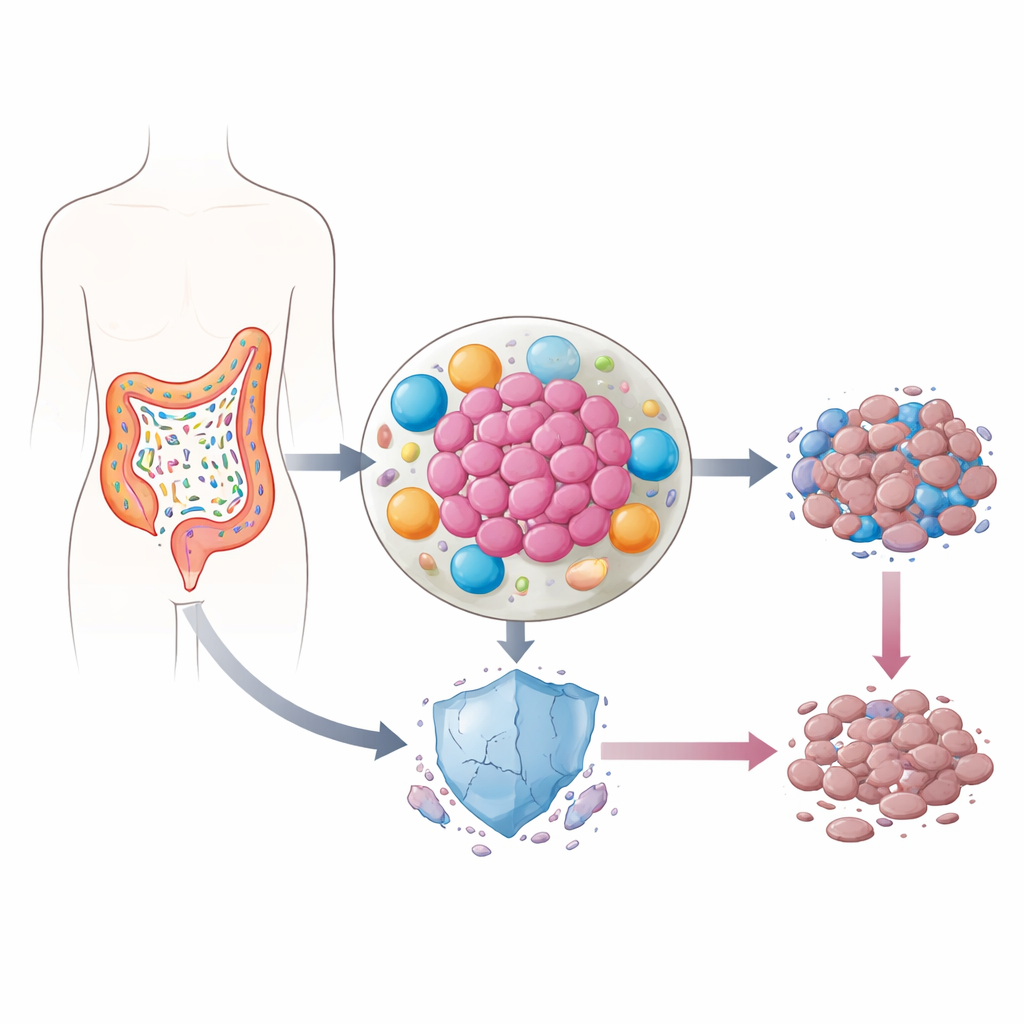
寄居于肿瘤内的微生物
我们的肠道栖息着万亿计细菌,其中大多数无害甚至有益。然而在结直肠癌中,菌群组成常发生变化。一些细菌会进入肿瘤本身,释放促炎分子并重塑包围癌细胞的细胞环境。先前的工作提示,在这些炎性病灶内,p53(一种常被称为“基因组守护者”的蛋白,能帮助受损细胞自我毁灭)的水平异常偏低。由于p53对癌细胞如何响应化疗至关重要,作者于是探问肠道细菌是否正在悄悄破坏这一防线。
环绕肿瘤细胞的隐秘支持网络
研究团队将注意力集中在脂多糖(LPS)上,这是一种强烈的促炎分子,存在于常见肠道微生物如克雷伯氏肺炎杆菌及其他肠杆菌科细菌的表面,而这类细菌在结直肠癌中常呈增多。出人意料的是,当他们将LPS直接加入结直肠癌细胞时,几乎没有变化:细胞并未变得更具耐药性,p53水平也保持不变。情形在先用LPS刺激免疫细胞(如巨噬细胞)或结缔组织细胞(如成纤维细胞),然后将这些细胞培养液转移给癌细胞时完全不同。在这种条件下,化疗导致的肿瘤细胞死亡大幅减少,p53蛋白在治疗后无法像正常那样积累。
装在微小囊泡中的信号
为弄清巨噬细胞传出的是什么,研究者使用先进的蛋白质组分析,绘制了在同时接受化疗与LPS刺激的巨噬细胞分泌物处理后,癌细胞内数千项变化的图谱。他们看到清晰的模式:与炎症和免疫激活相关的信号上调,而许多由p53控制、涉及细胞分裂与程序性细胞死亡的通路下调。进一步实验表明,这种抑制并非来自经典的促炎激素如白细胞介素-6。相反,关键信使是由被激活的巨噬细胞释放的小型膜性囊泡,即细胞外囊泡。当这些囊泡被分离并加入癌细胞时,p53蛋白被破坏性的去稳定化,并被细胞自身的回收机制更快地降解,从而保护细胞免受p53介导的死亡。
对“守护者”的选择性沉默
作者发现,这种由细菌-基质介导的信号并非在所有地方简单地关闭p53。相反,它选择性地压低一组由p53控制的基因,同时让其他基因——尤其是与炎症相关的基因——保持不变或甚至增强。当他们查看结直肠癌患者的肿瘤样本时,发现了匹配的模式:在炎症相关基因表达较高的肿瘤中,这一“p53活性”基因簇往往较低,尤其是在仍携带完整TP53基因的癌症中。重要的是,那些肿瘤中该p53依赖基因簇表达较强的患者,在化疗中的预后往往更好;这提示肿瘤内炎性环境对p53的非遗传性沉默可能会导致临床结局更差。
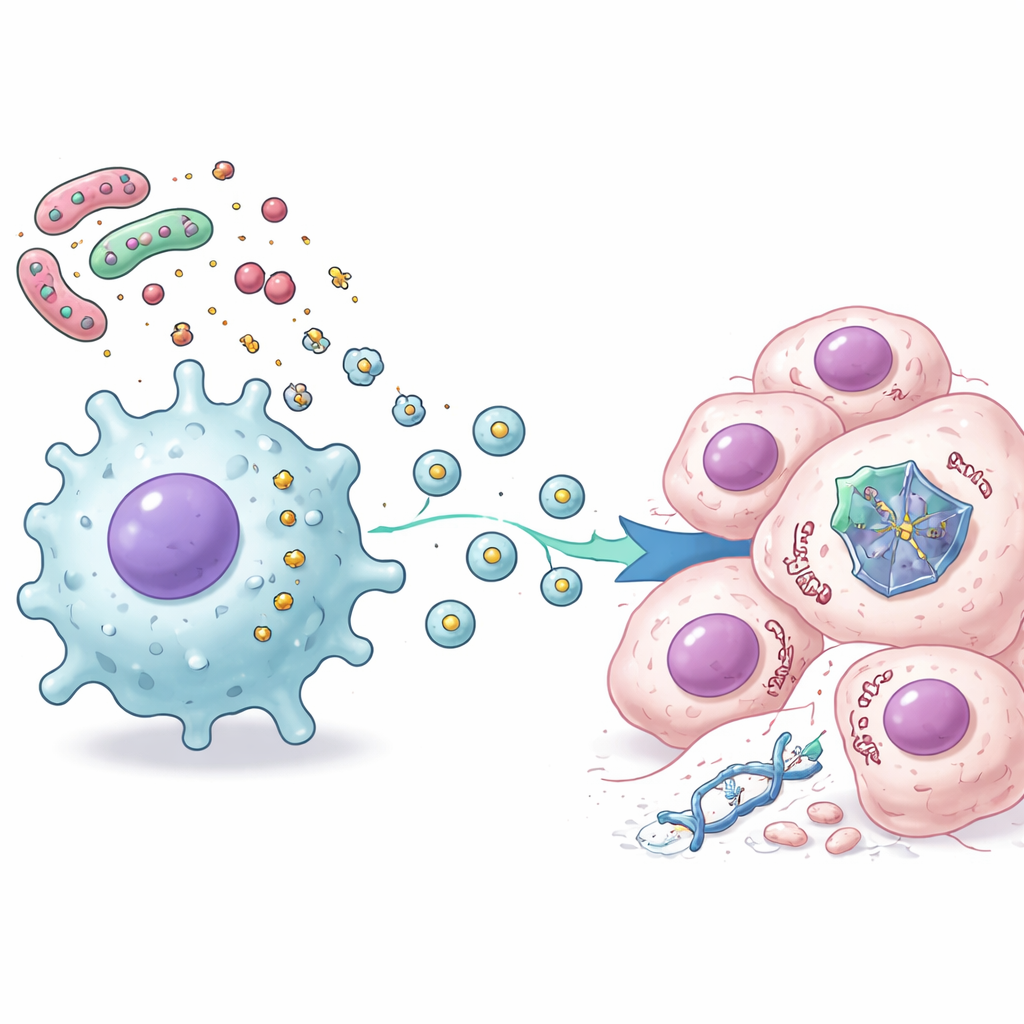
对患者与治疗的意义
综上所述,这项工作揭示了一条将肠道细菌与化疗耐药联系起来的事件链:细菌LPS激活邻近的基质和免疫细胞,受激活的细胞释放细胞外囊泡,囊泡进入癌细胞使p53蛋白不稳定,并削弱其在治疗后决定生死的功能。即便p53基因本身正常,这种外来压力也能有效地使其保护作用沉默。对患者而言,这意味着肠道微生物组的状态与局部炎症可能有助于解释为何某些结直肠肿瘤对常规药物置之不理。未来,通过重塑肠道菌群、抑制有害炎症或阻断这些囊泡的产生或作用,或可帮助恢复p53的肿瘤抑制功能并提高现有化疗的疗效。
引用: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
关键词: 结直肠癌, 肠道微生物组, 化疗耐药, p53 肿瘤抑制因子, 肿瘤微环境