Clear Sky Science · pt
LPS de Klebsiella pneumoniae promove repressão estromal de p53 e quimiorresistência no câncer colorretal
Por que as bactérias do seu intestino importam para o tratamento do câncer
O câncer colorretal costuma ser tratado com fármacos quimioterápicos potentes, mas muitos tumores aprendem a sobreviver a esses ataques. Este estudo investiga um parceiro inesperado no problema: certas bactérias intestinais. Os pesquisadores mostram como moléculas desses micróbios podem enfraquecer silenciosamente uma das principais salvaguardas do corpo contra o câncer dentro dos tumores, tornando os tratamentos padrão menos eficazes — mesmo quando as próprias células cancerosas não são diretamente alcançadas pelas bactérias.
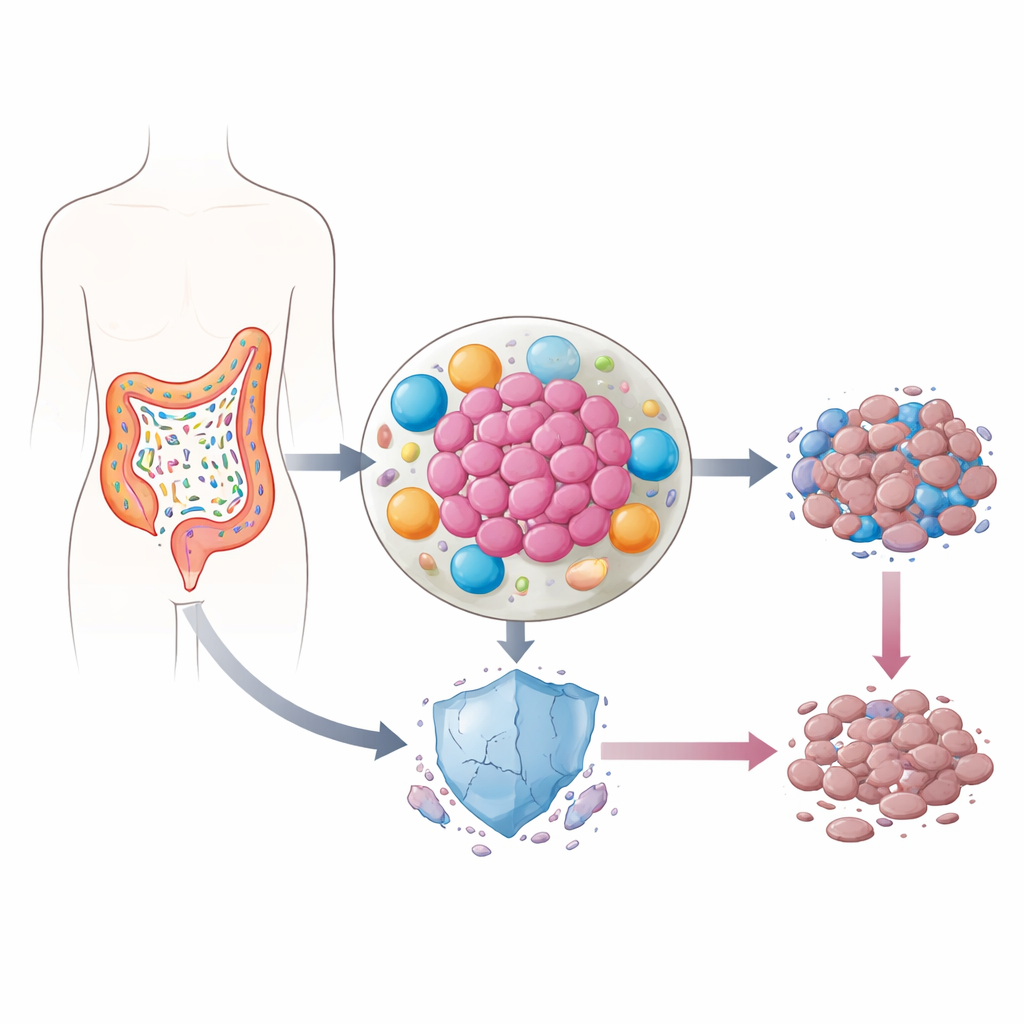
Germes vivendo dentro dos tumores
Nosso intestino abriga trilhões de bactérias, a maioria inofensiva ou mesmo benéfica. No entanto, no câncer colorretal, o equilíbrio de espécies frequentemente muda. Algumas bactérias migram para o próprio tumor, onde liberam moléculas inflamatórias e remodelam o ambiente de células que rodeiam o câncer. Trabalhos anteriores sugeriram que, nesses bolsões inflamados, os níveis de p53 — uma proteína frequentemente chamada de “guardião do genoma” por ajudar células danificadas a se autodestruírem — estão incomumente baixos. Como o p53 é crucial para a resposta das células cancerosas à quimioterapia, os autores perguntaram se bactérias intestinais poderiam estar saboteando silenciosamente essa defesa.
Uma rede de apoio oculta ao redor das células tumorais
A equipe concentrou-se no lipopolissacarídeo (LPS), uma molécula inflamatória potente encontrada na superfície de micróbios intestinais comuns, como Klebsiella pneumoniae e outras Enterobactérias, que frequentemente aumentam no câncer colorretal. Surpreendentemente, quando adicionaram LPS diretamente às células de câncer colorretal, quase nada aconteceu: as células não se tornaram mais resistentes a drogas e os níveis de p53 permaneceram os mesmos. O cenário mudou completamente quando expuseram primeiro células imunes chamadas macrófagos ou células do tecido conjuntivo chamadas fibroblastos ao LPS, e então transferiram o líquido em que essas células haviam crescido para as células cancerosas. Nessas condições, a quimioterapia matou muito menos células tumorais, e a proteína p53 não se acumulou como normalmente ocorreria após o tratamento.
Mensagens embaladas em minúsculas vesículas
Para entender o que os macrófagos estavam enviando, os pesquisadores utilizaram análises proteicas avançadas para mapear milhares de mudanças dentro das células cancerosas tratadas tanto com quimioterapia quanto com as secreções de macrófagos estimulados por LPS. Eles observaram um padrão claro: sinais relacionados à inflamação e ativação imune aumentaram, enquanto muitas vias controladas por p53 envolvidas na divisão celular e na autodestruição regulada diminuíram. Experimentos adicionais mostraram que essa supressão não decorria de hormônios inflamatórios clássicos como interleucina-6. Em vez disso, os mensageiros-chave eram pequenas bolhas de membrana, conhecidas como vesículas extracelulares, liberadas pelos macrófagos ativados. Quando essas vesículas foram isoladas e adicionadas às células cancerosas, a proteína p53 foi desestabilizada e degradada mais rapidamente pela maquinaria de reciclagem da própria célula, protegendo as células da morte mediada por p53.
Um silenciamento seletivo do guardião da célula
Os autores descobriram que esse sinal bacteriano–estromal não simplesmente desliga o p53 em todos os lugares. Ao contrário, ele atenua seletivamente um grupo de genes controlados por p53, enquanto outros — especialmente os ligados à inflamação — permanecem inalterados ou até aumentam. Ao examinarem amostras tumorais de pacientes com câncer colorretal, encontraram um padrão correspondente: em tumores onde assinaturas gênicas relacionadas à inflamação eram altas, esse conjunto de genes de “atividade de p53” tendia a ser baixo, particularmente em cânceres que ainda mantinham um gene TP53 intacto. Importante, pacientes cujos tumores apresentavam forte expressão desse conjunto dependente de p53 tenderam a responder melhor à quimioterapia do que aqueles com baixa expressão, sugerindo que o silenciamento não genético do p53 pelo ambiente tumoral inflamado pode agravar os desfechos clínicos.
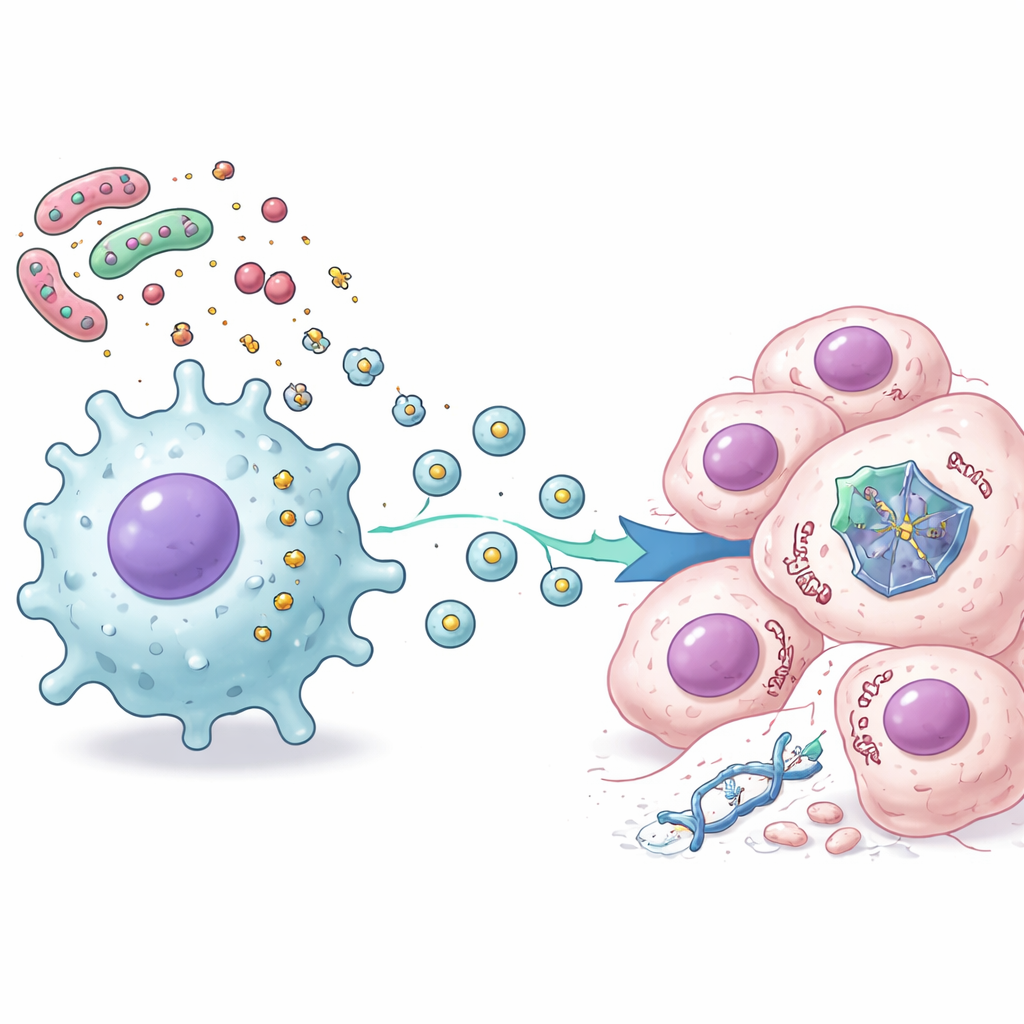
O que isso significa para pacientes e terapias
Em conjunto, o trabalho revela uma cadeia de eventos que conecta bactérias intestinais à resistência à quimioterapia: o LPS bacteriano ativa células estromais e imunes próximas, essas células liberam vesículas extracelulares, e as vesículas entram nas células cancerosas para desestabilizar a proteína p53 e atenuar suas decisões de vida ou morte após o tratamento. Mesmo quando o gene p53 em si é normal, essa pressão externa pode efetivamente silenciar seu papel protetor. Para os pacientes, isso sugere que o estado do microbioma intestinal e da inflamação local pode ajudar a explicar por que alguns tumores colorretais resistem aos fármacos padrão. No futuro, estratégias que redesenhem as bactérias intestinais, acalmem inflamações nocivas ou bloqueiem a produção ou ação dessas vesículas podem ajudar a restaurar o poder supressor tumoral do p53 e tornar as quimioterapias existentes mais eficazes.
Citação: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Palavras-chave: câncer colorretal, microbioma intestinal, resistência à quimioterapia, supressor tumoral p53, microambiente tumoral