Clear Sky Science · pl
LPS Klebsiella pneumoniae powoduje stromalne tłumienie p53 i oporność na chemioterapię w raku jelita grubego
Dlaczego bakterie jelitowe mają znaczenie dla leczenia nowotworów
Rak jelita grubego jest zwykle leczony silnymi lekami chemioterapeutycznymi, ale wiele guzów uczy się przeżywać te ataki. Badanie to bada niespodziewanego wspólnika przestępstwa: niektóre bakterie jelitowe. Autorzy pokazują, jak cząsteczki pochodzące od tych drobnoustrojów mogą po cichu osłabiać jedno z głównych mechanizmów obronnych organizmu przeciw rakowi wewnątrz guza, czyniąc standardowe terapie mniej skutecznymi — nawet gdy same komórki nowotworowe nie są bezpośrednio zainfekowane przez bakterie.
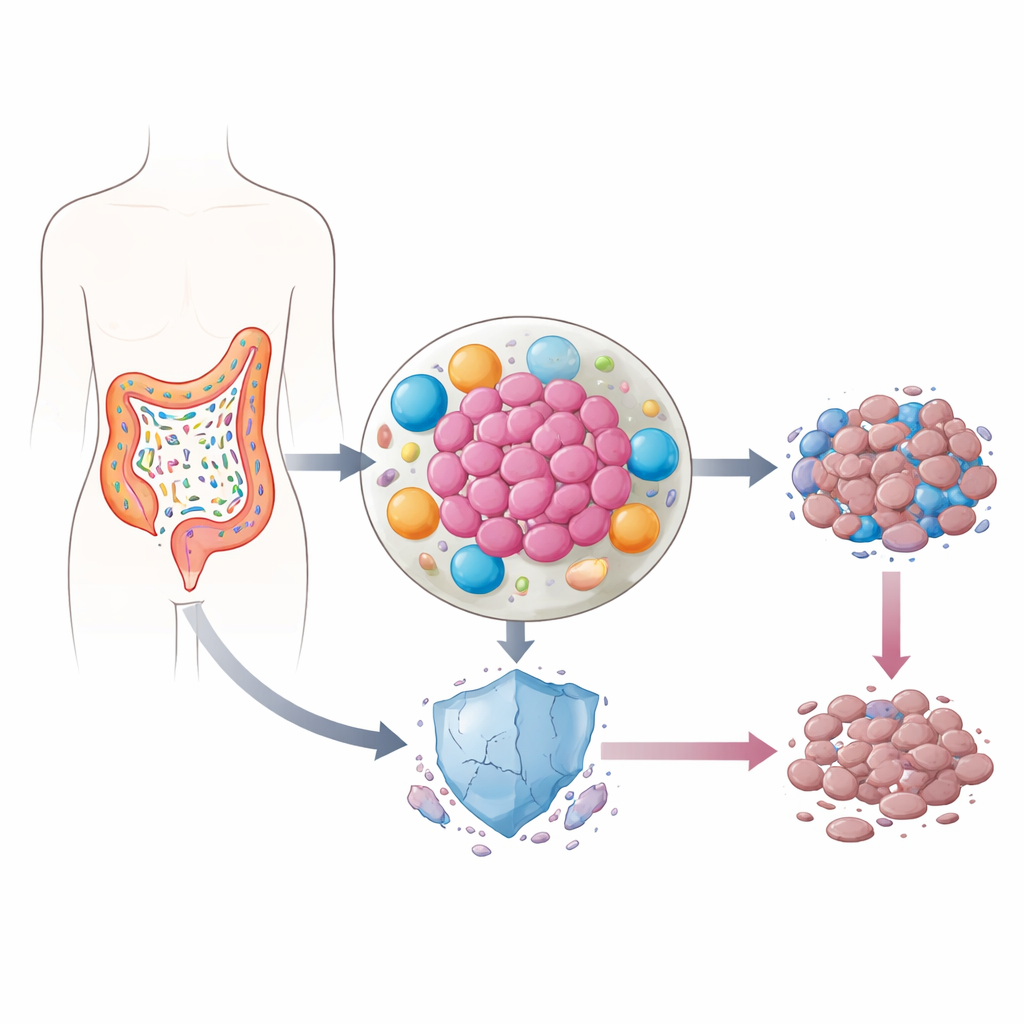
Germy żyjące wewnątrz guzów
Nasze jelita są domem dla bilionów bakterii, z których większość jest nieszkodliwa lub nawet korzystna. W raku jelita grubego równowaga gatunków często jednak się zmienia. Niektóre bakterie przemieszczają się do samego guza, gdzie uwalniają zapalne molekuły i przekształcają sąsiedztwo komórek otaczających nowotwór. Wcześniejsze badania sugerowały, że w tych zapalnych „kieszeniach” poziomy p53 — białka często nazywanego „strażnikiem genomu”, ponieważ pomaga uszkodzonym komórkom ulegać samozniszczeniu — są nietypowo niskie. Ponieważ p53 jest kluczowe dla odpowiedzi komórek nowotworowych na chemioterapię, autorzy postawili pytanie, czy bakterie jelitowe mogą potajemnie sabotować tę ochronę.
Ukryta sieć wsparcia wokół komórek guza
Zespół skoncentrował się na lipopolisacharydzie (LPS), silnej molekule zapalnej znajdującej się na powierzchni powszechnych drobnoustrojów jelitowych, takich jak Klebsiella pneumoniae i inne Enterobacteria, które często są zwiększone w raku jelita grubego. Ku zaskoczeniu, gdy dodano LPS bezpośrednio do komórek raka jelita grubego, niewiele się stało: komórki nie stały się bardziej oporne na leki, a poziomy p53 pozostały bez zmian. Obraz zmienił się całkowicie, gdy najpierw poddano na działanie LPS komórki odpornościowe zwane makrofagami lub komórki tkanki łącznej zwane fibroblastami, a następnie przeniesiono do komórek nowotworowych płyn, w którym te komórki rosły. W takich warunkach chemioterapia zabiła znacznie mniej komórek guza, a białko p53 nie zgromadziło się tak, jak zwykle po leczeniu.
Wiadomości zapakowane w maleńkie pęcherzyki
Aby zrozumieć, co wysyłają makrofagi, badacze użyli zaawansowanej analizy białek, aby wyznaczyć tysiące zmian w komórkach nowotworowych traktowanych zarówno chemioterapią, jak i wydzielinami makrofagów pobudzonych LPS. Zaobserwowali wyraźny wzorzec: sygnały związane z zapaleniem i aktywacją układu odpornościowego wzrosły, podczas gdy wiele szlaków kontrolowanych przez p53 związanych z podziałem komórkowym i programowaną śmiercią komórkową osłabło. Dalsze eksperymenty wykazały, że to tłumienie nie wynikało z klasycznych hormonów zapalnych, takich jak interleukina-6. Zamiast tego kluczowymi posłańcami okazały się maleńkie pęcherzyki błonowe, znane jako zewnątrzkomórkowe pęcherzyki, uwalniane przez aktywowane makrofagi. Gdy te pęcherzyki zostały wyizolowane i dodane do komórek nowotworowych, białko p53 ulegało destabilizacji i szybszemu niszczeniu przez wewnętrzne mechanizmy recyklingu komórkowego, chroniąc komórki przed śmiercią zależną od p53.
Selektywne wyciszanie strażnika komórkowego
Autorzy odkryli, że ten bakteryjno-stromalny sygnał nie wyłącza p53 wszędzie na oślep. Raczej selektywnie tłumi jedną grupę genów kontrolowanych przez p53, przy pozostawieniu innych — zwłaszcza powiązanych z zapaleniem — niezmienionych lub nawet wzmocnionych. Analiza próbek guzów od pacjentów z rakiem jelita grubego wykazała pasujący wzorzec: w guzach, gdzie sygnatury genów związanych z zapaleniem były wysokie, klaster genów związanych z „aktywnym p53” miał tendencję do niskiego poziomu, szczególnie w nowotworach, które nadal miały nienaruszony gen TP53. Co ważne, pacjenci, których guzy wykazywały silną ekspresję tego klastra zależnego od p53, mieli tendencję do lepszych wyników leczenia chemioterapią niż ci z niską ekspresją, co sugeruje, że pozagenetyczne wyciszanie p53 przez zapalne mikrośrodowisko guza może pogarszać rokowania kliniczne.
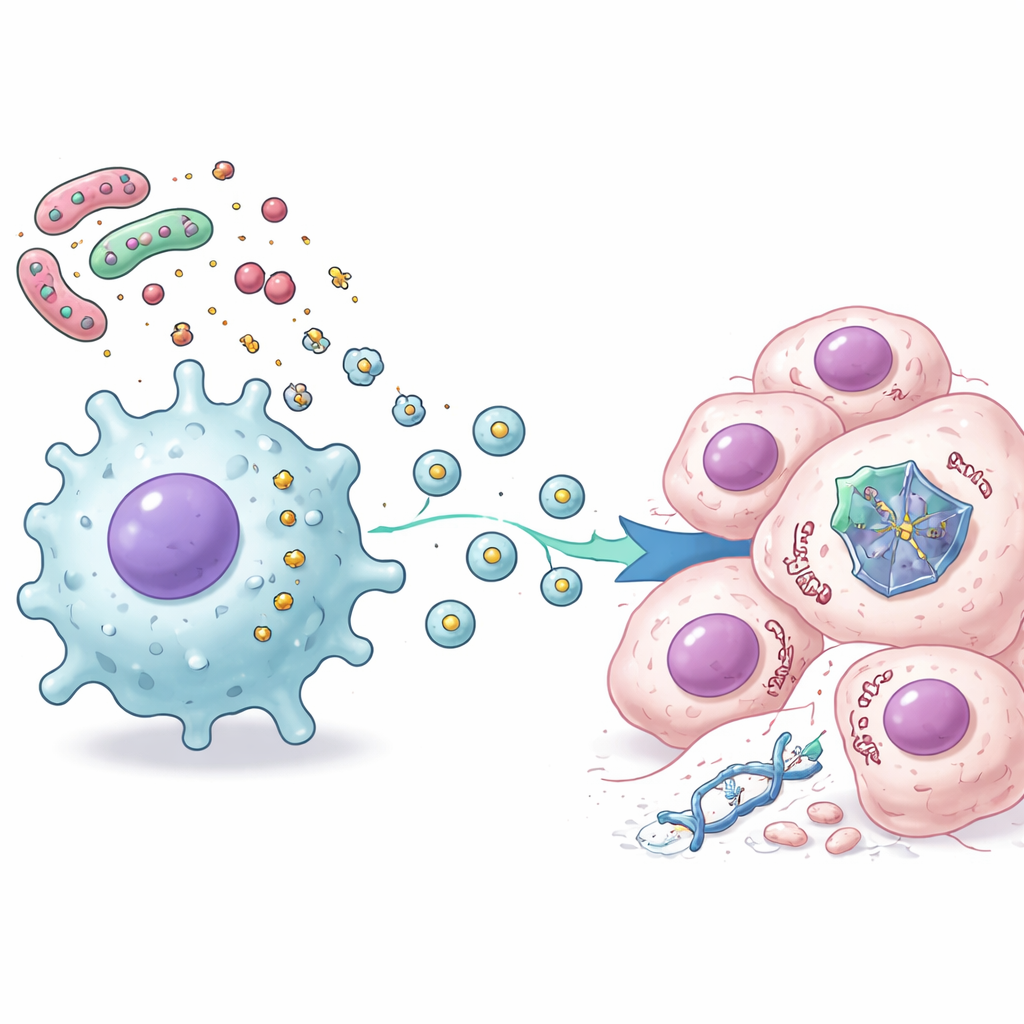
Co to oznacza dla pacjentów i terapii
Podsumowując, praca ujawnia łańcuch zdarzeń łączący bakterie jelitowe z opornością na chemioterapię: bakteryjny LPS aktywuje pobliskie komórki stromalne i odpornościowe, te komórki wydzielają zewnątrzkomórkowe pęcherzyki, a pęcherzyki wnikają do komórek nowotworowych, destabilizując białko p53 i osłabiając jego decyzje o życiu lub śmierci po leczeniu. Nawet gdy gen p53 jest prawidłowy, zewnętrzny nacisk może skutecznie wyciszyć jego ochronną rolę. Dla pacjentów sugeruje to, że stan mikrobiomu jelitowego i lokalne zapalenie mogą pomóc wyjaśnić, dlaczego niektóre nowotwory jelita grubego opierają się standardowym lekom. W przyszłości strategie zmieniające skład bakterii jelitowych, łagodzące szkodliwe zapalenie lub blokujące produkcję bądź działanie tych pęcherzyków mogą pomóc przywrócić antynowotworową funkcję p53 i zwiększyć skuteczność istniejących chemioterapii.
Cytowanie: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Słowa kluczowe: rak jelita grubego, mikrobiom jelitowy, oporność na chemioterapię, białko supresorowe p53, mikrośrodowisko guza