Clear Sky Science · nl
Klebsiella pneumoniae LPS veroorzaakt stromale onderdrukking van p53 en chemoresistentie bij colorectale kanker
Waarom je darmbacteriën ertoe doen bij kankerbehandeling
Colorectale kanker wordt meestal behandeld met krachtige chemotherapeutische middelen, maar veel tumoren leren deze aanvallen te weerstaan. Deze studie onderzoekt een onverwachte medeplichtige: bepaalde darmbacteriën. De onderzoekers tonen aan hoe moleculen van deze microben een van de belangrijkste beschermers tegen kanker in het lichaam binnen tumoren stilletjes kunnen verzwakken, waardoor standaardbehandelingen minder effectief zijn—zelfs wanneer de kankercellen zelf niet rechtstreeks door de bacteriën worden aangeraakt.
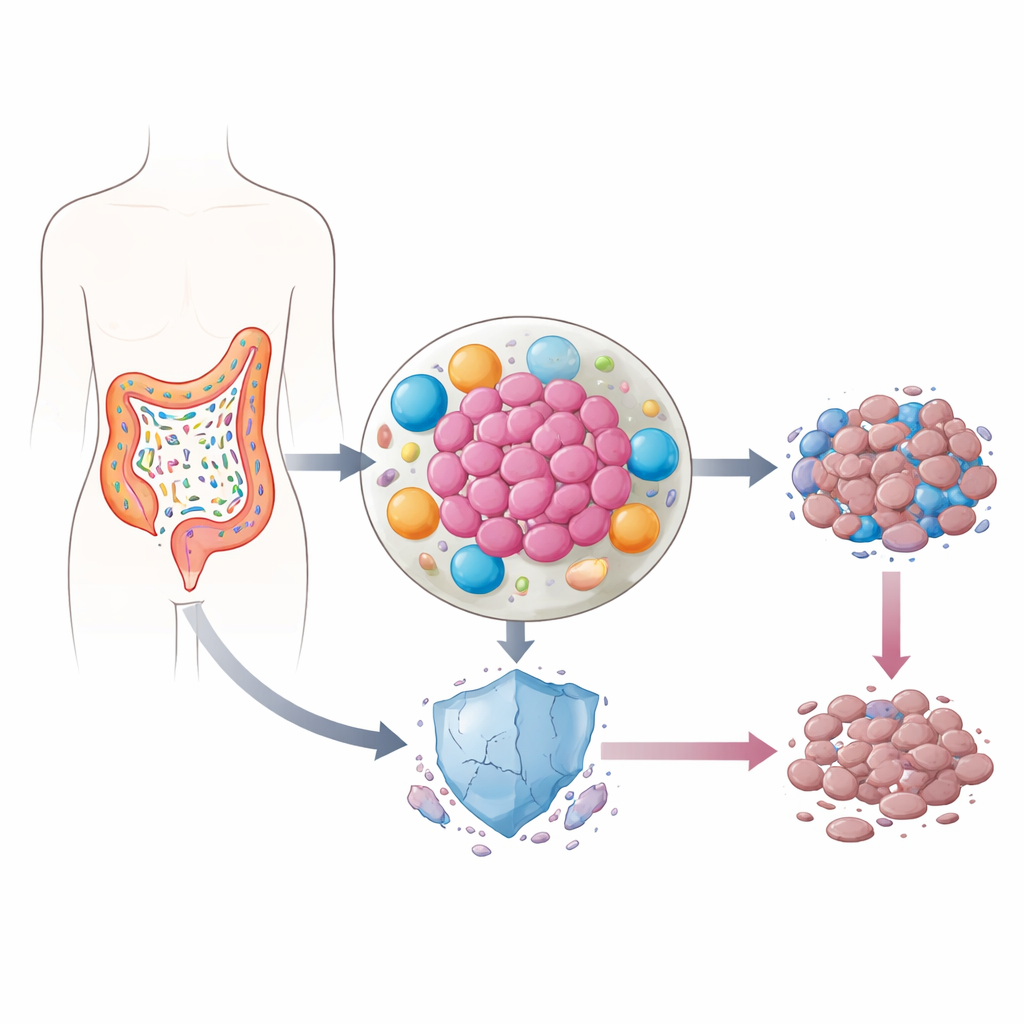
Bacteriën die in tumoren leven
Onze darmen herbergen biljoenen bacteriën, de meesten onschadelijk of zelfs nuttig. Bij colorectale kanker verschuift die balans echter vaak van soorten. Sommige bacteriën trekken in de tumor zelf, waar ze ontstekingsbevorderende moleculen afgeven en de omgeving van cellen rondom de kanker herschikken. Eerder werk suggereerde dat in deze ontstoken pockets de niveaus van p53—een eiwit dat vaak de “beschermer van het genoom” wordt genoemd omdat het beschadigde cellen helpt zichzelf te laten afsterven—ongewoon laag zijn. Omdat p53 cruciaal is voor hoe kankercellen op chemotherapie reageren, vroegen de auteurs zich af of darmbacteriën dit schild stilletjes konden saboteren.
Een verborgen ondersteuningsnetwerk rondom tumorcellen
Het team richtte zich op lipopolysacharide (LPS), een sterk ontstekingsmolecuul dat op het oppervlak voorkomt van veel voorkomende darmmicroben zoals Klebsiella pneumoniae en andere Enterobacteriaceae, die vaak verhoogd zijn bij colorectale kanker. Verrassend genoeg gebeurde er weinig wanneer ze LPS rechtstreeks aan colorectale kankercellen toevoegden: de cellen werden niet duidelijk resistenter tegen geneesmiddelen en p53-niveaus bleven gelijk. Het beeld veranderde volledig toen ze eerst immuuncellen genaamd macrofagen of bindweefselcellen genaamd fibroblasten aan LPS blootstelden, en vervolgens de vloeistof waarin deze cellen hadden gegroeid naar de kankercellen overbrachten. Onder deze omstandigheden werden veel minder tumorcellen door chemotherapie gedood en bouwde het p53-eiwit zich na behandeling niet op zoals normaal.
Boodschappen verpakt in kleine blaasjes
Om te begrijpen wat macrofagen uitzonden, gebruikten de onderzoekers geavanceerde proteïneanalyses om duizenden veranderingen in kaart te brengen in kankercellen die zowel met chemotherapie als met door LPS-geactiveerde macrofagen geproduceerde secreties werden behandeld. Ze zagen een duidelijk patroon: signalen gerelateerd aan ontsteking en immuunactivatie namen toe, terwijl veel p53-gestuurde routes betrokken bij celdeling en gecontroleerde zelfdestructie afnamen. Verdere experimenten toonden aan dat deze onderdrukking niet voortkwam uit klassieke ontstekingshormonen zoals interleukine-6. In plaats daarvan waren de sleutelboodschappers kleine membraanblaasjes, bekend als extracellulaire vesikels, vrijgegeven door de geactiveerde macrofagen. Wanneer deze vesikels werden geïsoleerd en aan kankercellen werden toegevoegd, raakte het p53-eiwit gedestabiliseerd en sneller afgebroken door het eigen recyclingmechanisme van de cel, waardoor de cellen werden afgeschermd tegen p53-gedreven celdood.
Een selectieve demping van de beschermer van de cel
De auteurs ontdekten dat dit bacterie–stromale signaal p53 niet overal simpelweg uitschakelt. Het dempt eerder selectief één groep p53-gestuurde genen, terwijl andere—vooral die gekoppeld aan ontsteking—onveranderd blijven of zelfs worden versterkt. Toen ze naar tumorstalen van patiënten met colorectale kanker keken, vonden ze een overeenkomstig patroon: in tumoren waar ontstekingsgerelateerde genexpressies hoog waren, was deze “p53-activiteits” gencluster vaak laag, vooral in kankers die nog een intact TP53-gen hadden. Belangrijk is dat patiënten waarvan de tumoren een sterke expressie van deze p53-afhankelijke cluster vertoonden, over het algemeen beter reageerden op chemotherapie dan zij met lage expressie, wat suggereert dat niet-genetische demping van p53 door de ontstoken tumorumgeving de klinische uitkomst kan verslechteren.
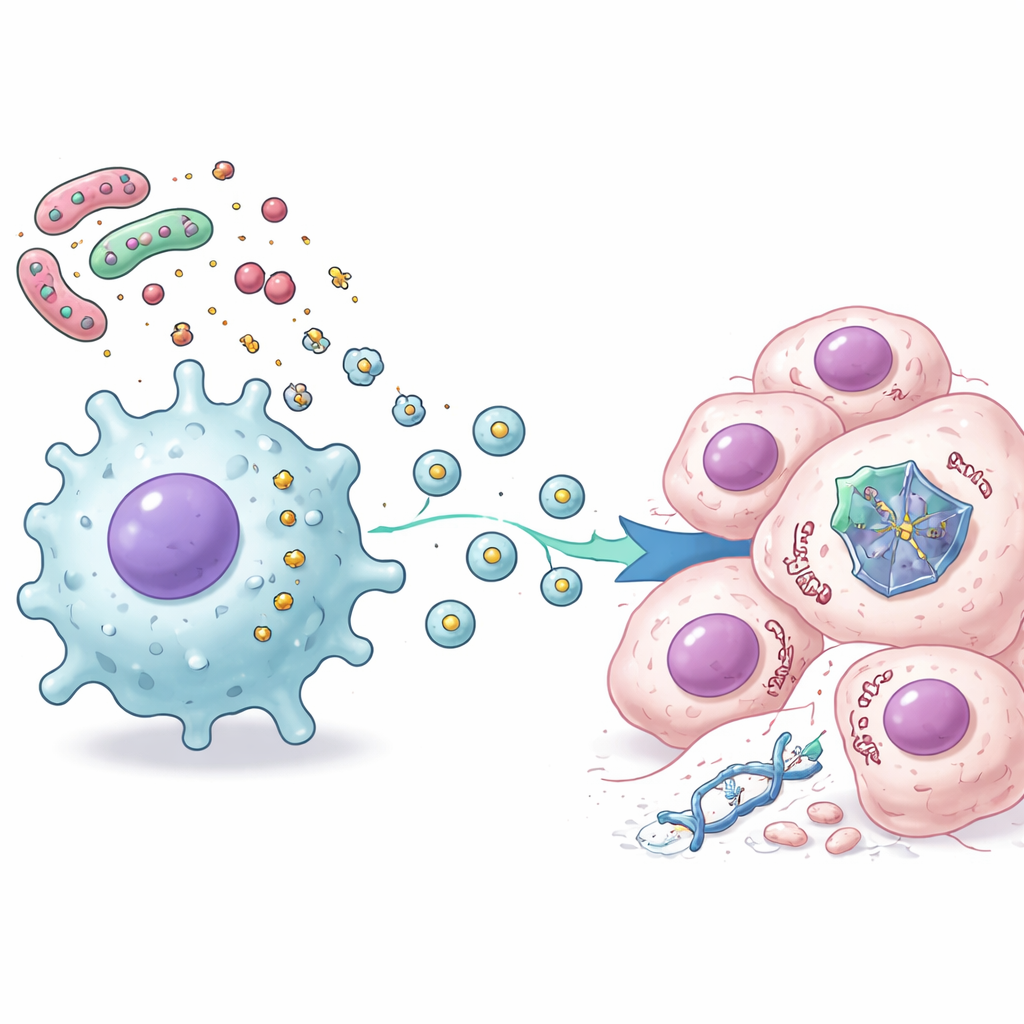
Wat dit betekent voor patiënten en therapieën
Alles bij elkaar onthult het werk een keten van gebeurtenissen die darmbacteriën koppelt aan chemoresistentie: bacterieel LPS activeert nabijgelegen stromale en immuuncellen, deze cellen geven extracellulaire vesikels af, en de vesikels dringen tumorcellen binnen om het p53-eiwit te destabiliseren en diens beslissingen over leven of dood na behandeling af te zwakken. Zelfs wanneer het p53-gen zelf normaal is, kan deze externe druk zijn beschermende rol effectief dempen. Voor patiënten suggereert dit dat de staat van het darmmicrobioom en lokale ontsteking kunnen helpen verklaren waarom sommige colorectale tumoren standaardmiddelen weerstaan. In de toekomst kunnen strategieën die het darmmicrobioom herschikken, schadelijke ontsteking kalmeren of de productie of werking van deze vesikels blokkeren, mogelijk helpen p53’s tumorsuppressieve kracht te herstellen en bestaande chemotherapieën beter te laten werken.
Bronvermelding: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Trefwoorden: colorectale kanker, darmmicrobioom, resistentie tegen chemotherapie, tumorsuppressor p53, tumormicro-omgeving