Clear Sky Science · sv
Klebsiella pneumoniae LPS driver stromalmedierad repression av p53 och kemoresistens vid kolorektal cancer
Varför dina tarmbakterier spelar roll för cancerbehandling
Kolorektalcancer behandlas ofta med kraftfulla cellgifter, men många tumörer lär sig att överleva dessa angrepp. Den här studien undersöker en oväntad medhjälpare: vissa tarmbakterier. Forskarna visar hur molekyler från dessa mikrober tyst kan försvaga en av kroppens viktigaste cancerbekämpande garantier inne i tumörer, vilket gör standardbehandlingar mindre effektiva — även när cancercellerna själva inte direkt berörs av bakterierna.
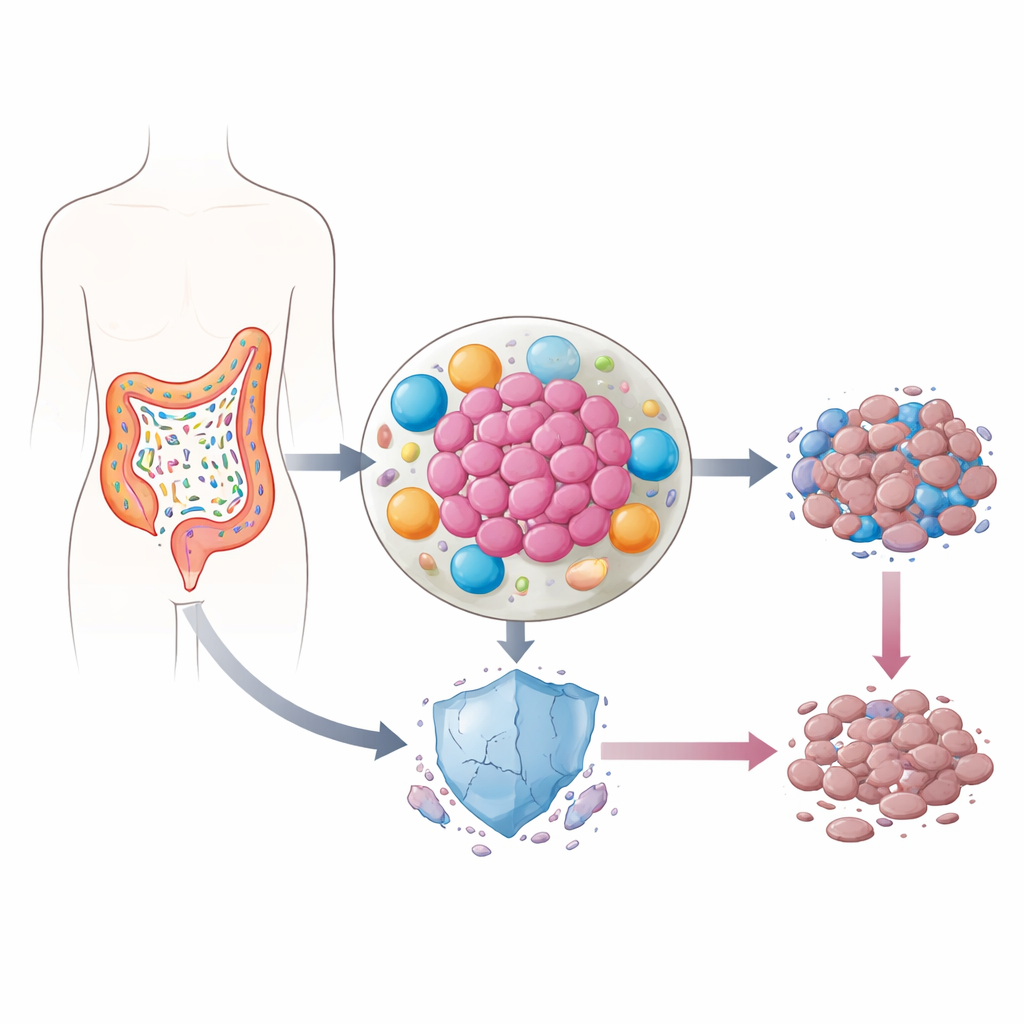
Bakterier som lever inne i tumörer
Våra tarmar hyser biljoner bakterier, de flesta ofarliga eller till och med hjälpsamma. Vid kolorektalcancer förändras dock ofta artbalansen. Vissa bakterier flyttar in i tumören, där de släpper ut inflammatoriska molekyler och omformar grannskapet av celler som omger cancern. Tidigare arbete antydde att nivåerna av p53 — ett protein ofta kallat ”genomets väktare” eftersom det hjälper skadade celler att självdestruera — är ovanligt låga i dessa inflammerade fickor. Eftersom p53 är avgörande för hur cancerceller svarar på kemoterapi, frågade författarna om tarmbakterier tyst kan sabotera denna försvarsfunktion.
Ett dolt stödnätverk runt tumörcellerna
Teamet fokuserade på lipopolysackarid (LPS), en stark inflammatorisk molekyl som finns på ytan av vanliga tarmmikrober som Klebsiella pneumoniae och andra Enterobacteria, vilka ofta är ökade vid kolorektalcancer. Överraskande nog hände nästan ingenting när de tillsatte LPS direkt till kolorektala cancerceller: cellerna blev inte mer drogresistenta och p53-nivåerna förblev oförändrade. Bilden förändrades helt när de först exponerade immunceller kallade makrofager eller bindvävsceller kallade fibroblaster för LPS, och sedan överförde vätskan som dessa celler odlats i till cancercellerna. Under dessa förhållanden dödade kemoterapin långt färre tumörceller, och p53-protein byggdes inte upp som det normalt skulle göra efter behandling.
Budskap paketerade i små vesiklar
För att förstå vad makrofagerna skickade använde forskarna avancerad proteomanalys för att kartlägga tusentals förändringar inne i cancerceller behandlade med både kemoterapi och sekret från LPS-stimulerade makrofager. De såg ett tydligt mönster: signaler kopplade till inflammation och immunaktivering ökade, medan många p53-styrda vägar som är involverade i celldelning och kontrollerad självdestruktion minskade. Ytterligare experiment visade att denna dämpning inte berodde på klassiska inflammatoriska hormoner som interleukin-6. Istället var de viktiga budbärarna små membranblåsor, kända som extracellulära vesiklar, som frigjordes av de aktiverade makrofagerna. När dessa vesiklar isolerades och tillsattes till cancerceller destabiliserades p53-proteinet och bröts snabbare ned av cellens eget återvinningssystem, vilket skyddade cellerna från p53-driven celldöd.
En selektiv tystnad av cellens väktare
Författarna upptäckte att denna bakterie–stromala signal inte helt enkelt släcker av p53 överallt. Snarare dämpar den selektivt en grupp p53-reglerade gener, samtidigt som andra — särskilt de kopplade till inflammation — lämnas oförändrade eller till och med förstärkta. När de undersökte tumörprover från patienter med kolorektalcancer fann de ett matchande mönster: i tumörer där inflammationsrelaterade gen-signaturer var höga tenderade denna ”p53-aktivitet” genkluster att vara låg, särskilt i cancerformer som fortfarande bar en intakt TP53-gen. Viktigt är att patienter vars tumörer hade stark uttryck av detta p53-beroende kluster ofta klarade sig bättre med kemoterapi än de med lågt uttryck, vilket tyder på att icke-genetisk tystning av p53 av en inflammerad tumörmiljö kan förvärra kliniska utfall.
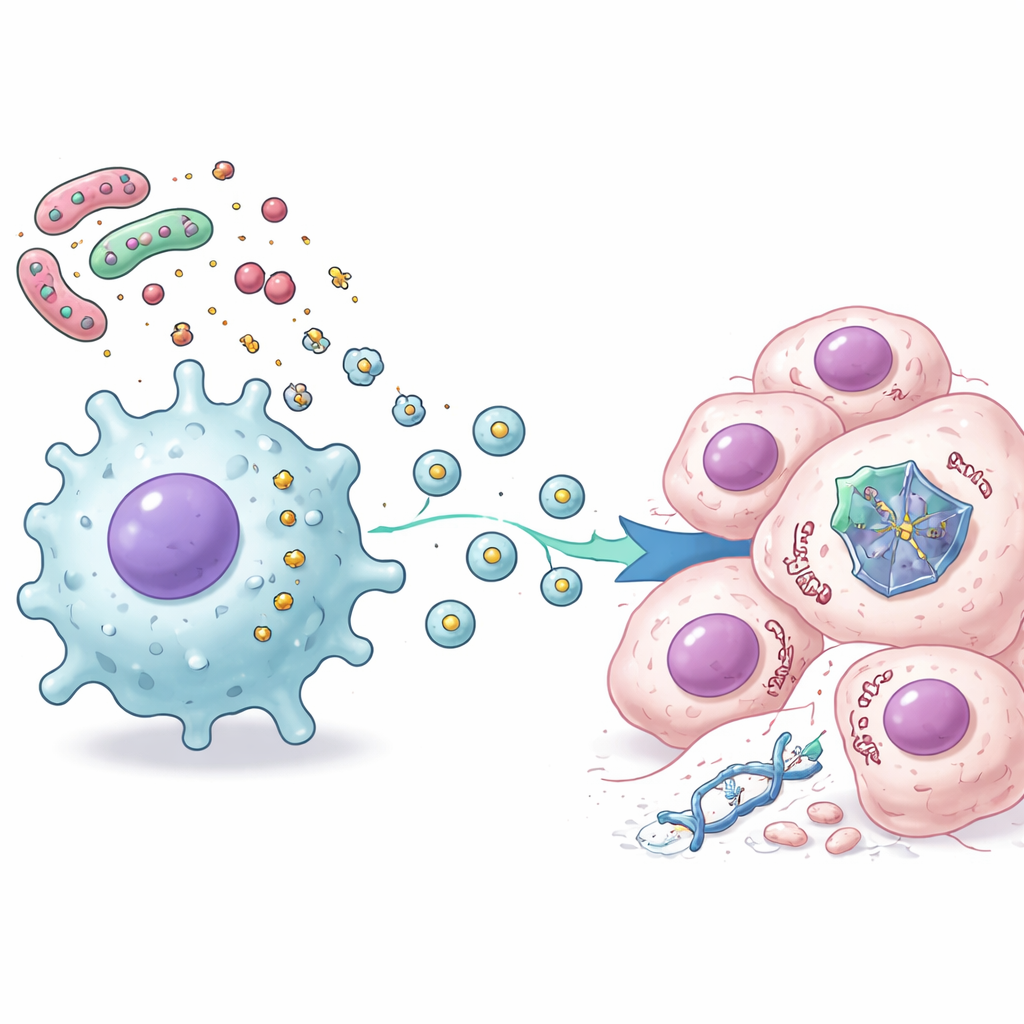
Vad detta betyder för patienter och behandlingar
Sammantaget avslöjar arbetet en händelsekedja som kopplar tarmbakterier till kemoterapiresistens: bakteriell LPS aktiverar närliggande stromala och immunceller, dessa celler frigör extracellulära vesiklar, och vesiklarna tar sig in i cancerceller för att destabilisera p53-protein och dämpa dess liv-eller-död-beslut efter behandling. Även när p53-genen själv är normal kan detta yttre tryck effektivt tysta dess skyddande roll. För patienter antyder detta att tillståndet i tarmmikrobiomet och lokal inflammation kan hjälpa förklara varför vissa kolorektala tumörer avvisar standardläkemedel. Framöver kan strategier som omformar tarmbakterier, lugnar skadlig inflammation eller blockerar produktionen eller verkan av dessa vesiklar bidra till att återställa p53:s tumörsuppressiva kraft och göra befintliga kemoterapier mer effektiva.
Citering: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
Nyckelord: kolorektalcancer, tarmmikrobiom, kemoterapiresistens, p53 tumörsuppressor, tumörmikromiljö