Clear Sky Science · ar
دور LPS الخاص بـ Klebsiella pneumoniae في قمع p53 بواسطة النسج المحيطة ومقاومة السرطان القولوني المستقيمي للعلاج الكيميائي
لماذا تهم بكتيريا أمعائك لعلاج السرطان
عادة ما يُعالج سرطان القولون والمستقيم بأدوية كيميائية قوية، لكن العديد من الأورام تتعلم كيف تبقى على قيد الحياة أمام هذه الهجمات. تستكشف هذه الدراسة شريكاً غير متوقع في التواطؤ: بعض بكتيريا الأمعاء. يوضح الباحثون كيف يمكن لمركبات من هذه الميكروبات أن تضعف بصمت أحد أهم أدوات الجسم لمكافحة السرطان داخل الأورام، مما يجعل العلاجات القياسية أقل فاعلية — حتى عندما لا تتعرض خلايا السرطان نفسها للبكتيريا مباشرة.
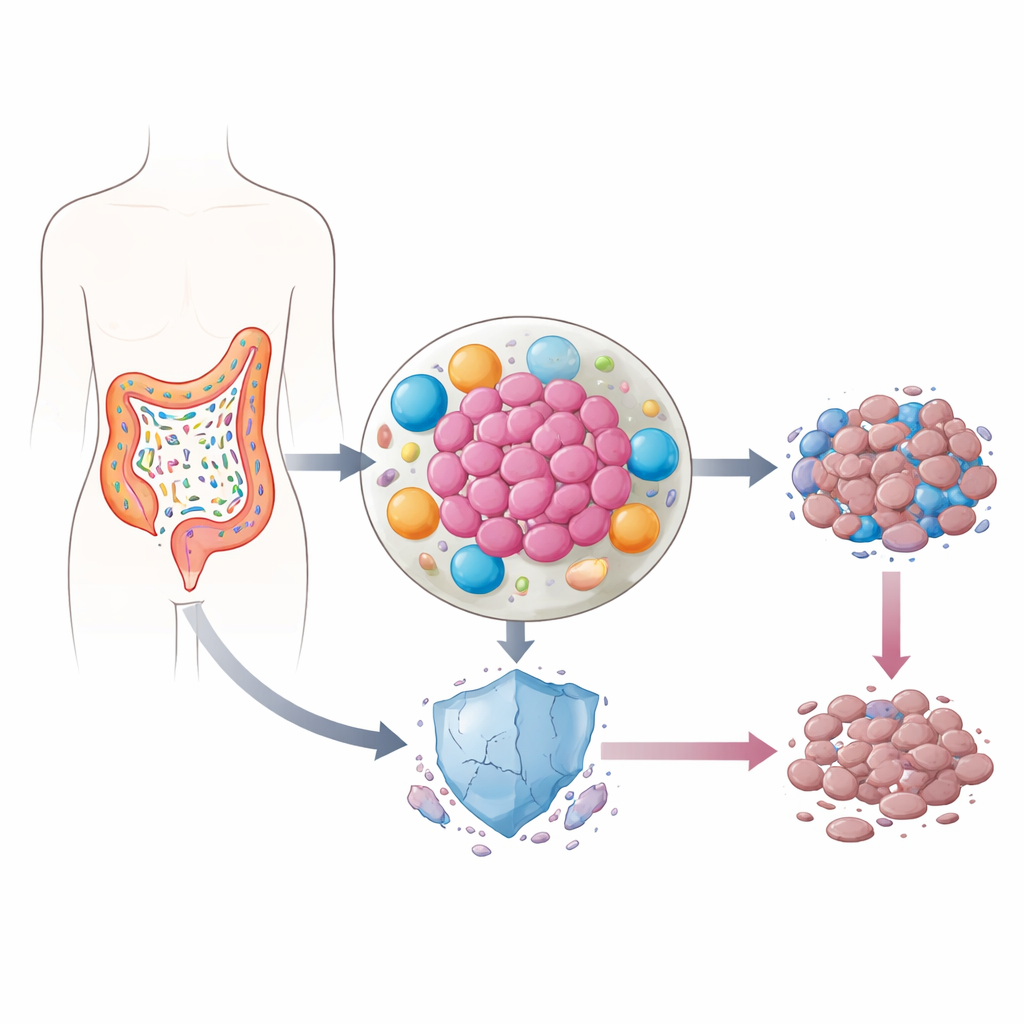
جراثيم تعيش داخل الأورام
تعيش أمعاؤنا على تريليونات من البكتيريا، معظمها غير ضار أو حتى مفيد. لكن في سرطان القولون والمستقيم، غالباً ما يتغير توازن الأنواع. تنتقل بعض البكتيريا إلى داخل الورم ذاته، حيث تطلق جزيئات مسببة للالتهاب وتُعيد تشكيل محيط الخلايا المحيطة بالسرطان. أشارت أعمال سابقة إلى أن مستويات p53 — وهو بروتين يُسمى غالباً «حارس الجينوم» لأنه يساعد الخلايا التالفة على الانتحار المبرمج — تكون منخفضة بشكل غير عادي في هذه الجيوب الملتهبة. ونظراً إلى أهمية p53 في استجابة خلايا السرطان للعلاج الكيميائي، تساءل المؤلفون عما إذا كانت بكتيريا الأمعاء قد تكون تقوم بتخريب هذا الحاجز بصمت.
شبكة دعم خفية حول خلايا الورم
ركز الفريق على الليبوبوليساكاريد (LPS)، وهو جزيء ملتهب قوي يوجد على سطح ميكروبات الأمعاء الشائعة مثل Klebsiella pneumoniae وأنواع أخرى من الإنتعربكتيريا، والتي تزداد عادة في سرطان القولون والمستقيم. بشكل مدهش، عندما أضافوا LPS مباشرة إلى خلايا سرطان القولون والمستقيم، لم يحدث الكثير: لم تصبح الخلايا أكثر مقاومة للأدوية وبقيت مستويات p53 كما هي. تغيرت الصورة تماماً عندما عرضوا أولاً خلايا مناعية تُدعى البلاعم أو خلايا نسيج ضام تُدعى الليفيات لـ LPS، ثم نقلوا السائل الذي نمت فيه هذه الخلايا إلى خلايا السرطان. في ظل هذه الظروف، قتل العلاج الكيميائي عدداً أقل بكثير من خلايا الورم، وفشل بروتين p53 في التراكم كما يفعل عادة بعد المعالجة.
رسائل مُغلفة في حويصلات دقيقة
لفهم ما كانت ترسله البلاعم، استخدم الباحثون تحليلاً بروتينياً متقدماً لرسم آلاف التغيرات داخل خلايا السرطان المعالجة كيميائياً والمُعرّضة أيضاً لإفرازات البلاعم المنشطّة بـ LPS. لاحظوا نمطاً واضحاً: ارتفعت الإشارات المرتبطة بالالتهاب وتنشيط المناعة، بينما انخفضت العديد من المسارات الخاضعة لتحكم p53 والمشاركة في انقسام الخلايا والانتحار المبرمج. أظهرت تجارب إضافية أن هذا الكبت لم ينشأ عن هرمونات التهابية كلاسيكية مثل الإنترلوكين-6. بل كانت الرسل المفتاحية فقاعات غشائية صغيرة تُسمى الحويصلات خارج الخلوية، التي تطلقها البلاعم المنشطّة. عندما عُزلت هذه الحويصلات وأضيفت إلى خلايا السرطان، تزعزع استقرار بروتين p53 وتدمره الخلية بسرعة أكبر عبر آليات التدوير الخلوية، فتصبح الخلايا محمية من موت موجه بـ p53.
إسكات انتقائي لحارس الخلية
اكتشف المؤلفون أن إشارة البكتيريا-النسيج هذه لا تقوم ببساطة بإيقاف p53 في كل مكان. بل تُخَمّد بشكل انتقائي مجموعة معينة من الجينات الخاضعة لتحكم p53، بينما تترك مجموعات أخرى — خاصة المرتبطة بالالتهاب — بدون تغيير أو حتى معززة. عند فحص عينات أورام من مرضى سرطان القولون والمستقيم، وجدوا نمطاً مطابقاً: في الأورام التي كانت فيها بصمات الجينات المرتبطة بالالتهاب مرتفعة، كانت مجموعة جينات «نشاط p53» منخفضة، لا سيما في السرطانات التي لا تزال تحتفظ بجين TP53 سليم. والأهم من ذلك، أن المرضى الذين أظهرت أورامهم تعبيراً قوياً عن هذه المجموعة المعتمدة على p53 كانوا يميلون إلى الاستجابة أفضل للعلاج الكيميائي مقارنة بمن كانت تعبيراتهم منخفضة، ما يشير إلى أن إسكات p53 بطرق غير جينية بفعل البيئة الورمية الملتهبة قد يفاقم النتائج السريرية.
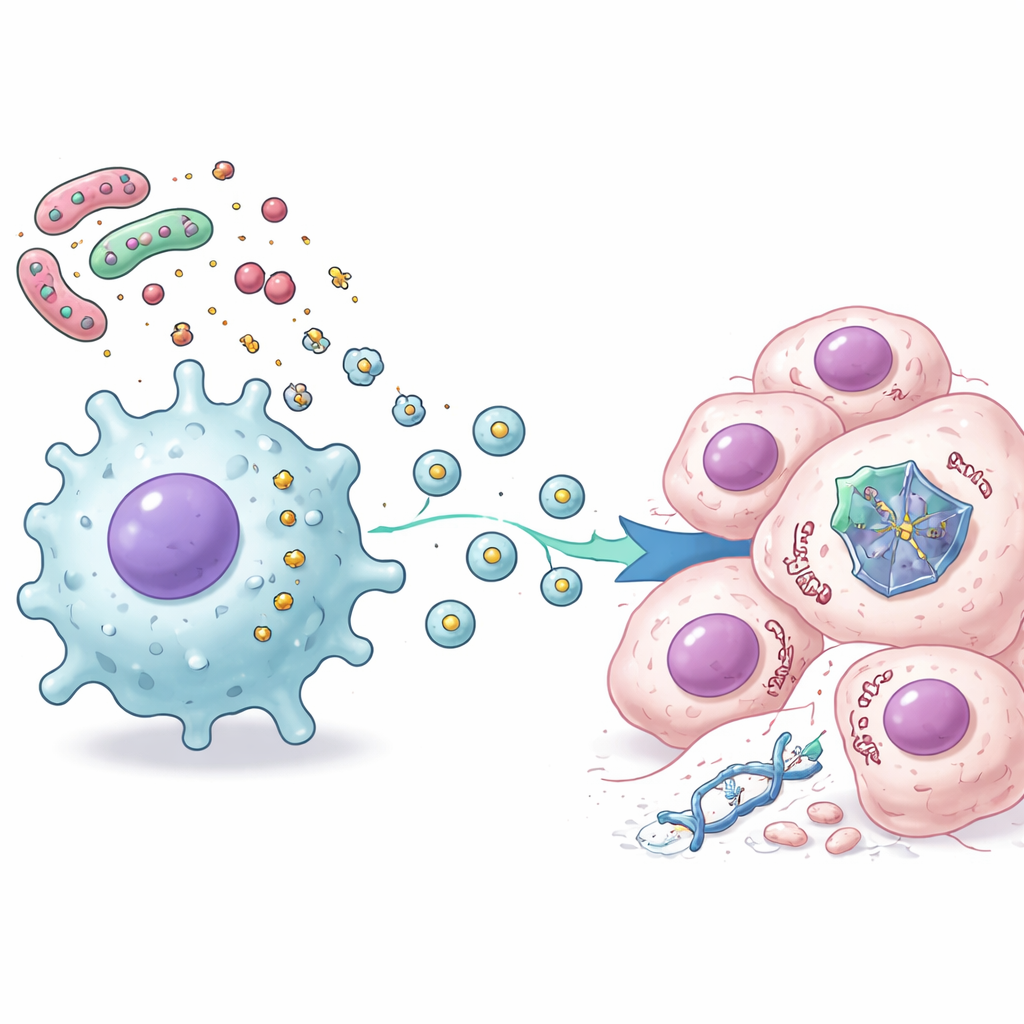
ماذا يعني هذا للمرضى والعلاجات
مجتمعة، تكشف النتائج عن سلسلة من الأحداث التي تربط بكتيريا الأمعاء بمقاومة العلاج الكيميائي: يُنشط LPS البكتيري الخلايا النسجية والمناعية المجاورة، هذه الخلايا تُطلق حويصلات خارج خلوية، وتدخل الحويصلات إلى خلايا السرطان لتزعزع استقرار بروتين p53 وتضعف قراراته بين الحياة والموت بعد المعالجة. حتى عندما يكون جين p53 طبيعياً، يمكن لهذا الضغط الخارجي أن يُخَمِّد دوره الوقائي بفعالية. بالنسبة للمرضى، يشير ذلك إلى أن حالة ميكروبيوم الأمعاء والالتهاب المحلي قد تفسر لماذا بعض أورام القولون والمستقيم تتحدى الأدوية القياسية. في المستقبل، قد تساعد استراتيجيات إعادة تشكيل ميكروبات الأمعاء، أو تهدئة الالتهاب الضار، أو منع إنتاج أو عمل هذه الحويصلات في استعادة قدرة p53 على كبح الورم وجعل العلاجات الكيميائية الحالية أكثر فاعلية.
الاستشهاد: Fragkoulis, K., Łasut-Szyszka, B., Végvári, Á. et al. Klebsiella pneumoniae LPS drives stromal-mediated repression of p53 and colorectal cancer chemoresistance. Cell Death Dis 17, 395 (2026). https://doi.org/10.1038/s41419-026-08756-4
الكلمات المفتاحية: سرطان القولون والمستقيم, ميكروبيوم الأمعاء, مقاومة العلاج الكيميائي, مثبط الورم p53, البيئة المجهرية للورم